编者按:疾病的正确诊断和合理治疗是患者和医务工作者共同的心愿。在广东省人民医院肿瘤中心, 吴一龙教授指导临床医生应用循证医学理论进行肿瘤的多学科综合治疗, 开展临床病例讨论。讨论会上各学科共同围绕一个病例或一个病种进行会诊, 临床、病理、B超、放射影像等资料齐全, 除相关科室提前准备的中心性发言外, 到会人员各抒己见, 气氛热烈。参会人员受益匪浅, 提高了对疑难病例的诊治水平。为了将他们的诊治经验传播出去, 让更多的临床医生获益, 我刊开辟“ 循证病例讨论” 栏目, 希望广大医务工作者关注此栏目。
患者XAK, 女, 30岁。2007年9月因右乳肿物于外院行右乳肿物切除活检术, 术中冰冻病理学结果提示右乳浸润性癌, 遂行右乳腺癌保乳术并右腋窝淋巴结清扫术。术后病理结果示:右乳浸润性导管癌, 各切缘阴性, 腋窝淋巴结2/11枚转移。TNM分期为pT2N1M0, Ⅱ B期。免疫组化:PR(-), ER(+++), CerbB2(-)。术后给予CAF方案(CTX 750 mg, d1、d8, 5-FU 750 mg, d1、d8, ADM 80 mg, d1)辅助化疗共6个疗程。化疗结束后开始予“ 三苯氧胺20 mg/d” 辅助内分泌治疗, 并予术后辅助放疗(右乳全乳、右锁骨上, 总剂量40 Gy)。放疗结束后未定期复查。
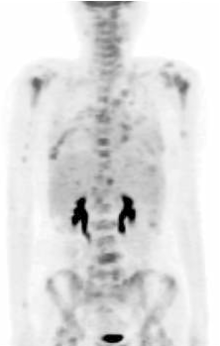
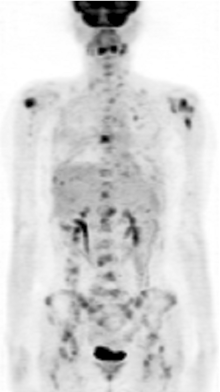
2009年5月患者自行发现右乳肿物, 遂于我院门诊行乳腺B超检查, 疑右乳腺癌保乳术后复发而收入院。入院后行PET检查示右乳腺癌保乳术后局部复发, 并全身多发性转移(见图1)。予化疗6周期后, 部分缓解。遂于2009年10月行右乳单纯切除术。术后病理结果示:(右侧) 乳腺浸润性导管癌, Ⅱ 级。肿瘤最大径无法准确评估; 未见明确脉管癌栓及神经束膜侵犯; 乳头及皮肤未见Paget’ s病; 各切缘及皮肤切缘均未见肿瘤。术后再予化疗2周期, 并予内分泌治疗, 嘱患者定期复查。
2010年4月, PET检查提示左上肺、肝左叶及全身多处骨髓新发病灶, 疾病进展。患者拒绝化疗, 改内分泌治疗方案维持。
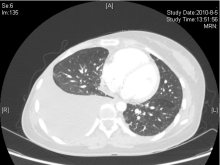
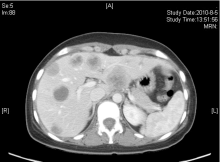
2010年8月, 胸腹部CT检查提示:双肺多发性转移癌, 右侧胸腔积液, 纵隔、肺门淋巴结肿大, 肝多发性转移瘤, 疾病进展。
诊断:右乳腺癌术后局部复发并全身多发转移, Ⅳ 期。
张国淳(肿瘤外科学博士):汇报病例特点(略)。本次讨论的主要内容为:(1)该病例既往治疗的循证评价。(2)该病例目前的治疗方案。
廖宁(肿瘤外科学副主任医师):患者为绝经前年轻女性, 分子分型为Luminal A型。保乳术后无病生存期(disease-free survival, DFS)短, 仅20个月。目前骨转移及内脏转移(双肺)同时存在, 无脑转移。复发风险的评估决定了初治时治疗方案的选择。该患者初治时< 35岁, 绝经前, 原发肿瘤pT1, 腋窝淋巴结阳性, 2/11, pN1, ER阳性, PR阴性, HER2阴性, Luminal A 型。可见该患者初治时是具有高复发风险的乳腺癌患者。那么该患者当初局部治疗方案采用保乳术是否恰当?
李学瑞(肿瘤外科学主治医师):年龄小于35岁的年轻乳腺癌患者行保乳手术目前仍然存在着争议。此类患者保乳术后局部复发的风险相对较高, NCCN指引亦将其列为保乳术的相对禁忌证。因此, 对于此类患者, 保乳手术必须慎重。如果患者强烈要求保乳, 外科医生应该与患者充分讨论, 令患者理解保乳手术后局部复发的风险后方可进行。
旁述:NCCN 2010年版乳腺癌临床指引中指出, 对于≤ 35岁的妇女, 由于已有研究结果显示≤ 35岁的年轻患者有相对高的复发和再发乳腺癌风险, 因此专家组提醒, 在选择保乳手术时, 医生应向患者充分交待可能存在的风险, 并据此将其列为乳腺癌保乳手术的相对禁忌证。
廖宁:循证医学的数据表明, 小于35岁的乳腺癌患者术后中位DFS约为20个月。该患者的DFS亦为20个月。因此, 尽管外院为其行保乳术值得商榷, 但并无太多不妥之处, 结合患者的DFS, 应属可以接受的范围。患者术后接受了6个周期的FAC方案辅助化疗, 治疗是否充分?
张国淳:我们利用Adjuvant !Online在线工具对该患者的化疗进行了评价。在把患者各项临床病理特征输入后发现, 该患者确实有极高的复发风险, 10年复发风险高达63%。而该患者采用蒽环类化疗方案进行辅助化疗, 10年无复发的临床获益可达22.3%。因此, FAC方案确实也大大降低了患者的复发风险, 是可以接受的辅助化疗方案。
郑登云(肿瘤内科主任医师):患者当时接受的FAC方案是临床指引推荐的一种方案, 尚算标准。然而, 根据目前的循证医学证据认为, 对年轻的腋窝淋巴结阳性的患者采用含紫杉类的方案可以明显降低复发风险, 但在Luminal A型的患者中则存在着争议。
廖宁:其实蒽环类与紫杉类都是乳腺癌化疗方案的基石。然而目前的证据大多数是10年甚至20年以前开展的临床试验, 存在的问题是缺乏根据分子分型分层的个体化治疗方案。目前乳腺癌已经进入以分子分型为基础的个体化治疗时代, 这些证据尽管级别很高, 但是否适合各种不同分子亚型仍然不得而知。因此, 紫杉类和蒽环类在Luminal A型乳腺癌中孰优孰劣并无明确的结论。因此, 6个周期的FAC方案是可以接受的标准治疗方案。该患者在化疗结束后接受了全乳放疗, 剂量为40 Gy, 但是没有进行瘤床加量放疗, 是否有所欠缺?
李伟雄(放射治疗学主任医师):乳腺癌保乳术后辅助放疗, 瘤床是否加量放疗目前尚无定论。一些研究表明瘤床加量可以降低40岁以下患者局部复发的风险, 但是绝对获益很少, 只有2%~3%。因此, 瘤床不加量放疗也是允许的。但该患者总剂量40 Gy略显不足, 常规的剂量是45~50 Gy。
廖宁:在化疗结束之后, 对于这样一个年轻的患者, 单用他莫昔芬内分泌治疗是否足够?
张国淳:对于绝经前ER阳性的乳腺癌患者, 他莫昔芬目前仍然是标准的内分泌治疗方案。然而近年新发表的一些证据则表明, 在年龄≤ 40岁的患者中, 他莫昔芬内分泌治疗同时加上药物卵巢去势则可以大大降低复发的风险, 幅度高达24.7%[1]。这也导致了今年出版的德国的AGO乳腺癌临床指引中出现了对小于35岁的患者强烈推荐药物卵巢去势联合他莫昔芬内分泌治疗的方案。因此, 该患者初治时仅用他莫昔芬内分泌治疗显得有所不足。
旁述:AGO 2010年版乳腺癌临床指引推荐在绝经前具有高危因素的小于40岁的乳腺癌患者中采用化疗序贯性腺激素释放激素(GnRH)类似物进行卵巢去势, 同时加用他莫昔芬内分泌治疗。证据级别为2a级。而卵巢去势的维持时间则推荐为2年。
陈晓明(介入治疗学主任医师):我们已经对该患者初治时的局部治疗与全身治疗手段进行了循证医学的评价。可以作如下的小结:①该患者初治时选择全乳切除术可能更为恰当; ②放疗总剂量略显不足; ③内分泌治疗方案应考虑加入卵巢去势; ④CAF辅助化疗6周期符合规范。那么该患者在复发转移后至目前为止的治疗方案应该作什么样的评价?
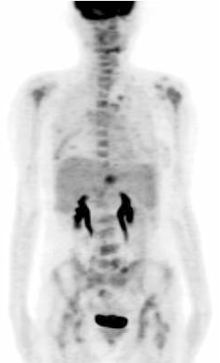
张国淳:该患者至我院治疗时局部复发及骨转移与内脏转移并存, 肿瘤负荷大, 应该考虑首选联合化疗。对于在辅助治疗中使用过蒽环类的患者, 复发转移后的一线治疗方案可以选择多烯紫杉醇联合卡培他滨(XT方案), 该方案的总有效率高于40%。该方案同时也是NCCN乳腺癌临床指引及AGO乳腺癌临床指引所强烈推荐的。因此, 我们在患者的一线治疗中采用了XT每3周方案。然而, 在化疗2个周期后我们又进行了一次PET的疗效评价, 结果显示:右侧乳腺、双肺多发结节、肝脏肿块、盆腔淋巴结及全身多处骨髓局灶性葡萄糖代谢异常增高灶, SUV较前明显降低; 与前一次本院PET影像比较, 可见新发病灶(肝脏), 见图2。那么如何评价此时的疗效呢?是否需要更换二线化疗方案?
廖宁:该患者的PET结果显示除肝脏新发病灶以外, 全身其它病灶均明显缩小, 代谢减弱。如果按照RECIST标准来衡量, 出现新病灶均应评价为疾病进展。然而, 在全身大部分病灶均明显缩小的情况下, 更换二线化疗方案是否可行?有无其它手段进行评价?
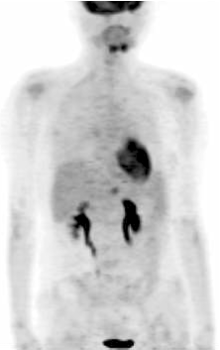
张国淳:目前对化疗效果的评价还有外周循环血肿瘤细胞(circulating tumor cells, CTC)检测这一手段。CTC检测已经被美国FDA批准为评价疗效的手段之一, 但尚未在中国正式上市。广东省人民医院乳腺科正在参与一项CTC检测用于转移性乳腺癌的多中心Ⅲ 期临床试验。因此, 该患者也加入了此研究。该患者开始一线治疗之前的CTC检测结果为185个/7.5 mL血, 而在2个周期后已经明显降低至92个/7.5 mL血。如果按照CTC检测的结果, 患者对XT方案的治疗是有效的, 不应该更换方案。因此, 我们为该患者制定了继续XT方案化疗的策略。在第4周期末时又进行了PET检查及CTC检测。PET结果显示:右侧乳腺结节、肝脏肿块局灶性葡萄糖代谢异常增高灶; 与前次PET影像比较, 原骨髓多发高代谢病灶明显减少, 葡萄糖代谢活性减低; 肝左叶转移灶缩小, 葡萄糖代谢活性减低, 提示化疗后转移瘤部分缓解, 见图3。而CTC检测的结果则显示:CTC数量为1个/7.5 mL血。因此, 在完成4个周期XT之后的疗效评价为部分缓解, 继续进行2个周期XT方案化疗。
旁述:外周循环血细胞检测技术已被美国FDA于2004年批准上市, 可用于监测转移性乳腺癌患者对治疗的反应、预测患者的预后。有研究表明, 与影像学检查方法相比, CTC计数能够更早期、更具重现性地提示疾病状态, 并且与总生存期的相关性优于传统的放射学检查[2]。
马冬(肿瘤内科学副主任医师):转移性乳腺癌一线治疗方案的疗效评价至关重要。然而, 单纯的影像学评价有时候会出现令人困惑的情况。此时结合非影像学的检查结果进行综合考虑是一种有效的解决方法。此例患者结合CTC检测结果, 采取了继续原方案的策略, 避免了贸然更换化疗方案造成治疗上的被动, 结果表明是十分正确的。
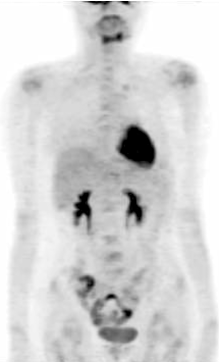
张国淳:该患者在完成了6个周期的XT方案之后又进行了一次PET疗效评价, 结果显示:与2009-08-25本院PET影像比较, 未见明确新发病灶, 原肝脏左叶病灶及乳腺病灶消失, 见图4。而CA15-3及CEA均降低至正常范围内。那么此时右乳局部复发灶是否应该进一步处理?
廖宁:对于转移性乳腺癌治疗之后的手术指征, 目前尚未达成明确的共识。但是全身病情控制良好的病例, 在局部病灶可以完全切除的情况之下, 是可以考虑进行局部手术的, 可以达到两个目的:一是避免局部病灶溃烂, 改善患者的生活质量; 二是有可能改善患者的长期生存。
张国淳:该患者在XT方案第6周期末时进行了右乳单纯切除术。术后病理检查结果示:(右侧)乳腺浸润性导管癌, Ⅱ 级。各切缘未见癌, 皮肤切缘均未见肿瘤。表明局部病灶已被完整切除。免疫组化结果仍为Luminal A型。此时该患者全身疾病控制良好, 局部病灶亦成功切除, 接下去的治疗策略应该是什么?是否采用XT方案维持治疗?
马冬:转移性乳腺癌的维持化疗目前亦没有共识。该患者可以采用原方案继续化疗2~4周期, 以后改内分泌维持治疗。
张国淳:该患者在术后再予2周期XT方案化疗后予内分泌维持治疗, 方案为戈舍瑞林卵巢去势加阿那曲唑, 并予氯膦酸二钠抗骨转移治疗。患者在2010年4月行PET复查时发现左上肺、肝左叶及全身多处骨髓局灶性葡萄糖代谢异常增高灶, 与前次PET影像比较, 以上均为新发病灶(见图5)。患者一线治疗的无进展生存期为8个月。患者此时拒绝化疗。改用依西美坦内分泌治疗。2010年8月复查胸腹部CT提示双肺多发性转移癌, 右侧胸腔积液, 纵隔、肺门淋巴结肿大, 肝多发性转移瘤, 多发性骨转移瘤, 提示疾病再次进展, 见图6和图7。患者此时同意任何形式的治疗, 包括化疗。那么此时应该如何选择治疗方案?
廖宁:该患者目前的治疗存在较大的困难。患者已经在辅助中接受过蒽环类化疗, 在一线治疗中又接受过紫杉类化疗。而内分泌治疗又接受过他莫昔芬、甾体类及非甾体类芳香化酶抑制剂。目前可选的化疗方案不多。新近上市的白蛋白结合型紫杉醇(Abraxane)是可以考虑的一个选择。循证医学证据显示, Abraxane 260 mg/m2每3周方案与紫杉醇175 mg/m2每3周方案相比用于转移性乳腺癌的一线治疗, 可将总体反应率从19%大幅提高至33%, 中位至疾病进展时间从16.9周提高至23周。Abraxane 100 mg/m2或125 mg/m2 d1、d8、d15每4周方案在紫杉类无效的转移性乳腺癌中的总体有效率仍可达到15%。因此, 我推荐选择Abraxane对该患者进行二线化疗[3, 4, 5]。
陈晓明:今天的病例讨论很好地体现了肿瘤中心乳腺科作为单病种专科的优势。对病例的手术、化疗、放疗、内分泌治疗都进行了充分的循证医学评价, 并在循证的基础上对患者制定了正确的治疗策略, 同时还结合最新的疗效评价手段CTC检测对患者进行了疗效的评价, 是有益的尝试, 也是本次病例讨论的一大亮点。患者接受Abraxane二线治疗后的效果如何, 大家将拭目以待。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|