作者简介:彭澍(1972-),女,江西余江人,主任医师,在读博士,主要研究心血管疾病的诊治。
目的 评价曲美他嗪在慢性心力衰竭患者中的应用价值。方法 应用Cochrane系统评价方法,检索1990年至2010年9月Cochrane 图书馆临床对照试验资料库、PubMed、EMBASE数据库,应用RevMan 5.0进行数据Meta分析,选择随机效应模型评价曲美他嗪对慢性心力衰竭的治疗效果。结果 共检索到122篇相关文献,经过评价,9个临床试验符合本设计的标准而入选。Meta分析显示,曲美他嗪联合常规抗心力衰竭治疗能够显著提高慢性心力衰竭患者的左心室射血分数[标准化均数差1.21,95%可信区间(0.99,1.42), P=0.000],可以显著减少左心室收缩末容积[标准化均数差-0.28,95%可信区间(-0.48,-0.07), P=0.008]和左心室舒张末容积[标准化均数差-0.72,95%可信区间(-0.96,-0.48), P=0.000]。结论 曲美他嗪对慢性心力衰竭的治疗具有积极的临床意义,与传统的抗心力衰竭药物联合应用,仍能够显示益处,临床受益与原发疾病无关。
Objective To evaluate the efficacy of Trimetazidine in combination with other traditional treatment agents in chronic heart failure patients.Methods We searched the Cochrane Central Register of Controlled Trials, PubMed, EMBASE, and identified randomized controlled trials on the effect of Trimetazidine in patients with chronic heart failure.Results Nine clinical trials meeting our criteria were identified and extracted. Results showed that Trimetazidine significantly reduced the LVEDV [95%CI(-0.48, -0.07), P=0.008] and LVESV [95%CI(-0.96, -0.48), P=0.000], and improve LVEF [95%CI(0.99, 1.42), P=0.000] in chronic heart failure patients.Conclusion The efficacy of Trimetazidine in the treatment of chronic heart failure was confirmed when used with conventional agents, in ischemic or non-ischemic cardiomyopathy.
代谢治疗是应用相关药物以提高心肌细胞功能[1]。曲美他嗪(Trimetazidine, TMZ)是该类药物中应用较多的一种。新近研究显示, TMZ通过选择性抑制长链3-酮酰基辅酶A硫解酶, 抑制氧化磷酸化和转移能量底物从脂肪酸到葡萄糖氧化[2], 改善衰竭心肌的能量代谢。然而, 有关TMZ对慢性心力衰竭患者的临床作用尚有争议[3, 4], 目前国内外在该领域已有临床和基础研究, 但单个研究的病例数较少, 结论尚存争议。本文即对TMZ治疗慢性心功能衰竭的临床试验进行系统评价, 用以评价TMZ对衰竭心肌的临床益处。
系统检索1990年至2010年9月Cochrane 图书馆临床对照试验资料库、PubMed、EMBASE数据库, 检索词:trimetazidine、dysfunctional myocardium 或 heart failure 或 left ventricular dysfunction 或 dilated cardiomyopathy 或 ischemic cardiomyopathy, 文献类型为randomized controlled trials、trial 或 clinical trial。检索目标为英文论著。
纳入研究均为随机、盲法(包括单盲和双盲)、对照研究, 研究目标为在常规抗心力衰竭治疗基础上联合应用TMZ对慢性心力衰竭的治疗效果。排除重复发表的研究和未设立对照组的研究; 一项研究观察时间为3天, 从临床治疗的角度认为时间过短可能导致结果偏倚, 予以排除。数据纳入由两位研究者独立完成。
有Meta分析认为治疗心力衰竭患者的指标改善包括左心室射血分数(left ventricular ejection fraction, LVEF)、左心室舒张末容积(left ventricular end-dilation volume, LVEDV)和左心室收缩末容积(left ventricular end-systolic volume, LVESV), 可以用来预测患者死亡率降低[5], 故本研究选用以上三个指标, 来评价TMZ对慢性心力衰竭患者的临床作用并预测对远期预后的影响。
分别对以上三个指标进行异质性分析, 根据分析结果选用合适的系统评价方法。应用RevMan5.0软件进行统计分析。异质性分析计算Z评分和卡方检验, 以α =0.1为检验水准。均数及标准差来自原始文献数据, 以P< 0.05表示差异有统计学意义。
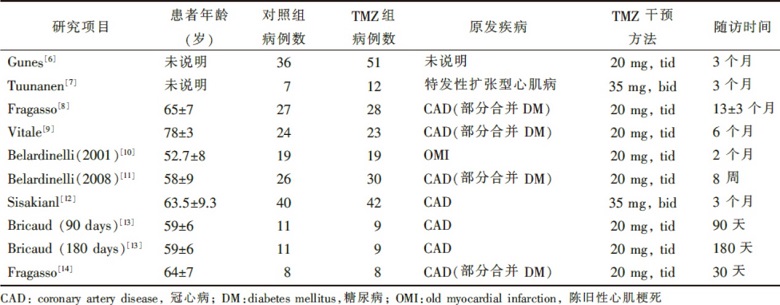
共检索到122篇文献, 经过筛选, 纳入9个研究, 均为盲法的随机对照研究。纳入研究的基本信息见表1。所有纳入研究均为英文文献, 入选患者病因不限, 基线LVEF< 45%, 排除了严重的心力衰竭患者; 部分研究包括了糖尿病患者, 其中有一项研究未说明原发疾病情况。各研究纳入对照病例的基线条件一致。
| 表1 纳入研究的基础情况 |
9项研究评价了LVEF、8项研究观察了LVEDV、7项研究观察了LVESV的变化。经过Meta分析提示, TMZ可以显著提高慢性心力衰竭患者的LVEF, 并缩小LVESV和LVEDV。
2.2.1 TMZ组和对照组治疗前后LVEF的变化
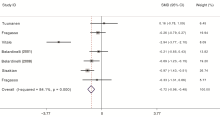
9项研究中有一项对纳入对象进行了两个阶段的观察和数据分析, 分别是90天和180天, 故在本分析时将其分别进行统计。异质性分析P< 0.1, 显示数据存在异质性, 采用随机效应模型进行进一步分析。分析显示, 与对照组对比, TMZ可以明显增加心力衰竭患者的LVEF值[标准化均数差(standard mean difference, SMD) = 1.21, 95%可信区间(confidence interval, CI)(0.99, 1.42), P= 0.000], 见图1。
Heterogeneity chi-squared = 44.74 (d.f. = 9) P= 0.000 Test of SMD = 0: Z = 11.21P = 0.000
2.2.2 TMZ组和对照组治疗前后LVEDV的变化
8项研究进行了治疗前后LVEDV的对比研究。异质性分析P< 0.1, 显示数据存在异质性, 采用随机效应模型进行进一步分析。分析显示, 与对照组对比, TMZ可以减少心力衰竭患者的LVEDV[SMD= -0.28, 95%CI(-0.48, -0.07), P=0.008], 见图2。
Heterogeneity chi-squared = 38.12 P= 0.000 Test of SMD = 0 : Z = 2.65 P = 0.008
2.2.3 TMZ组和对照组治疗前后LVESV的变化
7项研究进行了治疗前后LVESV的对比研究。异质性分析P< 0.1, 显示数据存在异质性, 采用随机效应模型进行进一步分析。分析显示, 与对照组对比, TMZ可以明显减少心力衰竭患者的LVESV值[SMD=-0.72, 95%CI(-0.96, -0.48), P=0.000], 见图3。
Heterogeneity achi-squared = 37.68 P = 0.000 Test of SMD = 0 : Z = 5.95 P = 0.000
心力衰竭的治疗传统上着眼于血流动力学的改善。然而, 虽然改善血流动力学的药物不断进展, 心力衰竭的治疗并未因此有令人鼓舞的结果。事实上, 衰竭心肌存在左心室需求和心肌能量摄入不平衡, 被称为机械-能量失偶联。新近研究显示在不影响氧摄入和血流动力学的情况下, 应用增强心肌能量的药物, 可能会提高心肌做功。大多数研究者致力于研究可以将能量物质利用从脂肪酸代谢转向糖代谢的药物, TMZ是其中为数不多的一种。TMZ对于缺血心肌的作用在早期的荟萃分析中已得到肯定, 但对于该类药物对衰竭心肌作用的研究, 目前主要针对基础机制和临床疗效, 但样本量均较少, 而且并未得到统一结果; 此类药物在对改善衰竭心肌作用的可能机制亦未完全阐明。本荟萃分析基于既往的9个随机对照研究, 认为TMZ联合心力衰竭常规系统治疗可能可以帮助改善左心室功能, 不论心力衰竭基于何种原发疾病均可以受益。另外, 对于增大的左心室容积, TMZ似乎表现出临床额外获益, 在伴或不伴糖尿病的心力衰竭患者中均得到类似结论。有Meta研究认为治疗心力衰竭患者的指标改善包括LVEF、LVEDV和LVESV可以用来预测心力衰竭患者死亡率降低[5], 因此本分析结论的得出可能可以推测, TMZ尚可以有效降低心力衰竭患者的住院率和死亡率。
TMZ对衰竭心肌的作用机制可能有以下几点。(1)代谢调节作用。TMZ可以直接抑制脂肪酸氧化[15, 16], 故称为3-酮酰基辅酶A硫解酶抑制剂。抑制氧化磷酸化和脂肪酸基质可以使基质利用从脂肪酸向葡萄糖转化, 并且在此过程中机体的胰岛素抵抗已经证明能够明显降低, 空腹血浆高密度脂蛋白浓度得以升高11%[17], 这或许可以解释TMZ使糖尿病患者受益。然而, 在本Meta分析中未得到TMZ与糖尿病患者的直接相关关系, 因为在纳入的研究中糖尿病患者是作为一个部分纳入到研究的, 而没有把糖尿病患者分开, 作为一个群体研究对象来进行研究。(2)对心肌代谢的直接作用。在不同基础疾病引起的心力衰竭的动物模型所做的实验中可以观察到一个共同现象, 磷酸肌酸(phosphocreatine, PCs)和游离肌酸因消耗而引起降低[18, 19]。总体肌酸水平和肌酸激酶活性在扩张型心肌病患者是降低的[20], 并与左心室功能障碍的不同分级呈正相关关系[21, 22]。基于此, 对于心力衰竭的治疗, 旨在提高PCr/ATP比例是目前的研究方向, 已有临床试验证明血管紧张素转换酶抑制剂和β 受体阻滞剂具有可以降低患者死亡率的作用, 至少部分是由于改善了心肌的能量转化。有趣的是, 新近研究显示, 血管紧张素转换酶抑制剂和β 受体阻滞剂在心功能衰竭患者中亦发挥出和TMZ类似的降低游离脂肪酸利用的作用, 降低血浆游离脂肪酸或直接抑制脂肪酸氧化可以提高丙酮酸酯氧化和心肌对能量的有效利用[23, 24]。这亦可以解释TMZ能提高心室功能和使扩大的心腔逐渐恢复。(3)心肌缺血会加重炎症, 这是这类患者再住院率和死亡率高的原因之一; TMZ可以改善缺血心肌的炎症状态[25], 而且可以提高心肌细胞对心肌超负荷的抵抗能力, 而这种现象与心力衰竭往往并存。
本Meta分析尚存在一定局限性。首先, 纳入的临床试验样本量均较小, 观察时间为3~6个月, 很难得出有关TMZ与临床硬终点诸如死亡率或住院率的结论, 而这些指标才是评价药物疗效的金指标; 其次, TMZ已经被证实可以改善缺血性心肌病患者的临床症状及预后。本研究所纳入的临床试验中研究对象的基础心脏病大多数是冠心病, 这样就会出现偏倚:冠心病患者缺血改善, 也可以帮助心脏功能的提高。另外, 研究对象中未排除糖尿病, 也就是未能排除TMZ由于对血糖代谢的益处进而会产生部分偏倚。所以, 大规模的相关临床试验, 特别是对于非缺血性心肌病心力衰竭的患者进行相关研究, 并且观察时间能够相对延长, 方有望得到TMZ在常规治疗基础上是否能够确实减少心力衰竭患者死亡率的确凿资料。
在慢性心力衰竭患者的最优治疗方案中加入TMZ可能可以通过代谢途径进一步提高心脏功能, 并缩小左心室容积, 从而改善生活质量, 并可能对预后有积极地影响。加大样本量并延长观察时间, 有望得到TMZ对慢性心功能衰竭患者再入院率和死亡率等临床观察终点疗效的确切资料。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|