| 黄诚, 福建省肿瘤医院肿瘤内科主任, 主任医师, 福建医科大学肿瘤内科教研室主任, 教授, 福建省肿瘤化学治疗质量控制中心主任。兼任中国抗癌协会肺癌专业委员会常委, 中国癌症康复与姑息治疗专业委员会常委。中国抗癌协会临床肿瘤学协作专业委员会执行委员, 中国抗癌协会临床肿瘤学协作专业委员会小细胞肺癌专业委员会副主任委员, 中国抗癌协会临床肿瘤学协作专业委员会血管靶向治疗专家委员会委员及生物标志物专家委员会委员。福建省肺癌专业委员会主任委员, 福建省癌症康复与姑息治疗专业委员会主任委员, 福建省化疗专业委员会副主任委员; 《中国肺癌杂志》、《临床肿瘤学杂志》、《中国肿瘤临床与康复》、《JTO》中文版等杂志编委。长期从事肿瘤内科的临床和科研工作, 并且参加多项国际多中心临床研究项目, 在省级以上核心刊物发表学术论文50多篇, 获省级以上科技成果奖2项。 |
中图分类号: R734.2 文献标识码:: A 文章编号:1671-5144(2012)01-0026-03
Spigel DR, Townley PM, Waterhouse DM, et al. Randomized phaseⅡ study of Bevacizumab in combination with chemotherapy in previously untreated extensive-stage small-cell lung cancer:Results from the SALUTE trial[J]. J Clin Oncol, 2011, 29(16): 2215-2222.
1b。
• 铂类与依托泊苷或伊立替康双药联用是治疗小细胞肺癌(small cell lung cancer, SCLC)的标准方案。但其治疗后的中位无进展生存期(progression-free survival, PFS)仅为2~6个月, 中位总生存期(overall survival, OS)为9~10个月。因此需要寻找新的治疗策略改善SCLC患者的预后。
• 贝伐单抗(Bevacizumab, BV)是一种抗血管
内皮生长因子(vascular endothelial growth factor, VEGF)单克隆抗体。已有三项关于BV与含铂化疗联用治疗初治广泛期SCLC的单组Ⅱ 期临床研究显示较好的疗效和总生存期。
• 对于初治广泛期SCLC患者, BV与标准化疗联用的疗效是否优于一线标准化疗方案目前尚不清楚。
评估BV联合标准一线化疗方案治疗初治广泛期SCLC的疗效和安全性。
• 研究条件: 美国田纳西州那什维尔Sarah Cannon研究所, 内布拉斯加州奥马哈Methodist Estabrook肿瘤中心肿瘤专家组, 俄亥俄州辛辛那提肿瘤学/血液学中心, 加利福尼亚南旧金山基因泰克公司, 北卡罗莱纳大学莱恩伯格综合肿瘤中心。
• 研究方法:多中心、随机、双盲、安慰剂对照Ⅱ 期临床研究。
• 研究起止日期:2007年3月至2009年2月。
• 研究对象:初治广泛期SCLC患者。
患者的入选标准为:组织学或细胞学检查明确诊断为广泛期SCLC, 包括有小细胞成分的混合性肿瘤; 从未接受过化疗; 年龄≥ 18岁, PS评分0~2分。
排除标准包括:有咯血、心肌梗死、不稳定型心绞痛、卒中、短暂性脑缺血发作、明显的血管疾病、周围动脉血栓形成、腹壁瘘等病史, 或者入组前6个月内曾患胃肠道穿孔; 高血压控制不良或有高血压危险及高血压脑病病史; 除SCLC脑转移之外的中枢神经系统疾病; ≥ 2度充血性心力衰竭; 出血体质或缺乏抗凝治疗的凝血性病; 全麻手术史; 入组前28天内有切开活检史或跌打损伤者; 有未愈合的严重伤口, 活动性溃疡, 或有未治疗的骨折; 蛋白尿(筛选时尿蛋白/肌酐比≥ 1); 药物过敏史; 孕妇。
• 评价指标:主要终点为PFS; 次要终点包括OS、总有效率(overall response rate, ORR)及客观有效时间。
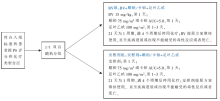
• 干预措施:随机接受标准一线化疗+BV或标准一线化疗+安慰剂治疗(见图1)。
与标准一线化疗方案相比, BV联合化疗可改善广泛期SCLC患者的PFS, 毒性反应尚可接受, 但是不能改善患者的OS。
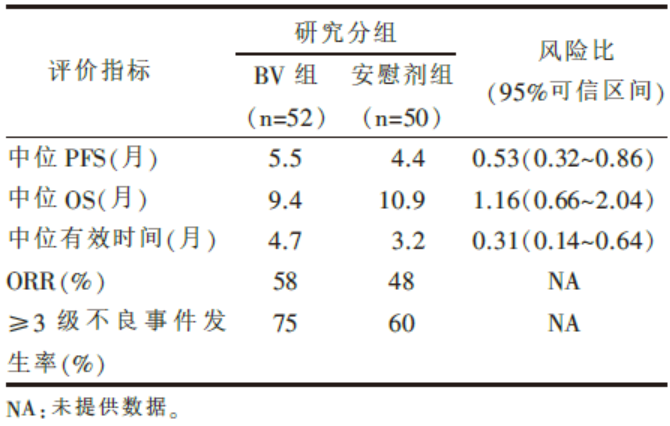
近二十年来, 小细胞肺癌的治疗模式及具体方案基本上没有发生明显变化, 一线化疗的标准方案仍然是顺铂或卡铂+依托泊苷的联合化疗。广泛期SCLC, 应用EP方案可使总有效率达到60%~80%, PFS 2~6个月, OS 为9~10个月。探索SCLC新的有效治疗方法和药物也是目前的一个研究热点, 但至今为止并未取得实质性突破[1]。近年来, 一些小样本的研究报道SCLC患者的血管内皮生长因子水平较高, 且可能与肿瘤分期、疾病进展、化疗耐药以及预后不良有关[2, 3, 4]。以往3个单臂的Ⅱ 期临床试验研究贝伐单抗联合化疗一线治疗广泛期SCLC的疗效, 研究结果显示了较为诱人的前景[5, 6, 7]。在这些研究的基础上, SALUTE临床试验应运而生, SALUTE临床试验是一项前瞻性、随机对照、双盲、多中心Ⅱ 期临床试验, 比较贝伐单抗与安慰剂联合标准EP方案一线治疗广泛期SCLC的疗效与安全性, 主要研究终点是PFS。研究结果显示:两组PFS 5.5个月(95%可信区间 4.5~6.7个月) vs. 4.4个月(95%可信区间 4.2~4.9个月), 风险比0.53(95%可信区间 0.32~0.86); 两组的OS 9.4个月(95%可信区间 8.7~11.3个月) vs. 10.9个月(95%可信区间 8.1~14.7个月), 风险比1.16(95%可信区间 0.66~2.04); 两组ORR 58% vs. 48%, P=0.326 9; 安全性方面, 两组≥ 3度不良反应发生率75% vs. 60%。该临床研究整体研究设计、统计方法合理, 研究结果达到其主要研究终点PFS的延长, 结果具有较高的可信度, 让我们再次看到贝伐单抗联合化疗可以进一步提高SCLC治疗疗效的希望。
但是对于该项临床研究结论应用于临床实践尚需谨慎, 原因如下:
第一, 该研究为Ⅱ 期临床试验, 样本量偏少, 直接体现在风险比的95%可信区间较宽, 因此, 在解读该临床试验数据时尚需谨慎。而且, 研究虽然获得了主要研究终点PFS的延长, 但PFS延长并没有转化为OS的延长, 这项研究结果仍需Ⅲ 期随机对照临床试验(以OS为研究主要终点)的进一步证实。
第二, 该篇文献中尚有需关注的问题。该项研究预先设置了两个分层因素, 一个是ECOG评分(0~1 vs. 2), 另一个是铂类(顺铂vs. 卡铂)。首先, ECOG评分是SCLC的一个独立预后因子, 在本试验中, 虽然在ECOG 0~1分与2分患者入组人数达到均衡, 但在ECOG 0~1分的分层中, 贝伐单抗组ECOG评分0分的患者人数明显多于安慰剂组, 两组分别为23 (46%)和15(29%), 这可能对两组的PFS、OS产生一定的影响, 但文献中并没有对其影响进一步分析。其次, 本研究另外一个分层因素是铂类, 在样本量较少的情况下, 临床试验设计应尽量减少其他混杂因素的干扰以及分层因素的设置, 如果以单纯一种铂类作为治疗方案, 可能更能凸显贝伐单抗对治疗结果以及安全性的影响, 同时也就避免了该研究中对卡铂与顺铂分层分析中难以解释的现象。另外, 该研究中, 两组有效率为58%vs.48%, 完全缓解率均为0, 与既往文献报道的有效率、完全缓解率相比偏低, 是否为研究误差还是入组人群的个体差异等其他原因, 尚待分析。
第三, 在我们看到希望的同时, 我们也要清醒地认识到:从Ⅱ 期临床试验的数据推测, 即使Ⅲ 期临床试验结果能够在统计学意义上证实贝伐单抗联合化疗可以提高广泛期SCLC的总生存期, 但其实际临床意义可能比较有限。另一方面, 一些同样具有抗肿瘤血管形成作用的药物, 如:索坦、索拉菲尼、Cediranib、沙利度胺、Vandetanib在临床试验中均未取得令人满意的疗效[8, 9, 10, 11, 12]。这里面, 是否存在具体药物的选择因素、究竟抗血管形成在SCLC有无作用仍有待进一步明确, 因此, 在目前我们对肿瘤血管形成在SCLC的作用及其地位所知甚少的情况下[13], 重视临床与基础的研究结合, 从分子角度进一步深入探讨。
综上所述, 在目前SCLC治疗疗效停滞不前阶段, SALUTE临床试验让我们看到了贝伐单抗联合化疗可能提高SCLC疗效的希望, 但研究结论应用于临床仍有相当一段距离, 进一步深入基础研究为抗肿瘤血管形成治疗策略在SCLC中的应用提供坚实的基础。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|