作者简介:汪雁博(1983-),女,河北秦皇岛人,博士研究生,从事心血管病学研究。
目的 对不同代谢途径他汀类药物联用氯吡格雷对急性冠脉综合征患者血小板功能和主要不良事件的影响进行系统评价。方法 检索PubMed、EMBASE、Cochrane图书馆、中国生物医学文献数据库、中国期刊全文数据库、维普中文科技期刊、万方数字化期刊群自创建至2011年6月发表的关于不同代谢途径他汀类药物联用氯吡格雷对急性冠脉综合征患者血小板功能影响的文献,并追踪已获文献的参考文献。由2名研究者独立进行质量评价和数据提取。采用RevMan 4.2.8 软件进行Meta分析。结果 共纳入11项随机对照研究,共计1 923例患者。Meta分析结果显示,不同代谢途径他汀类药物与氯吡格雷联用对急性冠脉综合征患者住院期间血小板聚集率的影响没有显著性差异(加权均数差0.39,95%可信区间-1.84~2.62, P=0.73),而接受经CYP3A4代谢的他汀类药物与氯吡格雷联用治疗的急性冠脉综合征患者P-选择素水平较低(加权均数差-1.16,95%可信区间 -1.77~-0.54, P=0.000 2),接受不同代谢途径的他汀类药物与氯吡格雷联用时,急性冠脉综合征患者1个月内的主要不良心脏事件发生率没有显著性差异(比值比1.07,95%可信区间0.77~1.49, P=0.69)。结论 不同代谢途径他汀类药物与氯吡格雷联用对急性冠脉综合征患者的血小板功能和主要不良心脏事件发生率可能无明显影响,但仍需大规模临床试验加以证实。
Objective To evaluate the effects of different statins (CYP3A4 metabolized statins and CYP2C9 metabolized statins) combined with Clopidogrel on the platelet functions in patients with acute coronary syndrome (ACS) by meta analysis.Method Both foreign and Chinese databases including PubMed, EMBASE, Cochrane library, and CNKI were searched to identify randomized controlled trials (RCTs) that reported the effects of different statins combined with Clopidogrel on the platelet functions and major adverse cardiac events (MACE). Two reviews assessed the quality of each trial and extracted data independently. The Cochrane Collaboration’s RevMan 4.2.8 software was used for statistical analysis.Results A total of 11 RCTs were included, and the methodological quality of each trial was good. There was no significant difference in platelet aggregation rate when different types of statins were used(WMD=0.39, 95%CI -1.84~2.62, P=0.73), as well as the incidence of MACE(OR=1.07, 95%CI 0.77~1.49, P=0.69). However, the level of P-selectin was lower in patients received CYP3A4 metabolized statins (WMD=-1.16, 95%CI -1.77 ~ -0.54, P=0.000 2).Conclusion Both statins metabolized with and without CYP3A4 were safe for ACS patients.
血小板二磷酸腺苷(adenosine diphosphate, ADP)受体拮抗剂氯吡格雷是目前急性冠脉综合征(acute myocardial infarction, ACS)双联抗血小板药物治疗的基石[1]。作为前体药物, 氯吡格雷在肝脏经细胞色素P450(CYP)3A4酶代谢转化为活性代谢产物, 通过二硫键不可逆地连接到血小板表面的P2Y12 ADP受体上, 进而抑制ADP受体依赖性的血小板糖蛋白Ⅱ b/Ⅲ a复合物的形成来抑制血小板的聚集[2]。以往研究表明, 以阿司匹林和氯吡格雷为基础的双联抗血小板治疗可以显著改善ACS患者的预后[3]。但是临床实践也发现, 部分患者在接受常规剂量的双联抗血小板治疗后, 仍反复发生动脉血栓事件, 即出现氯吡格雷抵抗现象, 严重影响患者的治疗效果和临床预后[4, 5]。产生氯吡格雷抵抗的原因主要包括患者个体差异、疾病状态和药物之间的相互作用[6, 7]。
他汀类药物因具有降低低密度脂蛋白、抑制炎症、稳定斑块等多种有益作用而广泛应用于冠心病患者[8]。部分他汀类药物(阿托伐他汀、辛伐他汀和洛伐他汀)在体内需要经CYP3A4代谢, 可能竞争性抑制氯吡格雷的代谢过程, 从而影响氯吡格雷的抗血小板作用, 导致产生氯吡格雷抵抗。而普伐他汀和氟伐他汀等他汀类药物不需要经过CYP3A4代谢, 因而可能对氯吡格雷的抗血小板作用影响较小。2003年, Lau等[9]的临床观察和实验室研究结果发现阿托伐他汀与氯吡格雷可能存在相互作用, 引起学者和临床医生的高度关注。
目前尚缺乏不同代谢途径他汀类药物与氯吡格雷联用对ACS患者血小板功能影响的大规模随机对照研究。本研究旨在采用Meta分析的方法, 回顾性总结目前已发表的关于不同代谢途径他汀类药物联用氯吡格雷对ACS患者血小板功能影响的文献, 并对其进行系统评价。
检索PubMed、EMBASE、Cochrane图书馆、中国生物医学文献数据库、中国期刊全文数据库、维普中文科技期刊、万方数字化期刊群。各数据库检索时间均从创建至2011年6月。英文检索词为: clopidogrel、statin、platelet、acute myocardial syndrome, 同时进行 MeSH 及自由词检索。中文检索词为:氯吡格雷、他汀、血小板、急性冠脉综合征。另外, 用 Google、Medical Martix等搜索引擎在互联网上查找相关的文献, 再根据已发表文献的参考文献进行文献追溯。最后根据文题及摘要查找出与本研究有关的文献并获取全文。
1.2.1 纳入标准
纳入同时符合以下条件的研究文献:(1)研究类型为随机对照试验; (2)文献中病例的要求:①研究对象为ACS患者, 接受或未接受经皮冠状动脉介入治疗(percutaneous coronary intervention, PCI); ②接受标准双联抗血小板治疗; ③接受常规剂量他汀治疗; (4)文献的评价标准中至少符合本研究选用的3项疗效判定指标(如下所述)中的一项。
1.2.2 排除标准
(1)研究文献的样本已被收录, 且其可提供的评价指标数据已被收录; (2)所能找到的文献或其摘要不能提供完整、有效数据者; (3)使用血小板膜糖蛋白GPⅡ b/Ⅲ a受体拮抗剂进行治疗; (4)文献样本中包含了有使用氯吡格雷或他汀类药物治疗绝对或相对适应证的患者。
(1)住院期间血小板功能检测:①血小板聚集功能检测, 采用比浊法测定ADP诱导的血小板聚集率(platelet aggregation rate, PAR); ②血小板活化功能检测P-选择素(P-selectin); (2)发病1个月随访期间的主要不良心脏事件(major adverse cardiac events, MACE)。
由2名评价员独立进行文献筛选和质量评价, 按预先设计的表格提取资料。如遇分歧讨论解决或交第三者判定。缺乏的资料尽量与作者联系予以补充。对纳入文献的全文, 依据 Cochrane 系统评价员手册 4.2.6 的文献质量评价方法进行评价。基于以上标准将纳入研究分为 3个等级:A(低度偏倚):所用的评价指标均正确; B(中度偏倚): 有一项或一项以上指标未描述; C(高度偏倚):有一项或一项以上指标不正确或未使用。
所有统计分析均通过RevMan 4.2.8 软件进行。分类变量采用比值比(odds ratio, OR)及其 95%可信区间(confidence interval, CI)为疗效分析统计量, 连续性变量采用加权均数差(weighted mean difference, WMD)及 其95%CI 为疗效分析统计量。Meta 分析时, 首先用χ 2检验对纳入研究进行同质性检验, 若P> 0.05, 选择固定效应模型进行分析; 反之, 则使用随机效应模型。
初检相关文献41篇, 经阅读后排除不符合条件的文献30篇, 最终纳入11篇[9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19]。其中10篇文献对住院期间不同代谢途径的他汀类药物与氯吡格雷联用时的血小板聚集率进行了比较, 5篇文献对住院期间P-选择素进行了比较, 4篇文献对短期(1个月内)的MACE发生率进行了比较(表1)。
| 表1 各纳入研究的特征 |
2.3.1 血小板聚集率比较
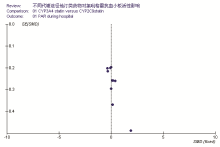
共纳入10项研究[9, 10, 11, 13, 14, 15, 16, 17, 18, 19], 各研究间有统计学异质性(I2=69.1%), 故采用随机效应模型进行Meta分析。结果显示:接受不同代谢途径的他汀类药物与氯吡格雷联用治疗时, ACS患者的血小板聚集率没有显著性差异(WMD=0.39, 95%CI-1.84~2.62, P=0.73), 见图1。
2.3.2 P-选择素比较
共纳入5项研究[11, 14, 16, 18, 19], 各研究间无统计学异质性(I2=45%), 故采用固定效应模型进行Meta分析。结果显示:接受经CYP3A4代谢的他汀类药物与氯吡格雷联用治疗时, ACS患者住院期间的P-选择素水平较低(WMD=-1.16, 95%CI -1.77~-0.54, P=0.000 2), 见图2。
2.3.3 随访1个月内MACE发生情况的比较
共纳入4项研究[10, 11, 12, 13], 各研究间无统计学异质性(I2=0%), 故采用固定效应模型进行Meta分析。结果显示:接受不同代谢途径的他汀类药物与氯吡格雷联用治疗时, 随访期间(1个月内)的MACE发生率没有显著性差异(OR=1.07, 95%CI 0.77~1.49, P=0.69), 见图3。
本研究纳入了不同代谢途径的他汀与氯吡格雷联用对ACS患者血小板聚集率、P-选择素以及MACE 3项指标影响的随机对照研究, 采用Cochrane系统评价方法对纳入的11项原始研究进行方法学质量评价和Meta分析, 涵盖病例1 923例。
系统研究的结果显示, 不同代谢途径的他汀类药物与氯吡格雷联用对ACS患者血小板聚集率的影响没有显著性差异, 而接受经CYP3A4代谢的他汀类药物与氯吡格雷联用治疗的ACS患者P-选择素水平较低, 不同代谢途径的他汀类药物与氯吡格雷联用对ACS患者1个月内的MACE发生率没有显著性影响。上述结果与先前其他研究的结果基本一致。
氯吡格雷是当前ACS双联抗血小板治疗的基石药物, 可以显著改善患者的临床预后。但是, 由于多种药物与氯吡格雷具有相同的代谢途径(CYP3A4), 因此可能影响氯吡格雷的代谢及其抗血小板作用。他汀类药物具有多重心血管保护作用, 是目前ACS治疗的重要药物。但是早期研究显示, 部分他汀类药物, 因与氯吡格雷具有相同的代谢途径, 可能降低氯吡格雷抗血小板治疗的效果, 进而导致MACE发生率的增加[9]。尽管此后的多项研究对此进行了分析[18, 20], 但目前尚无大规模随机对照研究的观察结果。
由于氯吡格雷主要通过抑制ADP诱导的血小板聚集达到其抗血小板治疗的作用, 因此临床常用ADP诱导的血小板聚集率作为监测血小板聚集程度的指标, 反映血小板的聚集程度和氯吡格雷的治疗效果[21, 22]。本研究采用Meta分析的方法, 对不同代谢途径他汀类药物与氯吡格雷联用时ACS患者血小板聚集率和MACE发生率进行Meta分析, 结果显示应用不同代谢途径的他汀类药物对血小板聚集率和MACE发生率无明显影响。
P-选择素不仅是活化血小板的特异性标志物, 而且在血栓形成过程中起重要作用。因此, P-选择素检测是反映血小板活化程度和功能状态的灵敏指标, P-选择素的升高可作为血栓疾病的病情监测和评价血栓前状态的有效指标[23, 24]。本研究显示氯吡格雷与CYP3A4代谢途径的他汀类药物联用时P-选择素的水平较低, 产生这一结果的原因, 一方面与不同他汀类药物降脂、抗炎的多效性作用不同有关, 另一方面与本研究纳入的研究较少、样本量较少有关, 因此还有待大规模的研究进行观察分析。
由于系统评价为二次研究, 其论证强度受到纳入研究的质量等多种因素的影响, 因此存在一定的局限性。首先, 本研究纳入的研究较少, 样本量较小; 其次, 对于他汀类药物的使用仅进行了针对代谢途径的简单分类, 对具体他汀类药物的使用未作限制; 第三, 对于血小板聚集率和P-选择素的检测仅要求在住院期间血药浓度达到稳态后进行(3~14天), 但未对具体检测时间进行要求; 此外, 各组的随访时间有所不同, 可能对分析结果产生影响。
综上所述, 不同代谢途径的他汀类药物与氯吡格雷联用可能并未对ACS患者的血小板聚集率和MACE产生显著影响, 但是仍需大规模临床试验加以证实。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|