| 科室带头人陆骊工教授为全国介入医学领域知名专家, 广东省干部保健专家, 广东省人民医院(广东省医学科学院)肿瘤中心副主任, 介入治疗科主任, 主任医师, 医学博士, 博士研究生导师, 卫生部医政司介入诊疗技术管理专家组成员, 卫生部办公厅成立的全国肿瘤规范化诊疗专家委员会委员, 原发性肝癌规范化诊疗推广项目委员, 广东省医师学会介入医师工作委员会副主任委员、广东省中西医结合学会肿瘤分会常委、广东省中西医结合学会影像专业委员会常委, 广东省介入治疗学组副组长, 具有南方医科大学、汕头大学、中山大学附属第三医院及广东省心血管病研究所硕士研究生导师资格; 目前承担广东省科委重大科技支撑项目、广东省卫生厅、广州市科技等多项课题的研究。 |
Kudo M, Imanaka K, Chida N, et al. Phase Ⅲ study of Sorafenib after transarterial chemoembolisation in Japanese and Korean patients with unresectable hepatocellular carcinoma [J]. Eur J Cancer, 2011, 14(47): 2117-2127.
2a。
• 肝细胞癌(hepatocellular carcinoma, HCC)是全球第五大肿瘤, 且是仅次于肺癌和胃癌的癌症第三大死因。目前全球每年新发病例超过65万例, 且四分之三的发病人数在东亚国家。 HCC起病隐匿, 大多数患者在确诊时已达局部晚期或已经远处转移, 仅30%~40%的患者适合接受手术、肝移植等根治性治疗。
• 对于失去手术机会的部分中晚期患者, 经导管肝动脉化疗栓塞(transarterial arterial chemoembolisation, TACE)治疗可以控制疾病、延长生存。但TACE的远期疗效并不理想, 5年生存率低于10%, 且其术后复发率较高。
• 最近几年, 新型分子靶向药物索拉非尼(多吉美)治疗晚期肝癌受到关注。2008年在欧美国家完成的SHARP及2009年在亚太地区完成的AP两项Ⅲ 期临床试验表明, 索拉非尼能延长晚期HCC患者的中位生存期、进展时间。
• 索拉非尼已先后获得美国FDA、欧洲医药评价署(EMEA)及中国SFDA批准, 成为治疗晚期HCC的标准用药。
评价韩国、日本不能切除的原发性肝癌患者在行TACE后服用索拉非尼的有效性及安全性。
• 研究条件:包括韩国7家研究中心、日本69家研究中心的一项双盲、安慰剂对照的Ⅲ 期临床试验。拜耳及玛瑙医药公司提供主要资助。
• 研究起止时间:2006年4月27日至2009年7月10日。
• 研究方法:多中心、双盲、安慰剂对照前瞻性随机对照研究。
• 研究对象:2个国家、76个研究中心的458名患者。
入组条件:不能切除的原发性肝癌患者; 年龄≥ 18岁; 在TACE术后1~3个月Child-Pugh评分为A级; 预期寿命≥ 12周; 目标病灶最大直径小于70 mm; ≤ 10个目标病灶; ECOG PS评分为0或1; 嗜中性粒细胞绝对值≥ 1 000/mm3; 血小板计数≥ 50× 109/L; 国际标准化比值≤ 2.3或凝血酶原时间≤ 6 s; 肝功能和肾功能指标适宜。
排除条件:有血管侵袭、肾功能不全、心脏病、感染HIV病毒、有临床症状的脑部及脑膜转移、肝外转移、需要药物治疗的癫痫、晚期肝癌患者接受过系统的全身治疗(但是在接受有效的全身治疗后辅助使用干扰素、类维生素A、维生素K2是允许的)、在开始服用研究药物前3周使用造血生长因子等制剂、在最后一次TACE后辅助应用细胞因子疗法、器官移植、有滥用药物病史、妊娠或哺乳期。
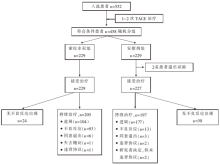
• 干预措施:入选552例晚期原发性肝癌患者在接受1~2次TACE治疗后, 将符合入组标准的458例患者随机分为索拉非尼组(400 mg/d, n=229)及安慰剂组(n=229)。试验的流程图见图1。
• 评价指标:主要终点指标是疾病进展时间(time to progression, TTP), 定义为完全缓解(complete remission, CR)的病人出现复发的时间, 或未完全缓解(NON-CR)的病人出现新病灶或肿瘤大小增加≥ 25%的时间; 次要终点指标是总生存期(overall survival, OS), 定义为从随机化分组到任何原因导致死亡的时间。
本项研究最终入组458名患者, 随机分为索拉非尼组400 mg/d(n=229)及安慰剂组(n=229)。组间的平均年龄、性别、ECOG PS评分、病灶的数目、病原学、TACE次数、TACE术后反应、以前接受过局部治疗均无显著差异。
76家中心回顾结果显示:中位TTP, 索拉非尼组为5.4个月(95%可信区间为3.8~7.2个月), 安慰剂组为3.7个月(95%可信区间为3.5~4.0个月), 风险比(hazard ratio, HR)为0.87(95%可信区间为0.70~1.09), P=0.252。
中位OS, 索拉非尼组为29.7个月(95%可信区间为28.6个月~NE), 安慰剂组为NE(95%可信区间为NE~NE), 风险比为1.06(95%可信区间为0.69~1.64), P=0.790。
NE:由于数据不完整故不存在结果。
研究者对超过人数10%患者进行了中位疾病进展时间的探索性亚组分析, 亚组分析因素包括病原学(乙型肝炎vs. 丙型肝炎)、TACE术后反应、病灶的数目、TACE次数、年龄、性别、从最近一次TACE到随机化分组的时间间隔、ECOG PS评分、入选国籍。
探索性亚组的中位疾病进展时间, 索拉非尼组为7.2个月(95%可信区间为5.6~9.1个月), 安慰剂组为5.3个月(95%可信区间为3.8~5.6个月), 危险比为0.79, 95%可信区间为0.62~1.00, P=0.049。索拉非尼在某些特定的人群显示出一定疗效, 包括男性、年龄小于65岁、TACE术后与服用索拉非尼间隔的时间较短、较长的治疗时间、每天较高的总剂量。
在日本及韩国不可切除的肝细胞癌患者行肝动脉化疗栓塞术后使用索拉非尼并未延长其中位疾病进展时间及总生存时间。但探索性亚组分析显示:索拉非尼在某些特定的人群显示出一定疗效, 包括男性、年龄小于65岁、TACE术后与服用索拉非尼间隔的时间较短、较长的治疗时间、每天较高的总剂量。
索拉非尼(Sorafenib, 商品名Nexavar, 多吉美), 作为新型的分子靶向药物, 属于多激酶抑制剂, 它一方面可以抑制受体酪氨酸激酶 KIT 和 FLT-3以及 Raf/ MEK/ ERK途径中丝氨酸/苏氨酸激酶, 从而抑制肿瘤细胞增殖; 另一方面它可以通过上游抑制受体酪氨酸激酶血管内皮生长因子(vascular endothelial growth factor, VEGF)受体和血小板衍化生长因子(platelet derivation growth factor, PDGF)受体及下游抑制 Raf/ MEK/ERK途径中丝氨酸/苏氨酸激酶, 从而抑制肿瘤新生血管的形成。因此它具有抗肿瘤血管生成和抑制肿瘤细胞增殖双重作用[1]。Llovet等报道的著名的SHARP研究(即索拉非尼与安慰剂对照治疗晚期肝细胞癌的多中心、随机、Ⅲ 期临床研究)证实:索拉非尼是第一个可显著延长肝细胞癌患者OS的分子靶向药物, 并确立了索拉非尼在晚期肝癌治疗中的一线地位[2]。与此类似, 在亚洲国家进行的Oriental研究也取得了和SHARP相一致的结果[4]。SHARP研究和Oriental研究证明了索拉非尼可显著延长肝细胞癌患者的OS和无病进展时间, 且耐受性良好。
肝癌是一种富血管的恶性肿瘤, 肿瘤的生长代谢、浸润转移和复发均与肿瘤的血液供应密切相关, VEGF过表达及其信号通路的激活在肿瘤进展和血管生成中发挥着重要作用。TACE在栓塞肿瘤血管的同时会上调VEGF, 索拉非尼的作用机制之一就是抑制血管内皮生长因子(VEGF-2、VEGF-3)、血小板衍化生长因子( PDGF-p)等多种受体的酪氨酸激酶活性, 下调VEGF的表达水平, 因此理论上, 这二者联合使用可以扬长避短, 并且可以获得任何一种单一治疗方案都无法获得的治疗效果。国内外大量文献也报道过TACE联合索拉非尼优于单纯TACE或索拉非尼:黄振等[3]报道了45例不伴有远处转移的晚期或进展期肝细胞癌患者, 口服索拉非尼治疗, 其中18例联合TACE (1~5次), 27例单用索拉非尼, 证实病变局限在肝内且不合并远处转移的晚期或进展期肝细胞癌患者, 口服索拉非尼联合TACE不增加并发症发生率, 且生存预后改善; Strebel等[4]研究结果也证实TACE之后造成缺氧环境, 诱导VEGF表达增加、血管生成 , 联合索拉非尼治疗可以有效抑制血管再生, 减少肿瘤复发、转移 , 提高肝癌的治疗效果。
但该文献中所述的此项双盲、安慰剂对照的Ⅲ 期临床试验却得出结论:在日本及韩国不可切除的肝细胞癌患者行肝动脉化疗栓塞术后使用索拉非尼并未延长其中位疾病进展时间及总生存时间。
究竟是何种原因所致本文献所述的此项临床研究与之前国内外报道过的大量文献结论截然不同呢?从本文献所述的背景介绍中不难看出, 在亚洲大多数国家大约有70%的原发性肝癌患者有慢性乙肝病毒感染的病史, 但在日本的原发性肝癌患者约有75%有慢性丙肝病毒感染的病史。且在本项试验中, 日本的原发性肝癌患者占84.5%(387/458), 韩国的原发性肝癌患者仅占15.5%(71/458)。入组病人的基础疾病不同, 有可能是导致不同结果的原因之一。
从试验设计来说, 本项临床试验是一个设计较为合理的多中心, 随机对照研究。两组患者的临床特征是均衡的, 脱落率低, 试验过程也严格按照试验设计进行, 因此该研究结果真实可靠。
从试验结论而言, 本项临床试验得出:在日本及韩国不可切除的肝细胞癌患者行TACE术后使用索拉非尼并未明显延长其中位疾病进展时间及总生存时间。但探索性亚组分析显示:索拉非尼在特定人群中可以获得明显的临床效益。这些特定人群包括男性、年龄小于65岁、在TACE术后较短时间内服用索拉非尼。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|