作者简介:李青(1983-),女,山东泰安人,在读博士研究生,主要研究方向为循证医学与中医临床疗效评价。
目的 评价使用免疫球蛋白对甲型肝炎暴露前和暴露后的预防效果及其安全性。方法 电子检索Cochrane肝胆病组对照试验注册中心、Cochrane临床对照试验注册中心、Medical Literature Analysis and Retrieval System Online、Excerpta Medica Database、Science Citation Index Expanded、中国生物医学文献数据库等,手工检索3种中文杂志,收集免疫球蛋白预防甲型肝炎的随机对照试验,以甲型肝炎的发病率为主要结局,效应指标用相对危险度及其95%可信区间表示。结果 共纳入13篇文献(567 476名患者),2/3的文献偏倚风险较高。对于甲肝暴露前的预防:免疫球蛋白与空白或安慰剂相比能够显著降低成年人及儿童6~12个月内的甲肝发病率( P均<0.05);随访第4周时免疫球蛋白与灭活甲肝疫苗相比在促抗-HAV抗体阳转方面差异没有统计学意义( P>0.05),但在随访第8、12、24周时,灭活甲肝疫苗在促抗-HAV抗体阳转方面的效果优于免疫球蛋白( P均<0.05);高剂量与低剂量相比能够显著降低甲肝的发病率( P均<0.01)。对于甲肝暴露后的预防:免疫球蛋白的预防效果优于安慰剂( P<0.01)。13篇文献未报告明显的全身不良事件。结论 使用免疫球蛋白对甲型肝炎暴露前和暴露后的预防有一定效果,但是由于纳入的文献数量有限、发表年代久远及存在高偏倚风险,应慎重对待这一结论,应该设计更为严格的随机对照试验进行验证。
Objective To assess the efficacy and safety of the pre-exposure and post-exposure prophylaxis with immunoglobulins for preventing hepatitis A.Methods We searched The Cochrane Hepato-Biliary Group Controlled Trials Register, the Cochrane Central Register of Controlled Trials in The Cochrane Library, Medical Literature Analysis and Retrieval System Online, Excerpta Medica Database, Chinese Biomedical Database, and Science Citation Index Expanded for randomized trials, and hand searched three Chinese journals. Randomized clinical trials on immunoglobulin prophylaxis for preventing hepatitis A were collected, the primary outcome was incidence of hepatitis A, and the results were presented as relative risks (RR) with 95% confidence intervals.Results Thirteen trials with 567 476 participants were included, and two thirds of the 13 trials had high risk of bias. For pre-exposure prophylaxis, immunoglobulin significantly reduced the number of adults or children patients with hepatitis A at 6 to 12 months compared with no intervention or inactive control ( P<0.05). There was no significant difference between immunoglobulin and inactivated hepatitis A vaccine in seroconversion to hepatitis A vaccine antibodies at four weeks ( P>0.05), but immunoglobulin was significantly less effective than vaccine regarding antibody levels at 8, 12, or 24 weeks ( P<0.05). Higher dosage was generally more effective than lower dosage in preventing hepatitis A ( P<0.01). For post-exposure prophylaxis, immunoglobulin was more effective than placebo ( P<0.01). No significant systemic adverse events were reported.Conclusions Immunoglobulins seem to be effective for pre-exposure and post-exposure prophylaxis of hepatitis A. However, caution is warranted for the positive findings due to the limited number of trials, old publication, and risk of bias. Further well-designed randomized controlled trials are expected for rigorous evidence.
甲型肝炎是人类已知的最古老的疾病之一, 它是由感染甲型肝炎病毒(hepatitis A virus, HAV)引起的, 主要通过粪-口途径传播, 其严重程度随着感染时年龄的增高而增高[1], 在一小部分病人中能够引起暴发性肝炎或死亡。HAV是导致世界许多国家人口死亡和社会经济损失的重要原因[2, 3, 4, 5], 全世界每年有140万人感染临床期明显的甲型肝炎[6, 7]。
自1940年起, 就有研究认为免疫球蛋白对甲型肝炎暴露前的预防有效[8], 但使用人血浆免疫球蛋白预防甲肝存在一定风险(如逆转录病毒HIV的传播、丙型肝炎或克-雅氏病), 因此, 很多经济发达的国家和地区已不再使用免疫球蛋白来预防甲型肝炎[9], 但在很多不发达国家, 免疫球蛋白仍被广泛应用。
针对以上现状, 有必要系统地评价免疫球蛋白预防甲型肝炎暴露前和暴露后的效果和安全性, 以获得免疫球蛋白预防甲型肝炎的疗效及安全性的证据, 为甲型肝炎暴露前和暴露后的预防提供循证医学证据。
1.1.1 研究类型
使用免疫球蛋白预防甲型肝炎的所有随机对照试验(randomized controlled trial, RCT), 对是否采用盲法、发表状态、发表语言或随机化单位(个体或群体)均不作限制。
1.1.2 研究对象
处于甲肝暴露前或暴露后阶段的人群(年龄、种族不限)。
1.1.3 干预措施
试验干预为免疫球蛋白制剂, 对免疫球蛋白的类型、剂量、用法均不作限制; 对照干预为空白、安慰剂、灭活甲肝疫苗; 免疫球蛋白联合甲肝疫苗与单用甲肝疫苗比较的试验、免疫球蛋白不同剂量或不同滴度比较的试验也予以纳入。
1.1.4 结局评价指标
主要结局指标包括甲肝发病率、亚临床期甲肝发病率。次要结局指标包括抗-HAV抗体水平、不良事件及例数、成本效益。
半随机试验和历史对照临床试验。
电子检索Cochrane肝胆病组对照试验注册中心(2010年10月)、Cochrane临床对照试验注册中心(2010年第3期)、Medical Literature Analysis and Retrieval System Online(1966年至2010年10月)、Excerpta Medica Database(1980年至2010年10月)、 Science Citation Index Expanded (1945年至2010年10月)、中国生物医学文献数据库(2010年10月)、中国重要会议论文全文数据库(http://www.bucm.edu.cn)。英文检索词为:hepatitis A; immune prophylaxis; immunoglobulin; prevention; random; controlled。中文检索词为:甲型肝炎; 甲肝; 免疫预防; 免疫球蛋白; 预防; 随机; 对照。此外, 手工检索《中华流行病学杂志》(1981-2010年)、《中华传染病杂志》(1983-2010年)、《中华预防医学杂志》(1953-2010年)。查阅纳入文献的参考文献以补充资料。对文献的语种不作任何限制。
由两名作者按照事先确定的纳入和排除标准对文献进行独立筛选, 并按照事先设计的资料提取表对英文文献进行独立提取, 遇有分歧通过讨论解决。非英文文献(如俄文)委托丹麦哥本哈根大学Dimitrinka Nikolova提取资料, 并与作者协商讨论。提取的资料包括第一作者、研究方法、研究场所、研究对象(平均年龄、种族、男性构成比)、随机分组病例数、失访例数、纳入及排除标准、干预措施(剂量、用法、联合干预)、结局指标、不良事件及例数等。
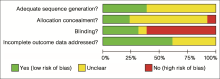
主要从随机序列的产生、随机分配方案的隐藏、盲法及随访的完整性四个条目对纳入文献的方法学质量进行评价[10, 11, 12, 13]。对于每一个条目, 如果满足(yes)则意味着低度风险; 不满足(no)则意味着高度风险; 当文献中未报告足够的信息让我们对相应条目作出明确的yes或no的判断时, 则将该条目定为不清楚(unclear)。如果四个条目均为yes时意味着低风险(方法学质量高), 如果有1条或1条以上为unclear或no时意味着高风险(方法学质量低)[12]。
采用Cochrane协作网提供的RevMan5.0软件进行资料的统计分析[14]。二分类变量用相对危险度(relative risk, RR)及其95%可信区间(confidence interval, CI)表示, 连续变量用均数差(mean difference, MD)及其95%CI表示。采用固定效应模型和随机效应模型进行资料的统计分析, 如果两种模型存在差异, 则分别报告两种模型的结果; 采用P值和I2评价各研究间的异质性, 如果P< 0.1, 则认为异质性检验有统计学意义, 如果I2> 50%, 则认为存在高异质性, 当异质性检验有统计学意义时选择随机效应模型的结果。可以根据免疫球蛋白剂量、随访时间长短、儿童或成年人、甲型肝炎高发区或低发区等进行亚组分析。
根据拟定的检索策略, 初步检索到文献1 077篇, 经阅读文献标题和摘要, 排除1 056篇, 得到全文21篇, 通过阅读其参考文献又补充获得3篇, 其中, 11篇因不属于RCT或研究目的与本系统评价不符而被排除, 最终共纳入文献13篇[15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26], 其中1篇文献未发表。包括8篇英文文献和5篇俄文文献, 共567 476名患者。11篇文献研究甲肝暴露前的预防, 2篇文献研究甲肝暴露后的预防[15, 26]。7篇文献以儿童为研究对象[15, 17, 18, 19, 22, 26], 6篇文献以成年人为研究对象[16, 20, 21, 23, 24, 25]。13篇文献中, 7篇为组群RCT, 分别以部队、班级或幼儿园为随机分配单位, 各随机分配单位大小不固定。1篇文献报告免疫球蛋白联合甲肝疫苗与单用甲肝疫苗比较[23], 6篇文献报告了不同剂量或滴度的免疫球蛋白之间的比较[16, 18, 19, 22, 24]。纳入研究报告的结局指标主要为发生临床或亚临床期甲肝的人数、抗-HAV血清转换。随访时间最长18个月, 最短1个月。4篇文献报告了不良事件[16, 23, 25, 26], 没有文献报告成本效益。
6 篇个体RCT中, 3篇描述了随机序列产生及随机隐藏方法[15, 16, 26], 3篇虽有“ 随机分组” 字样, 但未报告有关随机序列产生、随机隐藏的信息[22, 23, 25]。3 篇使用双盲[15, 16, 26], 1篇对病人使用盲法[23]。由于组群RCT不同于个体RCT, 故采用CONSORT声明扩展版从以下四方面对其方法学质量进行评价:采用组群设计的原理、在计算样本量时如何考虑群集效应、在分析时如何考虑群集效应、整群和个体从分配到分析的流程图[27]。7篇组群RCT均未报告采用组群设计的原理, 仅1篇介绍了样本量的估计[24], 在分析或结果解释中均未考虑群集效应, 均未报告整群和个体从分配到分析的流程图。1篇文献报告了病例失访[23], 1篇文献报告病例失访、退出例数及其原因并进行意向性分析[26], 其余文献均报告在试验过程中未出现病例失访。总的来说, 有1/3的文献偏倚风险较低, 方法学质量较高, 其余的偏倚风险均较高, 方法学质量低下, 见图1。
2.3.1 暴露前预防
2.3.1.1 免疫球蛋白与空白或安慰剂治疗的比较
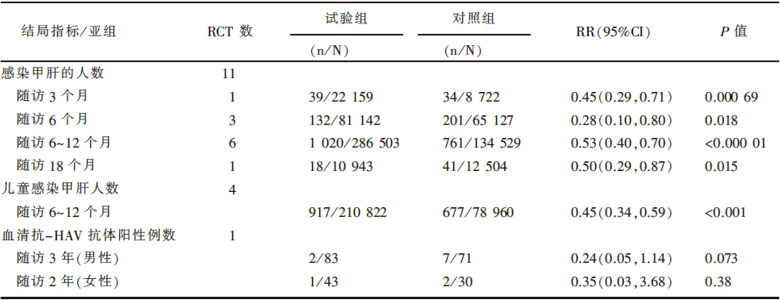
见表1。11篇文献报告免疫球蛋白与空白或安慰剂比较, 随访3个月、6个月、6~12个月、18个月时, 免疫球蛋白与空白或安慰剂相比均能显著降低甲肝发病率, 差异有统计学意义(P均< 0.05)。4篇文献比较免疫球蛋白与安慰剂预防儿童甲肝的效果, 随访6~12个月时免疫球蛋白与安慰剂相比能够显著降低甲肝发病率, 差异有统计学意义(P< 0.001)。分别对男、女性进行的为期3年、2年的随访发现, 免疫球蛋白与空白或安慰剂相比在促抗-HAV抗体血清阳转方面差异没有统计学意义。
| 表1 免疫球蛋白组与空白或安慰剂治疗针对甲肝暴露前预防的效果比较 |
2.3.1.2 免疫球蛋白联合甲肝疫苗与单用甲肝疫苗或单用免疫球蛋白的比较
1 篇文献报告免疫球蛋白联合甲肝疫苗与单用甲肝疫苗或单用免疫球蛋白的比较[23], 三组相比在降低甲肝发病率方面差别均没有统计学意义(P均> 0.05); 初次接受免疫4周后免疫球蛋白联合甲肝疫苗组与单用甲肝疫苗组均能检测到抗 -HAV抗体, 但单用甲肝疫苗组抗-HAV抗体滴度的几何均数是免疫球蛋白联合甲肝疫苗组的1.8~2.9倍。
2.3.1.3 免疫球蛋白与灭活甲肝疫苗的比较
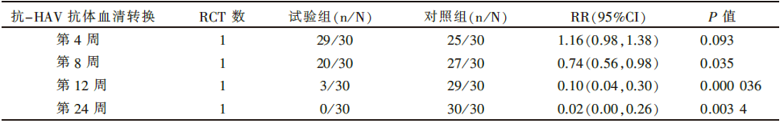
1篇文献比较免疫球蛋白与灭活甲肝疫苗的效果[25], 结果见表2。第8、12、24周时, 免疫球蛋白促进抗-HAV抗体血清阳转的效果低于灭活甲肝疫苗, 其差别有统计学意义(P均< 0.05)。
| 表2 免疫球蛋白组与灭活甲肝疫苗针对甲肝暴露前预防的效果比较 |
2.3.1.4 免疫球蛋白不同剂量或不同滴度的比较
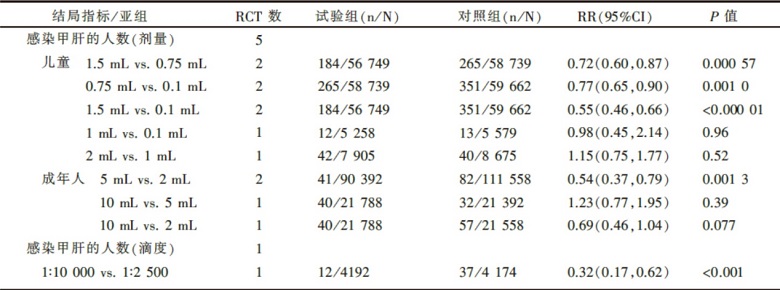
见表3。对于儿童甲型肝炎的预防, Meta分析结果表明1.5 mL在降低甲肝发病率方面的效果优于0.75 mL, 0.75 mL剂量在降低甲肝发病率方面的效果优于0.1 mL, 1.5 mL剂量在降低甲肝发病率方面的效果优于0.1 mL, 在另一未发表文献中, 高滴度免疫球蛋白(1∶ 10 000)预防甲肝的效果优于低滴度免疫球蛋白(1∶ 2 500)。对于成年人甲型肝炎的预防, Meta分析结果表明5 mL的预防效果优于2 mL。
| 表3 免疫球蛋白组不同剂量或不同滴度的预防效果比较 |
2.3.1.5 在甲型肝炎高发区与低发区使用免疫球蛋白的比较
1篇文献报告显示[18], 与空白组比较, 在甲肝高发区和低发区使用免疫球蛋白均能显著降低甲肝的发病率, 其RR值及95%CI分别为0.50(0.41, 0.60)与0.64(0.48, 0.84)。然而该作者后来所做的一项研究却表明如果分别在高发区与低发区使用滴度为1∶ 1 000的免疫球蛋白预防甲肝效果没有显著性差别, 但当使用滴度为1∶ 2 500的免疫球蛋白时, 在低发区的预防效果则显著优于高发区[22]。
2.3.1.6 不良事件
3篇文献提到不良事件, 其中1篇报告两组均未观察到明显严重的不良事件[25]; 1篇报告两组分别有13%、30%的人在注射部位出现局部反应(如疼痛、红肿、硬结或肿胀), 1例在使用免疫球蛋白后出现类似流感样的症状[16]; 1篇报告整个试验过程中所有研究对象均未出现任何不良事件[23]。
2.3.2 暴露后预防
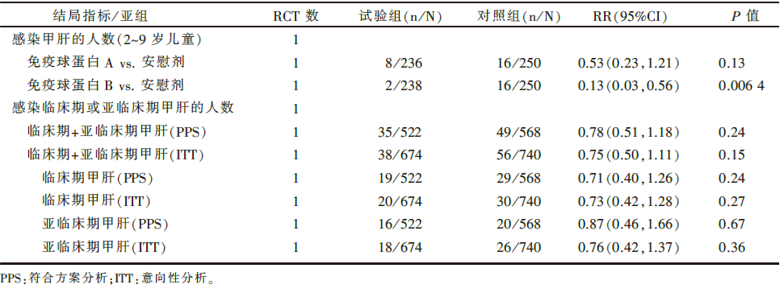
见表4。1篇文献比较两种不同类型免疫球蛋白(A和B)与安慰剂预防儿童(2~9岁)甲肝暴露后2周内的效果, 结果表明免疫球蛋白B与安慰剂相比能够显著降低甲肝发病率, 其差别有统计学意义(P< 0.01)[15]。1篇文献报告免疫球蛋白与灭活甲肝疫苗相比在预防临床期、亚临床期或临床期合并亚临床期甲型肝炎的效果上差异均没有统计学意义[26]。2篇文献均未报告不良反应, 但1篇报告共发生28例严重不良事件, 包括25例甲肝, 1例阑尾炎, 1例红疹, 1例中重度支气管炎, 但这些均与干预措施无关[26]。
| 表4 免疫球蛋白与安慰剂或灭活HAV疫苗针对甲肝暴露后预防的效果比较 |
本系统评价的研究结果提示:与空白或安慰剂治疗相比, 免疫球蛋白在甲肝暴露前的预防中具有良好的效果; 免疫球蛋白联合甲肝疫苗与单用甲肝疫苗相比在预防甲肝的效果方面没有显著性差异; 根据各研究报告的结果[28, 29, 30], 免疫球蛋白可能会为成年人暴露前的预防提供4~6个月保护期。但由于多数文献发表年代较早且方法学质量较低, 解释以上结果时应慎重。
《美国科学院儿科传染病委员会指南》推荐使用免疫球蛋白进行甲肝暴露后的预防, 尤其是针对那些在家中、儿童护理中心等场所与甲肝患者接触过的人[31]。在本系统评价中, 1篇以安慰剂对照的研究表明免疫球蛋白对急性传染性肝炎暴露后的预防有一定疗效[15]。最近发表的1篇低偏倚风险研究表明免疫球蛋白与甲肝疫苗相比在预防甲肝效果方面没有显著性差别, 建议可以用甲肝疫苗代替免疫球蛋白进行甲肝暴露后的预防[26]。
虽然本研究检索范围较广, 但仅检索到少数符合纳入条件的RCT, 6篇个体RCT在设计方法、场所、研究对象、干预措施及随访时间方面差异较大, 7篇组群RCT在随机分配单位的性质、大小方面也存在差异, 将个体RCT与组群RCT合并可能并不恰当[32], 因此在解释结果时应该慎重, 要考虑到各个研究之间的异质性; 本研究纳入的文献中既包括英文文献也包括俄文文献, 涉及不同的国家和地区, 由于种族的差异, 不同种族背景的国家对同一年龄阶段使用的剂量可能会不一致, 这也可能会造成免疫球蛋白预防甲型肝炎的效果存在差异。此外, 由于多数文献发表于10年甚至20年以前, 且方法学质量低下, 这些均影响研究结果的真实性。未有文献报告使用免疫球蛋白后发生不良事件, 仅有少数出现局部注射部位不适, 但仍然需要提防艾滋病、克雅氏病等血液传染病。
在某些情况下, 免疫球蛋白可以代替甲肝疫苗对暴露前的甲型肝炎进行预防, 但要考虑特殊场所(如日间护理中心、托儿所、小学)及特殊人群(如1岁以下儿童、年老者、感染艾滋病病毒者或其它免疫力低下者); 在进行试验期间要监测并报告与血液传染相关的不良事件; RCT与组群随机对照试验的报告规范均应遵照CONSORT声明。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|