|
黄诚,福建省肿瘤医院肿瘤内科主任,主任医师,福建医科大 学肿瘤内科教研室主任,教授,福建省肿瘤化学治疗质量控制中心 主任。兼任中国抗癌协会肺癌专业委员会常委,中国癌症康复与姑 息治疗专业委员会常委。中国抗癌协会临床肿瘤学会执行委员、小 细胞肺癌专家委员会副主任委员、血管靶向治疗专家委员会委员 及生物标志物专家委员会委员。福建省肺癌专业委员会主任委员, 福建省癌症康复与姑息治疗专业委员会主任委员, 福建省化疗专 业委员会副主任委员。《中国肺癌杂志》、《临床肿瘤学杂志》、《中国 肿瘤临床与康复》、《J Thorac Oncol》中文版等杂志编委。长期从事 肿瘤内科的临床和科研工作, 并且参加多项国际多中心临床研究 项目,在省级以上核心期刊发表学术论文60 多篇,获省级以上科 技成果奖2 项。 |
Yang JJ, Chen HJ, Yan HH, et al. Clinical modes of EGFR tyrosine kinase inhibitor failure and subsequent management in advanced non-small cell lung cancer[J]. Lung Cancer, 2013,79(1):33-39.
2a。
•表皮生长因子受体(epidermal growth factor receptor, EGFR)酪氨酸激酶抑制剂(tyrosine kinase inhibitor, TKI)吉非替尼和厄洛替尼对晚期非小细胞肺癌有明显疗效。但是大多数都会发展到吉非替尼、厄洛替尼治疗失败。
•许多治疗失败的患者有继发的EGFR T790M突变、c-MET扩增,或者二者同时存在。有TKI治疗失败模式多样性的零星报道,包括临床症状的迅速恶化或中枢神经系统的侵犯。
•目前尚无公认的EGFR-TKI治疗失败模式的总结。
对EGFR-TKI治疗失败模式进行分类,并探索应用这种临床模式对患者的后续治疗及预后评价的应用价值。
•研究条件:广东省人民医院。
•研究性质:单中心/回顾性研究。
•研究时间:2003年6月至2011年8月。
•研究对象: 120名来源于TRST、IPASS、OPTIMAL、CTONG 0901(NCT 01024412)临床试验的接受EGFR-TKI治疗的患者,另外107名接受常规TKI治疗的患者。
入组条件:病理确诊的局部晚期或转移性的非小细胞肺癌,EGFR-TKI治疗后疾病控制时间>3个月。
•评价指标:终点指标为无进展生存期(progression-free survival,PFS),进展后生存期(post-progression survival,PPS)和总生存期(overall survival,OS)。
•研究设计:分组的变量参考标准:临床定义为获得性EGFR-TKI耐药,RECIST标准,新的肺癌分期系统,三个临床因素(疾病控制时间、肿瘤负荷增长和临床症状)。
临床症状包括以下六项:咳嗽、咯血、胸痛、发热、气促、转移病灶相关的症状。
将227名患者的临床数据在Bayes判别模型中进行分析,将患者分为三组,对患者的后续治疗方法与预后进行分析。
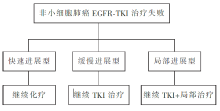
治疗失败模型分别定义为快速进展型、缓慢进展型和局部进展型。
120名来自临床试验的患者为训练集(training set),在Bayes判别模型中分析了以上三个因素和临床症状,得到三组的判别公式:
快速进展型=-16.19+0.39X+0.24Y+3.50Z+9.03S
缓慢进展型=-16.82+0.51X+0.98Y+2.08Z+5.30S
局部进展型=-10.08+0.35X+0.52Y+1.26Z+7.00S
这些数据在107名来自常规治疗患者的验证集(validating set)中也有87.9%的正确率。
基于以上数据,得到三种治疗失败模型的标准定义,见 表1。
| 表1 EGFR-TKI治疗失败模型的标准定义 |
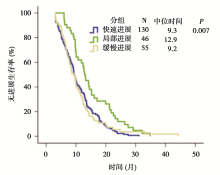
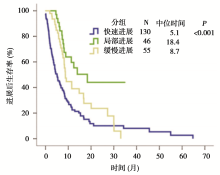
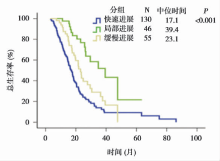
三种治疗失败模型的中位PFS、中位PPS和中位OS有差异,见 图1~4。
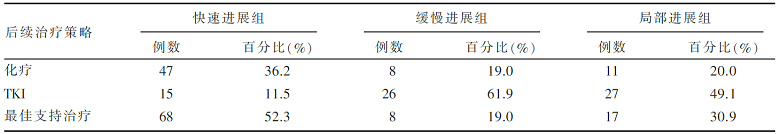
三组的后续治疗策略见 表2。
| 表2 三组的后续治疗策略 |
在快速进展、缓慢进展、局部进展的失败模式中,继续使用EGFR-TKI与改用化疗相比,中位OS分别为18.6个月 vs. 23.9个月( P=0.07)、39.4个月vs. 17.8个月( P=0.02)、23.6个月 vs. 23.7个月( P=0.66),提示在缓慢进展模式的患者中,继续应用EGFR-TKI的患者总生存要显著优于改用化疗的患者。
EGFR突变的非小细胞肺癌患者在接受EGFR-TKI治疗后不可避免地会发生疾病进展,目前虽然大部分EGFR-TKI继发性耐药的机制已经明确,但现阶段EGFR-TKI继发性耐药的后续治疗仍缺乏有效手段。以往的一些临床研究表明:患者在病情进展后停用EGFR-TKI可能会出现病情加重(Flare现象)[ 1],另外,一些回顾性研究提示一部分患者可以从继续使用EGFR-TKI中获益[ 2, 3, 4],但获益患者的临床特征并不十分明确。
这项研究对EGFR-TKI临床失败模式以及不同失败模式的后续治疗策略进行积极有益的探索,并尝试界定继续服用EGFR-TKI获益人群的临床特征。该研究根据疾病控制时间、肿瘤负荷以及临床症状的变化等临床因素,将EGFR-TKI临床失败模式分为快速进展、缓慢进展、局部进展三种模式。更为重要的是,与以往研究相比,该研究对上述临床因素都进行了详细的量化,临床可操作性较强。
研究结果表明:在快速进展、缓慢进展、局部进展的失败模式中,继续使用EGFR-TKI与改用化疗相比,中位OS分别为18.6个月 vs. 23.9个月( P=0.07)、 39.4个月vs. 17.8个月( P=0.02)、 23.6个月vs. 23.7个月( P=0.66),这提示在缓慢进展模式的患者中,继续应用EGFR-TKI的患者总生存要显著优于改用化疗的患者,该模型在现阶段临床实践中具有一定的指导价值。另一方面,在EGFR-TKI治疗失败后仅接受最佳支持治疗的患者中,缓慢进展患者的总生存也显著优于其他失败模式的患者,说明EGFR-TKI治疗失败的患者可能是一群异质性较强的群体,其预后及后续治疗的选择存在着较大的差异,因此,在解读或者设计EGFR-TKI继发性耐药的后续治疗的临床研究时也要充分考虑不同失败模式这一因素的影响。
但该篇文献仍存在有待商榷之处。第一,该研究应用Bayes判别分析方法建立EGFR-TKI临床失败模式的数学模型,在应用该研究方法的过程中,关键的一点是训练集样本的实际分类最好是由金标准确立的分类。但在该研究中,研究者预先设立了EGFR-TKI失败模型的分类,其分类是否能成为普遍接受的金标准可能正是研究者首先需要研究和回答的问题。另外,如果从临床应用的角度看,EGFR-TKI失败模式的建立主要是为了指导耐药后是否继续应用EGFR-TKI,从这个意义上说,进展患者中继续应用EGFR-TKI的获益情况作为分类的金标准可能更为合适(如何定义EGFR-TKI的获益又是一个新的问题)。第二,正如研究者自己在讨论中提到,该项研究是一个回顾性研究,而且不同失败模式中的亚组样本量偏低,部分亚组样本量少于20例,因此该临床研究结果仍有待扩大样本量进行进一步验证。
综上所述,在现阶段临床实践的背景下,该项研究对EGFR-TKI临床失败模式以及不同模式的后续治疗进行了积极有益的探索,研究结果对临床有一定的借鉴作用,但仍需进一步证实和完善。另外,不同的EGFR-TKI临床失败模式是否存在不同的分子生物学机制仍有待进一步明确,也是今后的研究方向之一。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|