秘营昌教授,中国医学科学院血液病医院(血液学研究所)白血病诊疗中心副主任,主任医师,博士研究生导师。1998年毕业于中国协和医科大学。中华医学会血液学分会青年委员,《中华血液学杂志》、《中国实验血液学杂志》、《中国实用内科杂志》、《国际输血与血液学杂志》编委,卫生部抗肿瘤药物合理用药专家组成员。主要从事白血病的临床与基础研究工作。作为主要执笔人参与起草了我国成人急性髓性白血病诊断治疗指南和成人急性淋巴细胞白血病的专家共识,作为负责人或主要人员参与多项课题研究,参编著作10余部。
Kantarjian HM,Thomas XG,Dmozynska A,et al. Multicenter, randomized, open-label, phase Ⅲ trial of Decitabine versus patient choice, with physician advice, of either supportive care or low-dose Cytarabine for the treatment of older patients with newly diagnosed acute myeloid leukemia [J]. J Clin Oncol, 2012,30(21):2670-2677.
1b。
急性髓性白血病(acute myeloid leukemia,AML)是一种常见的成人白血病,美国每年新发病例数约为12 330例,欧洲大约为18 000例。AML多见于老年患者,但对于老年患者,尤其是体能状况评分较差以及具有较多并发症的患者,治疗往往受到很大限制。美国癌症综合网(NCCN)、欧洲白血病网、欧洲肿瘤内科学会最近更新了其对AML治疗的推荐方法,其中包括小剂量阿糖胞苷(Cytarabine,Ara-C)、5-氮杂胞苷和地西他滨。
作为一种去甲基化药物,地西他滨能够抑制DNA甲基转移酶,具有直接的细胞毒作用和/或影响细胞的分化和凋亡。研究表明,地西他滨能够用于治疗所有FAB亚型的初治、复治的原发和继发的骨髓增生异常综合征(myelodysplastic syndrome,MDS),包括国际预后积分系统评分中危1、中危2和高危组的MDS。Ⅰ期和Ⅱ期临床研究已经证实了地西他滨单药、联合安吖啶或去甲氧柔红霉素治疗复发AML的疗效。
在AML发病过程中,甲基化能够沉默肿瘤抑制因子CCAAT/增强子结合蛋白δ。在一项随机临床试验中,设计了三种地西他滨方案治疗MDS或慢性粒单核细胞白血病,地西他滨20 mg/(m2·d),静脉输注(时间大于1小时),连用5天,能够最大程度地诱导去甲基化并取得最高的完全缓解率(complete response,CR)。这一方案对≥60岁的中高危细胞遗传学异常的老年AML患者同样有效,CR可达24%(13/55),耐受性较好。地西他滨20 mg/(m2·d),静脉输注(时间大于1小时),连用10天的方案治疗≥60岁的初治AML,CR可达47%(25/53)。
地西他滨治疗老年AML患者已经初见疗效。
与对症支持治疗或小剂量Ara-C治疗相比,评价地西他滨治疗老年中、高危初诊AML患者的疗效及安全性。
•研究条件:美国西南肿瘤协作组(SWOG)、东部肿瘤协作组(ECOG)中,年龄≥65岁的初诊、原发或继发的中、高危组AML(原始细胞≥20%)患者。
•研究方法:多中心、随机、对照、开放、Ⅲ期临床试验。
•入组时间:2006年1月至2009年4月。
•研究对象和干预措施:65家单位、共485例患者参加随机分组,地西他滨组242例(最终接受地西他滨治疗238例),其他治疗组243例(最终接受其他治疗237例)。地西他滨组治疗方案:20 mg/(m2·d),静脉输注(时间大于1小时),连用5天,每4周1个疗程。其他治疗组治疗方案:对症支持治疗,或者皮下注射Ara-C 20 mg/(m2·d),连用10天,每4周1个疗程。治疗终点:患者复发、疾病进展、死亡、不可耐受的毒性、缺乏临床疗效、出现其他影响治疗的并发症或患者/医生要求停止治疗。
•评价指标:主要评价指标为总生存期(overall survival,OS),次要评价指标为CR和副作用。
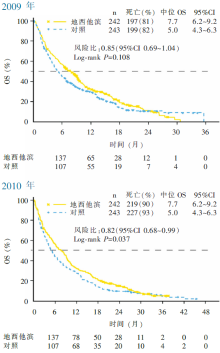
随访至2009年,共有396例患者死亡(死亡率81.6%)。地西他滨组中位OS 7.7个月[95%可信区间(confidence interval, CI)6.2~9.2个月],对照组为5.0个月(95%CI 4.3~6.3 个月),无明显差别(风险比0.85,95%CI 0.69~1.04, P=0.108)。随访至2010年,共有446例患者死亡(死亡率92%),两组的中位OS与2009年随访结果相同,但地西他滨组略显优势(风险比0.82,95%CI 0.68~0.99, P=0.037),见 图1。地西他滨组CR+CRp(CR伴血小板不完全恢复)为17.8%,对照组为7.8%( P=0.001)。地西他滨组患者中位疗程数为4个疗程,Ara-C对照组的中位疗程数为2个疗程。至2009年,药物相关不良事件发生率地西他滨组为74%、Ara-C组为73%(基本相似);地西他滨组最常见的药物相关不良反应是血小板减少(27%)和中性粒细胞减少(24%)。30天内的死亡率地西他滨组为32%(副作用相关死亡率24%),Ara-C组为28%(副作用相关死亡率19%)。
在老年AML患者,与标准治疗方案相比,地西他滨能够提高治疗反应率,同时在安全性上无明显差别。进一步随访显示,地西他滨能够使患者OS受益。
AML的中位发病年龄超过60岁(如意大利学者Ferrara[ 1]报道的中位年龄为69岁),老年AML是AML的一个重要人群,但治疗一直是个难题。目前国际上对老年AML的治疗往往比较消极,如2012年Oran等[ 2]报道的美国SEER (Surveillance, Epidemiology, and End Results)数据库2000-2007年5 480名AML患者的资料,中位年龄78岁(65~93岁),仅2 113例(38.6%)患者在诊断后3个月内接受了针对白血病的治疗,治疗组中位OS 6个月、未治疗组中位OS 仅2个月;46例(0.8%)患者接受了异基因干细胞移植。
目前关于老年AML的治疗方法主要有以下选择:(1)增强化疗,目的是取得CR;达CR后可以行干细胞移植; (2)减低强度的化疗,包括小剂量Ara-C、去甲基化药物如5-氮杂胞苷和地西他滨; (3)支持治疗和/或羟基脲控制白细胞增多;(4)临床试验。治疗方案的选择应注意治疗的目的是取得最好的疗效,但又要避免不必要的毒副作用。采用传统的诱导治疗方案,老年AML的CR多低于50%(45%~65%),3~5年的生存率多在10%以下(年龄越大疗效越差)。去甲基化药物氮杂胞苷和地西他滨可以在不取得CR的情况下获得长生存期,是老年AML十分有前景的治疗选择。2010年美国癌症综合网(NCCN)AML治疗指南中针对无严重并发症、≥60岁的AML患者首次将氮杂胞苷和地西他滨等低强度治疗方法列入治疗选择(2B类推荐)。
地西他滨作为一种去甲基化药物,可以抑制DNA甲基转移酶,已广泛用于MDS的治疗。关于该药的用药方法、剂量、用药时间均有相关研究,用于治疗AML的临床试验也在不断开展。如2007年Kantarjian等[ 3]报道了三种用药方案治疗高危MDS和慢性粒单核细胞白血病随机临床试验的结果。单药地西他滨用药方案分别为:20 mg/(m2·d),静脉输注(1小时以上),5天1个疗程;20 mg/(m2·d),皮下注射,5天1个疗程;10 mg/(m2·d),静脉输注,10天1疗程。结果表明5天静脉用药方案应该是最佳方案(能够最大程度地诱导去甲基化)。2010年Cashen等[ 4]报道了地西他滨一线治疗老年AML(年龄≥60岁,中位年龄74岁)的Ⅱ期、多中心临床试验(共55例患者)的结果,地西他滨用法为20 mg/(m2·d),静脉输注,5天1个疗程,每4周一个周期。总有效率25%(CR 24%),30天内的死亡率为7%,中位OS 7.7个月。2010年Blum等[ 5]报道地西他滨单药10天方案治疗老年AML的Ⅱ期临床试验的结果。用药方案为20 mg/(m2·d),静脉输注,10天1个疗程,每4周重复。共入组53例患者,中位年龄74岁(60~85岁)。CR达47%,总有效率64%,中位达CR的疗程为3个疗程。中位OS 55周、无病生存期46周。30天内的死亡率2%。欧洲的用药方法和美国并不完全一样,2012年Lübbert等[ 6]报道的欧洲白血病网有关单药地西他滨一线治疗老年AML(不适合诱导化疗的患者)的Ⅱ期多中心临床试验结果。采用的方案是15 mg/m2,每天3次,连续用药3天(总用量135 mg/m2)。总有效率26%(CR+部分缓解),中位OS 5.5个月,1年生存率28%。可以看出20 mg/(m2·d),连用10天方案的效果是最好的。
本文报道的临床试验是MD Anderson癌症中心牵头的多中心、随机Ⅲ期研究,分为地西他滨组和小剂量Ara-C/支持治疗组。设计是合理、科学的,但采用的用药剂量仍然是2007年报道的方案[20 mg/(m2·d),连续静脉输注5天,每4周1个疗程],没有参考Blum等报道的10天方案来设计。地西他滨组CR+CRp率为17.8%,中位生存7.7个月,疗效优于小剂量Ara-C/支持治疗的患者。CR+CRp患者取得疗效的中位时间为4.3个月。亚组分析可以看出年龄≥70岁的患者、基线骨髓原始细胞比例>30%的患者、体能状态2分(和0~1分比较)、细胞遗传学中危组(和高危组比较)的患者获益较大。结果说明,骨髓原始细胞比例较高的患者采用小剂量Ara-C或支持治疗,效果很差;采用地西他滨治疗可以改善疗效。而骨髓原始细胞比例较低的患者采用小剂量Ara-C可以维持一段时间,但达到CR的机会很小。研究结果还说明,地西他滨治疗是安全的,药物相关的毒副反应和小剂量Ara-C治疗相当。
如果本研究设计采用地西他滨10天方案,结果有可能进一步提高。也有必要比较地西他滨和联合化疗方案(甚至是偏低剂量的联合化疗)治疗老年AML的优劣。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|