| 董太明,男,副主任医师;1984年获医学学士学位,1991年获医学硕士学位;1991年至今一直在广东省人民医院、广东省心血管病研究所心内科从事临床、科研工作,曾任广东省重点实验室风湿热实验室主任,主要研究方向是风湿热、风心病、冠心病等,具有丰富的临床、科研及教学经验,先后在中华级、省级等核心期刊上发表文章30余篇,参与多部医学专著的编写。先后主持省科委、省卫生厅多项科研课题,并获广东省科学技术进步奖二等奖;从事冠脉介入治疗20年,完成经皮冠状动脉介入治疗手术1 500例以上。 |
Alli OO, Singh IM, Holmes DR Jr, et al. Percutaneous left ventricular assist device with TandemHeart for high-risk percutaneous coronary intervention: The Mayo clinic experience[J]. Catheter Cardiovasc Interv, 2012,80(5):728-734.
4。
左心室收缩功能不全、心源性休克或复杂冠脉病变(多支血管病变、左主干或类左主干病变)的患者可从外科血运重建中最大获益。然而,其中一些高危患者可能由于手术并发症禁忌行外科手术。不幸的是,这些患者行经皮血运重建发生心血管并发症的风险也极高。这些风险和球囊扩张、冠脉内旋磨术等复杂操作时出现的血流动力学崩溃相关。主动脉内球囊反搏(intra-aortic ballon pump,IABP)虽然是最常用的心脏支持装置,但它有以下的局限性:不能主动辅助心脏;心输出量的增加依赖自身心脏收缩及稳定的心脏节律,且支持程度有限;对严重左心功能不全或持续性快速型心律失常者效果欠佳。TandemHeart(Pittsburgh)是一种在心导管室经皮插入的左心室辅助装置。这种装置提供左心房-股动脉的临时旁路,最大血流量可达5 L/min。
分析不能外科手术和标准经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)高危患者的血流动力学和临床数据,报道作为血流动力学支持的经皮左心室辅助装置TandemHeart的初始使用经验和临床终点。
•研究条件:Mayo医院临床PCI注册处。
•研究起止时间:2004年12月到2009年7月。
•研究方法:单中心回顾性临床研究。
•研究对象:严重左心功能衰竭[左心室射血分数(left ventricular ejection fraction,LVEF)<30%]需要使用TandemHeart装置作为血流动力支持的高危PCI患者。高风险定义为LVEF<30%、Jeopardy评分>8的患者,短暂或持久的靶血管闭塞可导致这些患者心源性休克、心肺复苏术或死亡。患者由于其他适应证(如心源性休克、主动脉瓣膜成形术或射频消融)植入TandemHeart装置的不纳入本研究。
•干预措施:所有患者行PCI前服用双抗血小板治疗(阿司匹林325 mg和氯吡格雷600 mg)。如果PCI术中出现血流动力学崩溃,由术者决定置入TandemHeart或Impella。这个决定基于PCI期间(尤其应用旋磨术等复杂术式)预期缺血的程度和残余心肌的数量。不需要完全心脏支持的患者一般植入Impella,需要完全心脏支持的患者且有足够血管通路时植入TandemHeart。所有TandemHeart支持的PCI都纳入这个研究。
术后阿司匹林(162 mg/天)长期服用和氯吡格雷(75 mg/天)至少服用30天(植入金属裸支架)或12个月(植入药物洗脱支架)。抗凝方案由术者决定,通常使用维持活化凝血时间300~350 s的普通肝素量。
•评价指标:PCI手术成功率、生存率、并发症及死亡率。PCI术成功的定义为:靶血管完全血运重建,术后血流动力学和心电稳定,TandemHeart成功撤机。血管并发症参照血管外科协会报道的血管内主动脉移植修复术后的血管并发症的定义。主要的血管并发症定义为任何的主动脉夹层/损伤,穿刺点或通路相关血管损伤(夹层、狭窄、穿孔、破裂、动静脉瘘、假性动脉瘤、血肿、不可逆的神经损伤或骨筋膜间室综合征)导致死亡、需要4单位血液输注、未计划的经皮或外科介入、不可逆的终末器官损害,远端血管栓塞(需要外科手术、导致截肢或不可避免的终末器官损害)。
共64名高危PCI患者植入TandemHeart。其中,3名患者拒绝数据用于研究,7名患者数据丢失,最后54名患者的数据纳入分析。患者的临床及手术特征见 表1。
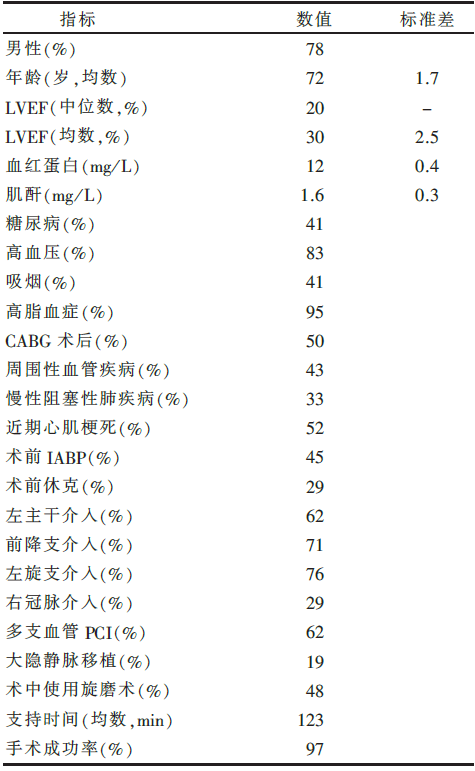
| 表1 患者的临床和手术特征 |
大部分患者是男性,平均年龄72±1.7岁。中位LVEF 20%,41%患糖尿病,绝大部分(83%)有高血压史。55%曾行冠状动脉旁路移植术(coronary artery bypass grafting,CABG),43%患者有外周动脉疾病。SYNTAX评分的中位数是33分,Jeopardy评分的中位数是10分。
疾病的严重程度:52%患者有最近心肌梗死史,29%患者有术前休克,45%患者有PCI前IABP植入史。使用标准和对数Euroscore评分评估外科血运重建的特殊风险。这群患者的平均Euroscore评分是13分(范围2~23分),与预计30天死亡率33%相一致。
手术成功率是97%。62%患者行左主干介入,62%患者行多支血管介入,48%患者使用冠脉内旋磨术切除重度钙化血管的斑块,76%回旋支和71%前降支介入干预。TandemHeart装置支持时间介于30 min~22 h,平均支持时间是123 min。前27例TandemHeart支持时间是130 min,后27例是116 min。9例(35%)患者由于血流动力学不稳定中断TandemHeart后植入IABP。少数(2例)患者植入TandemHeart时间长达12~24 h,直到稳定后才撤机。
平均右心房压力基线值16 mmHg,使用TandemHeart支持后下降到10 mmHg( P<0.001);肺动脉压从45 mmHg下降到36 mmHg( P=0.04);肺毛细血管楔压从基线值25 mmHg下降到17 mmHg( P=0.02)。这三项指标均能在撤机后维持6 h。心输出量从4.7 L/min增加到5.7 L/min( P=0.03),升幅高达23%。
术后30天,患者生存率是90%。而Euroscore评分和STS评分预测的生存率是67%和87%。应注意的是,Euroscore评分和STS评分适用于标准手术的患者,而不适用于该研究的患者。6个月时,无患者死亡人数增加且87%生存者病情稳定。同预期一样,大部分的并发症来自血管(13%)。在54名患者中,7名患者发生主要血管并发症,其中5名患者行外科修复,1名患者有大量血肿需要输血,1名患者有假性动脉瘤需要注射凝血酶。85%的并发症发生在前27例。其它并发症包括:10%患者血小板减少,1名患者发生预后较好的卒中;2%患者肾功能恶化。患者无造影剂肾病或需要透析。1名患者发展为弥散性血管内凝血导致严重的血液丢失而死亡。1名患者在PCI期间发生严重的右冠脉穿孔并发室颤而死亡。
为了评估学习曲线和术者经验的影响,该研究分早期和晚期亚组来检验终点。早期27例组成Mayo医院医生经验的早期亚组,晚期的27例组成医生经验的晚期亚组。相对于晚期亚组,虽然早期亚组的STS和Euroscore评分较低,但30天死亡率较高。这提示学习曲线与术者使用TandemHeart经验、患者选择和手术操作过程有关。
在标准经皮和外科血运重建都是极高危的情况下,严重冠心病和左心功能不全的患者植入左心室辅助装置TandemHeart是可行的治疗策略。
该研究入选54例高危PCI患者并报道这些非外科手术患者的血流动力学、并发症的发病率、死亡率等终点数据。它的主要发现是:严重左心室功能不全和复杂冠心病不能外科手术患者可在血流动力学支持下行高危PCI。外科手术和标准PCI都极高危的患者使用TandemHeart心脏辅助装置,可使手术成功率达到97%。然而,13%的主要由于血管并发症和10%的30天死亡率使TandemHeart应用前景变得复杂。
已有多个研究报道心源性休克患者在TandemHeart装置辅助下行高危PCI[ 1, 2, 3]。Thomas等最近报道了37例行高危PCI的心源性休克患者,这些患者的平均Euroscore评分是11分[ 4]。Vranckx等报道了相似的研究,平均Euroscore评分是6.5分[ 5]。本文Mayo医院高危患者的平均Euroscore评分是13分(2~23分),与预计评分30天死亡率33%相一致。
这个研究报道了一个亚组的情况,既有外科手术风险又有经皮血运重建风险的患者使用IABP支持的标准技术。完全血流动力学支持使血运重建成为可能,这些手术本质上代表一个结合机械心脏支持和经皮血运重建技术联合的方法。介入和外科团队紧密协作和交流是正确选择和成功处理病人的关键。该研究中这组高危特征的人群改善了30天和6个月时的观察终点数据。同样,Thomas等报道出院患者生存率为71%,Vranckx等报道的6个月生存率为57%[ 5]。
TandemHeart植入后,患者血流动力学参数明显改善。伴随心输出量的增加,右心压力和左心充盈压明显下降。这个发现与TandemHeart装置已知的血流动力学效应(前后负荷下降、心输出量和平均心房压增加、改善组织灌注后心肌需氧量减少)相一致。因为TandemHeart是左心室辅助装置而不是人造心脏,所以功能性的右心室是必要条件。且室颤不能很好耐受,需快速除颤。
两个对比TandemHeart和IABP的随机试验得出这样的结论:由于心脏动力改善和肺毛细血管楔压下降,TandemHeart对维持、改善甚至反转不良血流动力学参数更有效,而死亡率没有明显差异[ 6, 7]。
BCIS1试验(高危PCI选择性植入IABP):把多支血管病变(Jeopardy评分>8)伴严重左心室功能不全(LVEF<30%)的稳定患者随机分配到IABP组和无IABP组。两组的30天和6个月的结局指标没有差异[ 8]。对比高危PCI中Impella 2.5和IABP应用的前瞻性多中心试验证实,非急诊高危PCI术应用Impella优于IABP[ 9]。这个试验中SYNTAX评分的中位数是29(IABP)和30(Impella)。30天和90天的临床结局指标没有差异。上述两个研究显示,血流动力支持装置在稳定患者行非急诊PCI中没有获益。值得注意的是,因为选择的是超过IABP提供血流动力支持的患者,所以纳入该研究的患者不适合进行随机分组,因此上述试验的结果不能直接适用于该研究。
通过使用主-髂动脉造影确定合适的股动脉和髂动脉、缝合式血管封堵器和血管外科临时开放血管修复等手段已经降低了之前报道的血管并发症的高发生率。在该研究中,TandemHeart大部分的并发症来自血管(13%)。其它已知的并发症包括血小板减少症、低体温、溶血、血栓栓塞、套管移动、肢体缺血和冠脉穿孔引起心脏填塞[ 10, 11]。很明显,TandemHeart的使用技术是广泛使用该装置的最大障碍。一旦广泛应用,它将可能是转诊中心最好的压轴技术。
多学科(麻醉、心脏、血管外科)密切协作是达到最佳临床结局的关键。诊疗患者和管理装置的介入医生、护士及相关员工有明显的经验效应(学习曲线)。该研究数据分析显示,相对于研究阶段的前半部分的患者,后半部分手术患者的临床结局得到改善。我们相信后半部分患者终点的改善不仅是由于技术的改进,也是由于更好的患者选择。
细化患者选择的一个主要影响因素是主要血管并发症减少。主-髂动脉的仔细评估减少了后半部分患者血管并发症的发生率。85%主要血管并发症发生在我们研究的前半部分。在研究的后半部分,IABP作为患者撤除TandemHeart的过渡装置的使用率也增高。这为围手术期的患者提供血流动力支持,从而避免发生TandemHeart相关的血管和其它并发症(如套管移位和凝血障碍)。一旦患者转运到重症监护病房,IABP使用的简易性也使它成为一个有利的选择。在选择的病人中,IABP作为TandemHeart撤机的过渡装置是合理并有利的。
值得注意的是,实际变差的患者终点暗示明显的学习曲线效应。很难说介入医生在精通该装置之前需要多少练习病例。这高度依赖每一个术者的经验、复杂介入技术(间隔穿刺、冠脉旋磨、大动脉套管和高危患者的处理)的水平。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|