|
黄诚,福建省肿瘤医院肿瘤内科主任,主任医师,福建医科大学肿瘤内科教研室主任,教授,福建省肿瘤化学治疗质量控制中心主任。兼任中国抗癌协会肺癌专业委员会常委,中国癌症康复与姑息治疗专业委员会常委。中国抗癌协会临床肿瘤学会常务委员、小细胞肺癌专家委员会副主任委员、血管靶向治疗专家委员会委员及肿瘤生物标志物专家委员会委员。福建省肺癌专业委员会主任委员,福建省癌症康复与姑息治疗专业委员会主任委员,福建省化疗专业委员会副主任委员;《中国肺癌杂志》,《临床肿瘤学杂志》,《中国肿瘤临床与康复》,《J Thorac Oncol》中文版等杂志编委。长期从事肿瘤内科的临床和科研工作,并且参加多项国际多中心临床研究项目,在省级以上核心刊物发表学术论文60多篇,获省级以上科技成果奖2项。 |
Wu YL, Lee JS, Thongprasert S, et al. Intercalated combination of chemotherapy and Erlotinib for patients with advanced stage non-small-cell lung cancer (FASTACT-2): A randomised, double-blind trial[J]. Lancet Oncol, 2013,14(8): 777-786.
1b。
之前的随机对照Ⅱ期临床试验FASTACT结果表明化疗间插联合厄洛替尼能有效延长晚期非小细胞肺癌(non-small cell lung cancer,NSCLC)的无进展生存期(progression-free survival,PFS)。
进行Ⅲ期临床试验进一步确认化疗间插联合厄洛替尼这一治疗方案的疗效。
•研究条件:本研究在28家研究中心实施,其中中国9家、中国香港4家、印度尼西亚3家、韩国1家、菲律宾3家、中国台湾3家、泰国4家。
•研究起止时间:2009年4月29日至2010年9月9日。
•研究方法:多中心、随机、对照、双盲、Ⅲ期临床试验。
•研究对象:18岁以上,诊断明确的ⅢB/Ⅳ期NSCLC,ECOG评分为0~1分。
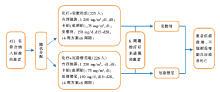
•干预措施:患者随机分为两组,试验组方案为吉西他滨+卡铂(或顺铂)+厄洛替尼,对照组方案为吉西他滨+卡铂(或顺铂)+安慰剂, 具体实施方案见 图1。疾病进展后,化疗+安慰剂组患者可以交叉使用厄洛替尼,而化疗+厄洛替尼组患者也可以根据研究者的决策接受进一步的治疗。
患者的数据根据以下因素进一步分层:(1)临床分期(Ⅲ期或Ⅳ期),(2)病理类型(腺癌或非腺癌),(3)吸烟状态(目前吸烟、既往吸烟或不吸烟),(4)化疗方案(吉西他滨+卡铂或吉西他滨+顺铂)。
•评价指标:主要研究终点指标为研究者评价的PFS;次要研究终点指标为独立审查委员会评价的PFS、总生存期(overall survival,OS)以及亚组的PFS和OS;其他次要研究终点指标为客观缓解率(objective response rate,ORR),生活质量(quality of life,QoL)。
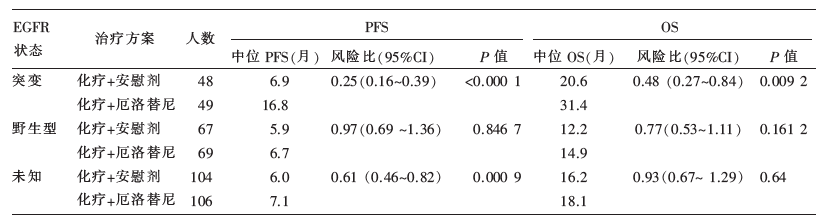
总共入组451例患者,225例随机分配到化疗+安慰剂组,226例随机分配到化疗+厄洛替尼组,结果显示,在总人群中,化疗+厄洛替尼组相比化疗+安慰剂组能显著延长PFS及OS(PFS 7.6个月vs. 6.0个月, P<0.000 1;OS 18.3个月vs. 15.2个月, P=0.042 0),见 表1。研究者按患者EGFR状态进行分类,发现只有EGFR突变患者能从化疗+厄洛替尼方案中显著获益(PFS 16.8个月vs. 6.9个月, P<0.000 1;OS 31.4个月vs. 20.6个月, P=0.009 2; ORR 84% vs. 15%, P<0.000 1);在EGFR状态未明患者中,PFS显著获益,而OS无显著差异;而在EGFR野生型患者中,两组之间PFS和OS均无明显差异(ORR 26% vs. 19%, P=0.35),见 表2。
| 表1 化疗+安慰剂组对比化疗+厄洛替尼组在总人群的疗效结果 |
| 表2 化疗+安慰剂组对比化疗+厄洛替尼组不同EGFR突变状态的疗效结果 |
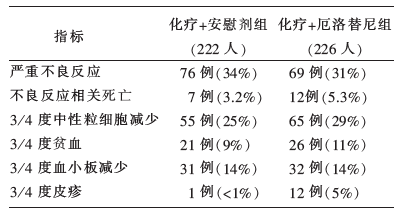
在毒性方面,最常见的为中性粒细胞减少、贫血、恶心以及皮疹。化疗+厄洛替尼组相比化疗+安慰剂组皮疹、腹泻更多见,严重不良反应发生率两组类似(31%vs.34%),见 表3。
| 表3 化疗+安慰剂组和化疗+厄洛替尼组的严重不良反应 |
对于EGFR突变阳性或EGFR突变状态不明的晚期NSCLC患者,化疗与厄洛替尼间插联合治疗方案是一种可行的一线治疗手段。
FASTACT-2是一个随机、双盲、安慰剂对照的Ⅲ期多中心临床试验,旨在比较一线化疗联合间插式厄洛替尼与单纯化疗在初治的非选择性晚期NSCLC患者的疗效及安全性。研究结果显示化疗联合间插式厄洛替尼组的ORR、PFS(主要研究终点)、OS均显著优于化疗组,在不良反应方面,两组均耐受良好,与预期结果一致,厄洛替尼与化疗联合应用组的腹泻和皮疹的发生率高于化疗组。两组患者临床病理特征均衡可比,从入组患者的基线特征看,腺癌患者占75%以上,半数以上患者明确EGFR基因状态,其中EGFR突变占40%左右。更为重要的是,两组患者EGFR突变比例基本相当,这也高度反应了该临床试验结果分析的可靠性。
对于该临床试验,研究者的结论是化疗联合间插式厄洛替尼可以作为EGFR状态不明或EGFR突变阳性的NSCLC患者的一线治疗选择,这一结论相对于临床试验本身而言无可厚非。但值得注意的是:亚组分析的结果提示试验组的生存优势似乎仅仅体现在EGFR突变阳性的患者中,在临床实践中,对EGFR状态不明的NSCLC患者是否能够应用这一治疗模式仍应谨慎。回顾以往的IPASS、 WJTOG3405、 NEJ022、OPTIMAL、EURTAC、TAILOR、DELTA以及新近报道的CTONG 0806等一系列临床试验,已经有相当多的研究结果提示EGFR-TKI获益人群的本质核心是EGFR突变,EGFR-TKI无论是一线治疗还是二线治疗,EGFR野生型患者均无法从中获益。无独有偶,一项培美曲塞联合间插式厄洛替尼治疗已知EGFR突变状态的复治晚期NSCLC患者的单臂Ⅱ期临床试验,共入组27例患者,其中仅1例为EGFR突变阳性,试验结果并未看出联合治疗的优势[ 1]。因此,将FASTACT-2临床试验结果运用于EGFR状态不明的患者中仍应谨慎。
在EGFR突变阳性患者中,化疗与EGFR-TKI联合应用的最佳模式一直是研究的热点,以往回顾性数据分析提示EGFR-TKI与化疗孰先孰后对OS并未产生显著影响。FASTACT-2临床试验中,对照组高达79%患者二线接受EGFR-TKI治疗,在EGFR突变阳性患者的亚组分析中,间插式给药组的OS要显著优于对照组,中位OS 31.4个月 vs. 20.6个月, P=0.009 2。这一结果提示该联合模式可能有助于提高OS,值得进一步研究。目前EGFR-TKI已经成为EGFR突变阳性患者的标准一线治疗的选择,因此,今后FASTACT-2这种模式的临床研究应该以EGFR-TKI单药治疗作为对照应该更有说服力。
FASTACT-2临床试验也存在一些争议之处:首先,该临床试验选用了吉西他滨联合铂类的化疗方案(吉西他滨1 250 mg/m2 d1、d8,顺铂75 mg/m2或卡铂 AUC=5 d1,每4周重复),从临床试验结果看,化疗中位PFS、ORR的点值估计分别仅为7.6个月、18.2%,这一方案是否可以代替3周方案作为标准的一线化疗仍存在争议,需要进一步研究。另外,EGFR-TKI间插给药模式源于EGFR-TKI导致肿瘤细胞G1期阻滞从而影响化疗疗效的理论,但间插给药模式是否能真正达到这一效应、这种理论是否成立仍值得探讨。以往体外研究表明EGFR-TKI间断给药产生耐药的速度要快于持续给药[ 2],因此有必要对联合模式的最佳给药方法进一步研究。
| [1] |
|
| [2] |
|