作者简介:麦丽萍(1985-),女,广州人,技师,主要从事Ⅰ期临床试验管理工作。
目的分析Ⅰ期临床试验中影响受试者管理的主要因素,探讨增强受试者依从性、提高试验质量的方法。方法比较2008-2011年措施前与2012年措施后受试者招募、知情同意、筛查、试验过程控制和试验后管理情况。结果联合使用多种招募方式能增加受试者招募人数,招募时长缩短1倍,为后续的筛查工作提供足够的研究对象。充分的知情、严格的筛查和试验过程培训能增强受试者的依从性;专业的随访有助于受试者评价我们的工作。结论通过在受试者招募、知情同意、筛查、试验过程和试验后的受试者管理等环节采取措施能明显增强受试者的依从性,提高试验质量。
Objective To analyze the main factors affecting volunteer management in phase I clinical trials and explore the methods of enhancing the volunteer compliance and the quality of clinical trials.Methods In terms of the volunteer recruitment, informed consent, screening, the control of the trial procedure and the follow-up, we compared the volunteer management before the measures in 2008-2011 and after the measures in 2012.Results The rate of recruited subjects increased and the recruitment period was shortened one fold by the combined recruitment methods. A fully informed consent, strict screening and volunteer training in the trials improved the compliance of the subjects. The professional follow-up was useful for our work.Conclusion Taking effective measures in volunteer management improved the compliance of the subjects, which enhanced the quality of clinical trials.
Ⅰ期临床试验是在人体身上进行初步的临床药理学及安全性评价试验,是新药人体试验的起始阶段,为后续研究提供科学依据。除肿瘤药物外,Ⅰ期临床试验的受试对象多为健康受试者。文献报道,Ⅰ期临床试验的实施与Ⅱ、Ⅲ期临床试验相比有其特定的难度, 尤其是对受试者的管理, 直接关系到受试者的安全、权益及试验结果的科学可靠性[ 1, 2]。目前,有关新药临床试验中受试者的管理研究也已成为当代医学界需要重点解决的问题。由于没有统一的标准流程,各研究机构的受试者管理质量参差不齐。本研究室已开展Ⅰ期临床试验百余项,近年来研究室特别重视受试者管理,现已建立和总结出一套受试者管理模式和经验,明显增强了受试者的依从性,对保障受试者安全和提高试验质量有重要的现实意义。
受试者管理主要包括以下环节:受试者招募、知情同意、筛查、试验过程和试验后管理。为探讨措施前后受试者管理的情况,收集了我院2008-2012年的新药Ⅰ期临床试验10项,其中2008-2011年共7项,2012年共3项。耐受性试验2项, 药动学试验1项, 生物利用度试验7项, 受试新药包括抗生素类、抗血小板类、降脂类、免疫增强剂等。2011年12月前的Ⅰ期临床试验受试者管理均采用传统的模式(以下称“2008-2011年措施前”),2012年1月后,研究室在受试者管理的各环节均采取多种措施,加强管理(以下称“2012年措施后”)。
2008-2011年开展的7项临床试验均采用广告形式招募,在学校内网和公告栏等地方发布招募信息。
2012年开展的3项临床试验招募方式除以广告形式外,还通过参观学习的方式改进,具体措施有:①定期举办临床试验知识讲座和参观学习,并提供免费接送、午餐等;②学习内容主要是Ⅰ期临床试验的试验目的、流程、风险、权利和义务等;③与各大高校(包括非医学类院校)的学生负责人联系,建立联络点,为志愿者提供更加便利的报名和参加方式;④报名时填写问卷,主要询问志愿者对临床试验的了解和了解途径、参加临床试验前的心理状况等。
为比较受试者招募的周期,以研究室2012年措施后开展的一项临床试验招募80名志愿受试者与2011年措施前招募的耗时进行比较。
2011年12月前的Ⅰ期临床试验受试者知情同意过程是成批进行。研究者向志愿受试者介绍试验相关情况并回答志愿受试者提出的问题后便开始签署知情同意书。
2012年后,研究者在受试者知情同意环节采取措施:①研究者与受试者谈知情前经过培训;②知情同意过程采取“一对一”的方式,每名志愿受试者知情时间不少于30分钟;③从受试者签署知情同意书到随访结束,与受试者保持良好的沟通和足够的联系,需要时可以给予“顺带”帮助。
以2012年研究室开展一项周期为42天连续耐受性试验共入组健康受试者16人与2011年开展一项周期为28天连续耐受试验共入组健康受试者18人为例,比较措施前后受试者脱落或失访情况。
2011年12月前受试者筛选流程:受试者签署知情同意书、研究者询问其现病史及既往史后,受试者凭体检表到体检中心体检;体检中心统一发放体检报告,研究者根据体检报告并按照研究方案要求筛选合格受试者。
以2011年和2012年研究室开展一项筛查30例受试者的试验为例,比较措施前后受试者入组和剔除情况。
2011年12月前受试者试验过程的管理:受试者在规定时间(一般为试验前夜)入住Ⅰ期病房并进行受试者培训,次日按方案要求进行试验。
2012年后研究室在受试者试验过程中加强管理:①受试者培训后,为避免受试者对培训内容的遗忘,制定了“受试者温馨提示”;②为受试者提供电视、网络、书报等娱乐设施;③受试者进入病房后集中管理,穿着统一、非试验物品由研究者统一管理,锁于受试者储物柜,不得带入试验区;④密切注意受试者的精神心理状况,特别是开展时间较长的研究项目,如连续耐受性试验。必要时进行个别的心理辅导。
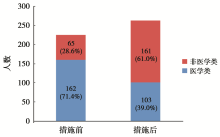
2012年(措施后)研究室开展的3项临床试验共招募志愿受试者264名,年龄18~30岁,平均年龄:(23.0±2.5)岁;其中医学类学生103人,占招募总人数的39.0%;非医学类学生161人,占招募总人数的61.0%。2008-2011年研究室开展的7项临床试验共招募志愿受试者227名,年龄18~30岁,平均年龄:(24.3±2.4)岁;其中,医学类学生162人,占招募总人数的71.4%;非医学类学生65人,占招募总人数的28.6%。与2008-2011年措施前研究室开展的临床试验仅通过学校内网和公告栏发布信息招募相比较,非医学类学生人数和比例均提高,见 图1。
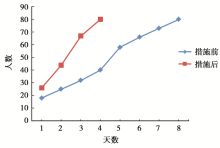
研究室2012年措施后开展的一项临床试验招募80名志愿受试者与2011年措施前招募耗时比较,见 图2。结果显示:自举办讲座后,每天招募人数均较措施前增加,获得足够的志愿者的时长缩短1倍。由此可见,研究室采取的招募方式能有效提高了招募志愿者的工作效率。
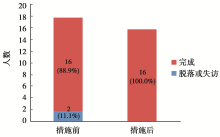
2012年研究室开展一项周期为42天连续耐受试验共入组健康受试者16人,未见受试者脱落或失访;2011年开展一项周期为28天连续耐受试验共入组健康受试者18人,其中2名受试者失访,脱落或失访率为11.1%。因此,研究者与受试者的及时沟通和联系,能使受试者脱落或失访率明显降低,见 图3。
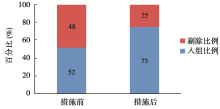
2011年与2012年研究室各开展一项筛查30例受试者的试验,措施前后受试者入组率提高23%,见 图4。由此可见,通过在体检过程严格把关、与受试者及时沟通与联系,能使拟定的体检人数内筛查出符合方案的受试者几率提高。
2012年措施后受试者在试验过程中的依从性得到有效的提高:未见受试者私自携带食物或饮料进入病房;受试者知晓每个试验步骤,整个试验能有条不紊地进行,试验过程更加规范。
2008-2011年措施前,未对所有受试者随访,故没有相关数据。2012年的一项临床试验对80名受试者进行随访,结果显示:28.8%的受试者在研究结束后会主动咨询研究者下次试验开展的时间;91.3%的受试者对试验全过程的安排满意;61.3%的受试者愿意再次参加研究项目。
随着《药物Ⅰ期临床试验管理指导原则》的颁布,国家对于新药Ⅰ期临床试验的要求越来越严格。如何有效管理受试者,控制风险以达到试验目的是临床试验非常核心的环节[ 3]。
本文从受试者招募、知情同意、筛查、试验过程和试验后管理等环节加强受试者管理,保障受试者的安全和权益、控制风险、提高试验质量。
传统的受试者招募一般以广告形式进行,如在医院、医学院校内网和公告栏等地方发布。招募的对象多针对个人素质较高的大学生,尤其是医学院校的学生,因其对医学有所认识,更具有医学科学研究的贡献精神;对研究者而言其依从性更好,更易于管理。然而,由于招募渠道单一,据报道80%的临床试验因受试者招募数量不足而导致试验入组较慢而推迟至少1个月[ 4]。药物临床试验受试者招募、依从性等方面存在影响试验的风险,有可能会影响试验进程[ 3]。
作为研究者,理想的受试者招募是在最短的时间内完成招募工作并筛选出足够数量并符合方案要求的受试者。然而,研究者常面临的问题除志愿受试者招募时间过长或拟定时间内招募数量不足外,还有志愿受试者撤回知情同意书退出试验等情况。文献显示,对临床试验研究的认知程度和心理状态与志愿者退出临床试验相关[ 5]。如何消除志愿者对参加临床试验的各种恐惧和忧虑心理也是成功开展受试者招募的关键!研究室针对上述问题,采取讲座、参观学习等多种形式联合,使志愿者对Ⅰ期临床试验有了更深的认识,有效地解除了他们对参加临床试验的各种恐惧和忧虑心理。从2012年研究室开展的临床试验健康受试者招募情况可见,招募总人数增加,且非医学类的学生人数增加较显著,由此可见,招募人群的扩大能为后续的试验提供充足的试验对象;招募周期缩短,能提高研究者的工作效率。
知情同意过程是受试者管理中的重要环节。充分知情是获得受试者信任、提高依从性的首要条件。文献报道[ 1, 6],在知情同意环节,必须纳入关于最大利益、自主权、隐私权等原则,研究者应尽可能使用受试者能听得懂的语言来描述有关试验的全部信息,应充分告知受试者试验的目的、方法、试验药物的用药剂量、已知的药理作用和不良反应、试验分组、采样时间点及补偿费、参与此次试验的受益和可能的风险,特别是对已有国内外文献报道有诸多不良反应的药物,充分告知、充分知情更为必要。
Ⅰ期临床试验的受试者知情同意过程往往是成批进行的,研究者通常集中向受试者介绍研究情况并完成知情同意,这种知情同意方式往往流于形式,对项目的介绍不够全面、解释不清,并忽略给予受试者充分的知情同意考虑时间,也无法逐一听取并答复受试者的疑问和意见[ 7]。
如何与志愿受试者谈好知情同意,是对研究者的一个考验。研究者在与受试者知情同意前经过培训,充分熟悉方案内容,使受试者的提问得到更好的回复;通过延长知情同意时间,使受试者得到充分考虑;从受试者签订知情同意书到随访结束,研究者与受试者保持良好的沟通和密切的联系,这对于取得受试者的信赖、提高依从性非常重要,特别对于连续耐受或连续药代动力学试验,能降低受试者脱落或失访率。
Ⅰ期临床试验受试者筛查一般由研究者根据体检结果,按方案要求进行筛选。理想的受试者筛查是在拟定的时间、拟定的体检人数内筛查出足够的完全符合方案要求的受试者。然而,研究者在受试者筛查工作中面临着各种问题,导致筛查失败:①部分志愿受试者为了获取免费体检,隐瞒病史;②部分志愿受试者为了获取试验补贴,不但隐瞒病史,还找人冒名顶替参加体检;③受试者短时间内在同一或不同单位参加多个临床试验;④试验前不良的饮食、生活作息会影响体检结果,导致筛查失败等。
研究室针对上述问题,在受试者体检过程严格把关,引入指纹识别系统和条码系统、与合同研究组织联合建立网络受试者资料库等方式增加受试者的入组率,从2012年的受试者筛选情况可见,这种措施有效可行。
Ⅰ期临床试验受试者一般是成批或分批入组进行试验。由于试验人数较多,试验过程的管理显得尤其重要。受试者在试验过程中的依从性是试验过程管理的重要环节,关系到试验能否高质量、顺利完成。如何提高受试者依从性是临床试验的瓶颈问题。研究室制定了“受试者温馨提示”,既可以提高受试者依从性,又有助于试验质量控制;电视、网络、书报等娱乐设施,增加受试者在Ⅰ期病房的归属感;受试者进入病房后集中管理能规范试验流程,便于研究者对试验情况的观察。
为进一步提高试验质量,本研究室在试验过程的其他环节进行严格把关:在药代动学试验中,受试者给药前和给药后需要进行血样或尿样采集,如何准确地把握好采血时间一直是药代试验过程的瓶颈问题。我院开发了“一种药物代谢动力学采样和数据收集系统及方法”[ 8],自动化系统使样本采集时间可以精确到秒,在减少人手操作错误发生的同时可以有效地对样本采集过程进行质量控制。
为避免研究者对不良事件观察的忽略,本室研究者除了于试验前充分了解试验方案外,还根据文献报道和临床前药理、毒理资料对可预见的不良反应制定相关的应急预案和标准操作规范。试验过程中密切观察受试者情况,并适时询问受试者是否有不适,此过程要认真观察,绝不能掉以轻心,任何的疏忽都会影响试验安全性的判断,甚至对受试者造成不可逆的伤害。对于试验中不可预见的不良反应,轻者给予对症治疗,重者积极救治,将损害降至最低,以挽救受试者的生命为宗旨[ 9]。
临床试验后受试者管理是不容忽视的环节,及时的随访对试验后药物不良事件的评价非常重要,尤其是迟发性的不良反应,如不及时随访其往往被忽略,这对Ⅱ、Ⅲ期临床试验甚至药物上市后的应用都有着重要的影响。此外,专业的随访也有助于受试者对我们工作的评价,使我们的后续试验工作能更顺利地开展。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|