编者按:疾病的正确诊断和合理治疗是患者和医务工作者共同的心愿。在广东省人民医院肿瘤中心,吴一龙教授指导临床医生应用循证医学理论进行肿瘤的多学科综合治疗,开展临床病例讨论。讨论会上各学科共同围绕一个病例或一个病种进行会诊,临床、病理、B超、放射影像等资料齐全,除相关科室提前准备的中心性发言外,到会人员各抒己见,气氛热烈。参会人员受益匪浅,提高了对疑难病例的诊治水平。为了将他们的诊治经验传播出去,让更多的临床医生获益,我刊开辟“循证病例讨论”栏目,希望广大医务工作者关注此栏目。
患者男性,20岁。因“左侧腹部疼痛伴停止排气排便半月”入院,PS评分2分,腹痛强度评分3分。
入院检查资料:2011-10-14外院CT示:乙状结肠与降结肠交界处肠壁增厚,考虑恶性肿瘤性病变可能性大,伴肠系膜淋巴结转移;低位肠梗阻。CEA 57.21 ng/mL;CA125 58.0 ng/mL,CA199 255 kU/L。肠镜示乙状结肠腺癌。患者有低位肠梗阻,需急诊手术,2011-10-20行乙状结肠癌切除 + 降结肠造口术。术中见:肿物位于乙状结肠中段,侵出浆膜面,侵犯周围乙状结肠,肠系膜下动脉旁和大网膜内广泛转移,髂血管、腹主动脉周围淋巴结明显肿大。
术后诊断:乙状结肠中分化腺癌pT4aNxM1,腹腔及腹腔淋巴结广泛转移。
杨冬阳(肿瘤内科医师):汇报病史(略),提出讨论要点:(1)评价既往手术治疗、化疗、局部治疗方案的选择,并作疗效评估。(2)下一步的治疗方案,制定最佳治疗策略。
马冬(肿瘤内科教授):该患者为年轻男性,肠梗阻入院,急诊手术,术中发现腹腔广泛转移及多发淋巴结转移,急诊手术行姑息改道治疗,未行淋巴结清扫等扩大手术,请外科专家评价一下手术方式。
杨学宁(肿瘤外科教授):该患者入院时肠梗阻,所行手术为急诊手术,目的是改善梗阻并造口,对于该类患者未行进一步的淋巴结清扫、腹腔病灶清扫应该是恰当的,不违反手术原则。
杨冬阳:患者术后恢复可,PS评分1分。KRAS野生型,术后(2011-10-25)CT示:乙状结肠癌切除术后,肠系膜根部及左侧侧锥筋膜前方结节及多发淋巴结肿大。如何选择治疗方案让患者获益最大?
李伟雄(放疗科教授):放疗对结肠癌淋巴结转移的患者意义不大,主要原因为结肠位置呈动态变化,肠系膜淋巴结接近肠管放疗易至肠损伤,放疗剂量难把握,超过放疗剂量易出现肠穿孔、粘连等并发症。而直肠癌因病灶及转移淋巴结所在位置相对固定适合放射治疗。
杨冬阳:患者腹腔姑息性术后,病灶广泛,不可治愈,以延长总生存期为目的,原发病灶已经切除。本着缩小肿瘤以延长生存期、缓解肿瘤相关症状、增加手术切除几率的原则,我们选择了化疗加靶向治疗的方案。因患者经济条件一般,未选用C225,选择了FOLFIRI化疗加贝伐单抗靶向治疗12周期方案。
旁述:NCCN(2011)结肠癌临床指引中,对能够良好耐受强烈化疗患者的初始治疗,推荐FOLFOX、FOLFIRI、CapeOX、输注5FU/LV或卡培他滨,FOLFOXIRI可用于初始治疗的生物制剂包括贝伐单抗、西妥昔单抗、帕尼单抗。对于KRAS突变的患者, 伊利替康为基础的化疗加贝伐单抗作为目前转移性结直肠癌初始治疗有更多的证据支持[ 1, 2]。
曹小龙(肿瘤内科教授):患者姑息性手术是否可以行扩大手术?目的是减少肿瘤负荷后再行药物治疗,患者KRAS野生型,倾向选择FOLFOX加贝伐单抗然后维持治疗,进展后再行FOLFIRI加C225治疗。
马冬:跟外科讨论的目的就是明确行扩大手术如清除腹腔病灶、转移淋巴结等的可行性及手术对患者的获益。鉴于该患者的手术方式为局部改善梗阻并行结肠造瘘,现以控制肿瘤缩小延长生存期、缓解肿瘤相关症状为原则,选择药物治疗,现阶段化疗加靶向药物的选择方案及优先方案仍有待讨论,患者KRAS基因野生型,在不考虑经济因素前提下,请各位发表化疗药物及靶向药物的选择意见。
吴一龙(肿瘤学教授):现阶段KRAS是重要的指标吗?是否已达成共识?
马冬:KRAS基因的检测结果的指导意义在结直肠癌已成共识,野生型患者可使用C225治疗,部分亚组分析显示外显子13突变虽然预后差,但这部分患者使用C225 仍有获益,BRAF等的小样本的研究虽提示对疗效有影响,但NCCN、欧洲指南等仍以KRAS的检测作为C225靶向治疗的指导。
吴一龙:对于KRAS在结肠癌应用的评价目前基本有共识,即不仅要看KRAS还要看其他的RAS基因。但目前主要存在两个问题需重视,一个是由一两个研究做出来的结果我们采信的程度怎样。另一个问题是加上了靶向药物后能将生存期提高多少,这都是我们要回答的问题。
马冬:关于结直肠癌近年的研究结果,请刘医生向大家汇报一下。
刘建化(肿瘤内科医师):目前结直肠癌一线治疗方案主要为两个基本方案:化疗+贝伐单抗或化疗+西妥昔单抗(或帕尼单抗)。根据不同治疗目的分为晚期不能治愈结直肠癌,潜在可切除病灶结直肠癌和瘤相关症状、恶化风险结直肠癌。按分类选择药物进行治疗。在进行相应基因检测后使用化疗加靶向药物治疗的疗效好于单纯化疗,在强烈治疗达到最大疗效后选择有效药物进行维持治疗是可考虑的选项。
马冬:对于该患者治疗方案的选择,从循证医学的依据考虑,对比相关研究结果,使用FOLFIRI加贝伐单抗治疗证据更充分些。
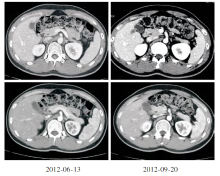
杨冬阳:患者治疗4周期时疗效评价为疾病稳定,病灶相仿;治疗8周期时疗效评价为疾病稳定,病灶缩小10%,12周期时疗效评价仍为疾病稳定,病灶缩小15%,见 图1。那么下一步的治疗方案我们该如何选择?是继续原方案化疗?靶向药物维持?还是单药维持化疗?
曹小龙:可以根据患者的耐受情况评估,耐受性好的可继续化疗加靶向治疗,耐受性一般,可选择氟尿嘧啶类单药维持,因为也有研究提示使用贝伐单抗维持治疗的报道。
吴一龙:临床上选择治疗方案应以证据最全的临床研究为基准,如要采纳证据级别低一点的方案需对照评估,需要告诉我们的是FOLFIRI加贝伐单抗治疗的设计思路是什么。提醒大家注意维持治疗的概念问题,之前认为使用原来化疗方案中的一种药继续治疗即为维持治疗的提法曾引起较大的争议,不少人认为这只是原来治疗方案的组成部分,认为维持治疗应该是原方案治疗后换药继续治疗。
马冬:现阶段,在结直肠癌没有所谓的维持治疗。序列研究OPTIMOX-1、2、3的设计思路是:以FOLFOX为基础化疗,第一项试验单药治疗的生存期无影响、副作用下降,第二项试验未用药物治疗的生存期降低,第三项试验用贝伐单抗+厄洛替尼维持的无进展期延长[ 3, 4, 5]。在这些结果的基础上我们探讨维持治疗的可行性。患者化疗加靶向治疗后评价最大获益时选择有效的单药继续治疗。我科曾对35例患者进行了初步统计,51%的患者的无进展生存期超过了12个月。在最后一次随访时有10例没有疾病复发或进展的迹象,仍继续获得维持治疗获益,从治疗开始至今控制时间7~34个月。所以对于该患者我们也使用卡培他滨进行维持治疗。
旁述:NCCN 2012结肠癌临床指引,OPTIMOX2研究的结果显示OPTIMOX1治疗方法与早期采用无化疗间歇期CFI的策略相比,主要终点指标疾病控制时间差异有统计学意义,维持治疗组为13.1个月,CFI组为9.2个月。
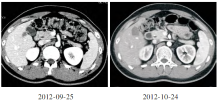
杨冬阳:卡培他滨1 500 mg bid×14天×3周期,无进展生存期9个月,2012-09-20的CT片与2012-06-13的CT片比较,肝S5出现新发病灶,考虑转移。肠系膜根部淋巴结及左侧侧锥筋膜前方结节较前有所缩小,见 图2。下一步的治疗如何选择:局部治疗?化疗?靶向治疗?
杨学宁:患者曾行姑息性手术,腹腔情况可能复杂,外科微创治疗可能存在难度,可能需开腹手术,结合肝病灶位置,考虑手术完整切除且对诊断有帮助。
陆骊工(介入科教授):结合患者病史及CT图像上病灶的表现,可选择射频消融术,或是亚氦刀局部治疗,可减少疼痛。
旁述:NCCN结肠癌临床指引(2012)有些患者由于伴发病或者转移瘤的位置而不能切除或者手术切除后剩余肝脏不足以维持正常生理功能,可以采用消融治疗。
杨冬阳:患者于2012-09-25行肝S5病灶射频消融术,术后CT图像见 图3。消融术后下一步的治疗方法如何选择?
曹小龙:患者新发肝病灶已局部治疗,结合CEA情况,如稳定可继续卡培他滨维持治疗。
吴一龙:对于每个病例,我们要总结成功的地方、不成功的地方,对于该病例来讲,在内科治疗阶段,经过了三个阶段,第一阶段治疗是化疗加抗血管生成剂治疗,第二阶段是卡培他滨继续治疗,第三阶段是发现肝新病灶,进行局部射频消融处理。该患者的治疗主要在前两个阶段,其中哪一阶段患者获益更多,是我们回顾病例时需重点考虑的,是诱导治疗阶段获益多,还是维持治疗阶段获益多,还是维持治疗只是锦上添花、或是安慰治疗?
马冬:我们认为诱导及维持治疗都发挥了作用,在诱导治疗期间靶病灶缓慢缩小,维持治疗期间复查时原来靶病灶仍有缩小。
吴一龙:如何评价疗效有客观指标观察,如第一阶段化疗加靶向治疗的获益与相关临床研究结果对比,如获益较临床试验的方案好,证明该方案治疗效果好,另一个指标是CEA标志物,从治疗开始降到正常,后再升高,对照诱导及维持治疗阶段进行评价,如果诱导治疗阶段CEA降至正常,而维持治疗时CEA未升高,提示维持治疗可能继续维持诱导治疗时的效果,如果维持治疗时CEA升高,那可能提示维持治疗效果不好,该患者诱导化疗期间CEA降至正常,维持治疗时CEA未升高,提示患者最大获益在诱导治疗阶段,对比该患者治疗获益与相关研究结果并未体现更好的疗效,不能体现维持治疗带来的效果。可为下一步治疗选择提供参考。另一个问题是出现肝独立病灶,这是比较特殊的进展,不是原发病灶的进展。按照原来内科学的标准评价就是进展,需更换治疗方案,但如果原来病灶不发展,而是新发孤立病灶,不认为原来原发病灶的治疗是失败的,陈志勇和钟文昭的一篇肺癌文章在晚期患者里提出“混合疗效关系”问题,指在肺癌里一些病灶控制得好,却突发一些新的病灶,在仔细分析后认为新发病灶在分子学角度跟原来病灶不一样,提出新的治疗方案,原来的病灶继续原方案,新的病灶采用独立方式处理。一个国际著名内科专家进行了详细评述,认为这里提出一个重要概念,为靶向治疗提出新认识,在化疗领域是否存在同样问题,在其他肿瘤是否也存在同样问题。既往认为一个地方失败就需更换原全部治疗方案的认识可能不是最佳选择。结合到该病例,我认为治疗方法选择得当。进一步从腹腔影像学评价有困难,我们就看CEA,局部治疗后CEA从升高降至正常水平,可考虑由该病灶引起CEA升高,经局部治疗已控制可认为是混合疗效关系,结合之前内科治疗获益第一阶段疗效仍在持续,可能不是维持治疗带来的,可以观察。我们对每个病例都要好好总结,以指导下一步的治疗。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|