| 杨学宁,中山大学肿瘤学博士。广东省人民医院副主任医师。国际肺癌研究会(IASLC)会员,中国抗癌协会会员。现任广东省人民医院肺癌研究所副所长,中国抗癌协会肺癌专业委员会常委兼秘书,广东省医学会循证医学专业委员会主任委员,《循证医学》杂志副主编。 长期从事胸部肿瘤多学科综合治疗临床工作,主要研究方向为以外科为主的肺癌多学科综合治疗。近年来参与组织多个有关非小细胞肺癌围术期化疗的多中心随机对照研究,参与多个国际国内多中心随机对照临床研究。参加国家“十五”重大科技专项、国家卫生部和广东省科委等多项科研项目。作为共同参与者获广东省科学技术进步奖二等奖一项。专著《肺癌多学科综合治疗的理论与实践》副主编。在国内外学术期刊发表论文四十余篇。 |
Goss GD, O' Callaghan C, Lorimer I, et al. Gefitinib versus placebo in completely resected non-small-cell lung cancer: Results of the NCIC CTG BR19 study[J]. J Clin Oncol, 2013, 31(27):3320-3326.
1b。
完全切除的非小细胞肺癌(non-small cell lung cancer, NSCLC)患者预后仍不理想, 2002年BR19研究启动时, 以铂类为基础的术后辅助化疗尚未建立, 在前期的几项Ⅱ 期临床研究中, 吉非替尼在NSCLC患者中显示出较好的疗效。鉴于NSCLC患者术后辅助化疗只获得了轻微的生存改善, 而吉非替尼针对晚期NSCLC显示出活性, 结合吉非替尼的毒性可以接受以及口服给药的特点, 从而进行了本项研究, 探究NSCLC术后辅助吉非替尼治疗的疗效。
评估NSCLC完全切除术后吉非替尼辅助治疗对患者生存期的影响及毒性反应。
• 研究条件:由加拿大国立癌症研究所临床试验组(NCIC CTG)与美国国立癌症研究所临床试验单位合作实施。
• 研究起止时间:2002年9月至2005年4月。
• 研究方法:多中心、前瞻性、双盲、随机、安慰剂对照、Ⅲ 期临床试验。
• 研究对象:入组标准:年龄大于18周岁; 完全切除术后, 病理证实Ⅰ B、Ⅱ 或Ⅲ A期NSCLC; PS评分0~2分。排除标准:接受肺段切除术或者楔形切除术者; 5年内患有其他恶性肿瘤者; 混合小细胞或类癌成分的混合型肿瘤; 多原发癌; 临床症状明显或者未经治疗的眼病或胃肠疾病者; 临床症状明显的心功能不全、活动性感染或神经精神障碍。
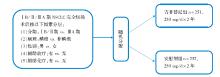
• 干预措施:流程图见图1。
• 评价指标:主要终点指标为总生存期(overall survival, OS), 次要终点指标为毒性反应、无病生存期(disease-free survival, DFS)等。
总共入组503例患者, 251例随机分入吉非替尼组, 252例随机分入安慰剂组。吉非替尼组的中位DFS为4.2年, 安慰剂组的中位DFS尚未达到, 两组间差异无统计学意义[风险比(hazard ratio, HR)=1.22, 95%可信区间(confindence interval, CI) 0.93~1.61, P=0.15, 见图2A]。Cox回归分析显示, 吉非替尼为潜在的有害因素(HR=1.27, 95%CI 0.96 ~1.69, P=0.096)。
吉非替尼组的中位OS为5.1年, 安慰剂组的中位OS尚未达到, 两组间差异无统计学意义(HR=1.24, 95%CI 0.94~1.64, P=0.14, 见图2B)。Cox回归分析显示, 年龄≥ 65岁(HR=1.42, 95%CI 1.05~1.91, P=0.02)以及肿瘤≥ 4 cm(HR=1.72, 95%CI 1.28~2.30, P=0.003)与预后不良相关, 而吉非替尼为潜在的有害因素(HR=1.27, 95%CI 0.96 ~1.69, P=0.097)。
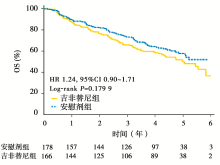
503例患者中, 有359例进行了EGFR突变检测, 其中344例患者为野生型, 只有15例(4%)患者存在EGFR突变。在344例EGFR野生型患者中, 吉非替尼组没有DFS(HR=1.28, 95%CI 0.92~1.76, P=0.14)和OS(HR=1.24, 95%CI 0.90~1.71, P=0.179 9, 见图3)的获益; 同样, 在15例EGFR突变型患者中, 也没有看到吉非替尼组在DFS(HR=1.84, 95%CI 0.44~7.73, P=0.40, 图4A)和OS(HR=3.16, 95%CI 0.61~16.45, P=0.15, 图4B)的获益。
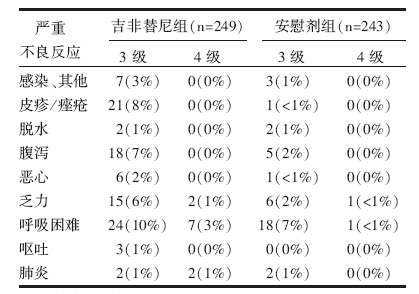
相比安慰剂组, 吉非替尼组皮疹、皮肤干燥、腹泻、厌食、恶心的发生率更高, 但胸痛、肌肉疼痛、呼吸困难的发生率更低。两组的严重不良反应见表1。
| 表1 两组的严重不良反应∗表内数据为人数(百分比) |
术后辅助吉非替尼治疗不能使NSCLC患者获益。
2014年, 《中国医学论坛报》在全国范围内做了一项术后辅助治疗的调查显示, 对于1例Ⅰ B期腺癌(肿瘤大小4.5 cm, EGFR EX19 Del)病例, 148位受访专业医生中, 有62%支持术后辅助化疗, 其中有51%的医生支持辅助表皮生长因子受体(epidermal growth factor receptor, EGFR)酪氨酸激酶抑制剂(tyrosine kinase cinhibitor, TKI)治疗[1]。这一调查显示, 我国的临床医生对于术后辅助EGFR-TKI的疗效非常乐观。但让临床医生们如此乐观的证据在哪里呢?
2002年BR19研究启动时, 术后辅助化疗尚未成为标准[2]。奠定含铂双药术后辅助化疗标准的IALT研究要到2004年发表。吉非替尼作为一个全新机制的靶向治疗药物, 在Ⅱ 期临床研究(IDEAL1、IDEAL2)中发现, 对NSCLC二线及二线以上治疗的有效率达到9%~19%, 优于当时的二线标准细胞毒性药物多西紫杉醇的7.1%。还有非常重要的一点, 相对于细胞毒性化疗药物, 吉非替尼的毒性似乎可以忽略不计。在此利好数据的鼓舞下, 吉非替尼在2001-2003年间对NSCLC“ 四期出击” , 开展了多项Ⅲ 期随机研究, 有针对晚期的一线研究INTACT1/INTACT2(阴性结果, 2004年), 针对晚期二线的ISEL研究(阴性结果, 仅亚组分析显示东方人和非吸烟者获益, 2004年)和INTEREST研究(非劣效, 2008年), 针对局部晚期NSCLC化放疗方案后吉非替尼维持治疗的S0023研究(阴性结果, 2008年), 针对完全切除术后辅助治疗的BR19研究(阴性结果, 2013年)。这些研究有个共同的特点, 就是没有根据EGFR突变状态选择患者, 结果是除了INTEREST研究的非劣效性设计达到目标, 其他三项研究都铩羽而归, 这其中就包括2013年发表的BR19研究。
站在今天的角度看, BR19研究有以下缺陷:
(1)研究入组未经选择的完全切除术后的Ⅰ B~Ⅲ A期NSCLC患者。今天, 我们已经明确了没有敏感靶点的EGFR-TKI治疗无益。
(2)入组病例数不足。计划入组1 050例, 实际仅入组503例, 最终报告的突变亚组数据分析只来自15例患者, 突变患者太少致无法进行有效分析。突变患者少也与入组患者中吸烟(占89%)、鳞癌患者多有关。
(3)吉非替尼疗程不足。原计划是吉非替尼辅助治疗2年, 但由于BR19提前结束, 实际中位服药时间仅4.8个月。
有以上三个主要缺陷, 即使BR19研究没有因为ISEL和S0023研究的失败而在2005年4月提前中止, 也必然是阴性结果。
2005年, BR21研究提示EGFR表达情况即EGFR拷贝数和EGFR突变可能预测厄洛替尼疗效[3]。那么, 基于BR21研究的成果设计的研究能否克服以上缺点呢?
2007年开始的RADIANT研究选择性入组EGFRIHC/FISH阳性的Ⅰ B~Ⅲ A期NSCLC病例, 厄洛替尼辅助治疗2年[4]。研究共随机入组973例患者。2014年ASCO报告显示, 厄洛替尼辅助治疗并不能延长总体患者的DFS。分析显示EGFRIHC/FISH和KRAS对于OS和DFS均无预测作用。针对EGFR基因突变(19 Del和L858R)(EGFR M+)的161例患者的亚组分析显示, 厄洛替尼组的中位DFS(46.4 个月vs. 28.5个月, HR 0.61, P=0.039 1)更优。中位OS目前仍未达到。RADIANT研究提示EGFR IHC/FISH阳性并非EGFR-TKI有效的预测因子, 低效的预测方法导致所选择的人群EGFR-TKI治疗效率低, 最终RADIANT研究得到阴性结果。虽然随后增加EGFR基因突变检测以期获得更多的数据, 但已不是设计者的初衷了。
同样是2007年, MSKCC发起了一项厄洛替尼辅助治疗早期可切除的EGFR突变阳性NSCLC患者的单臂、多中心、Ⅱ 期研究— — SELECT研究[5]。2014年报告时入组100例患者。EGFR突变、Ⅰ A~Ⅲ A期NSCLC术后接受常规辅助化疗或放化疗后, 口服厄洛替尼150 mg/d 2年。主要终点指标为2年DFS。中位随访时间为3.4年(17~74个月)。2年DFS为89%(与历史对照的76%相比, P=0.004 7), 但中位DFS时间未达到。研究提示EGFR突变阳性NSCLC患者行2年厄洛替尼辅助治疗是可行的。2年DFS率分别为:Ⅰ 期96%, Ⅱ 期78%, Ⅲ A期91%。Ⅱ 期患者2年DFS劣于Ⅲ 期患者。有学者因此认为, 提示相对早期的患者获益可能不明显。另外, 厄洛替尼的毒性也不小, 11%的患者因为毒性在1个月内停药, 有40%的患者需要减量(24%调整至100 mg, 16%调整至50 mg), 但仍然有69%的患者完成超过了22个月的辅助治疗。研究提示100 mg/d可能是更合适的起始剂量。
SELECT研究是首个报告EGFR突变患者可能从辅助厄洛替尼治疗中获益的前瞻性研究。但该研究只是Ⅱ 期单臂研究, 在没有随机对照研究长期随访结果之前, 仍难以确定TKI术后治疗能否使该类患者获益。
BR19、RADIANT和SELECT这三项研究在设计上逐步深入, 选择性逐渐增强, 结果也大不相同。BR19和RADIANT入组了大量的病例, 但因为没有选择或者错误选择靶向人群, 结果都为阴性。SELECT虽然只有100例患者, 但经过高度选择, 显示出了较好的趋势, 也充分显示出精准治疗时代靶向人群选择的重要性。
以上三项研究都是西方国家开展的以高加索人群为主的研究。我们更加期待在亚洲进行的两个多中心随机对照研究, 中国的CTONG1104(ADJUVANT)和日本的WJOG6410L(IMPACT)研究[5, 6], 这两个研究均在2011年开始入组, 病例数分别为220例和230例, 而且计划最终将会合并数据分析。这两个研究都入组EGFR敏感突变的Ⅱ ~Ⅲ A期(CTONG1104仅入组N1、N2的病例)NSCLC, 口服吉非替尼与标准的长春瑞滨联合铂类对照。与前述三个研究都不同的是, 入组的病例不包括Ⅰ 期患者, 吉非替尼组不接受辅助化疗, 没有安慰剂组。显然, 这两项亚洲研究所入组的患者更可能是真正从辅助治疗中获益的人群, 而且所选择的吉非替尼毒性也更小。这两项研究预计最早到2016年有初步的结果。
在CTONG1104和WJOG6410L研究最终结果出来之前, 仍然无法确定能够从EGFR-TKI治疗中获益的早期人群, 因此不建议EGFR-TKI应用于术后辅助治疗。良好的愿望需要有足够的随机对照研究结果支持, 而不是仅有理论支持。我国的临床医生需要抑制住“ 早用” EGFR-TKI的冲动。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|