| 陆舜, 教授, 医学博士, 主任医师, 博士研究生导师。上海市肺部肿瘤临床医学中心主任。目前参加和承担国家863重大课题、国家十一五科技支撑计划课题和上海市科研基金项目8项。2012年作为第一负责人承担科技部国际合作课题“ 中瑞合作肺癌临床医学中心肺癌诊治关键技术转化医学研究” 。至2014年作为主要研究者之一参与或承担40余项国际国内多中心随机对照临床研究。2010年获上海市医学领军人才, 2013年获上海市优秀学术带头人称号, 2013年获上海市医学科技奖三等奖。 作为第一作者发表论文及论著80余篇, 其中SCI收录30篇。目前担任美国临床肿瘤学会(ASCO)国际事务部委员, Journal of Thoracic Oncology杂志副主编, The Oncologist杂志编委, 中国抗癌协会肺癌专业委员会候任主任委员, 国家食品药品监督管理局新药评审专家, 中华医学会肿瘤学会委员, 中国临床肿瘤协作中心(CSCO)副秘书长、常委, 上海市医学会肿瘤学会候任主任委员, 上海市抗癌协会理事等。 |
Brahmer J, Reckamp KL, Baas P, et al. Nivolumab versus Docetaxel in advanced squamous-cell non-small-cell lung cancer [J]. N Engl J Med, 2015, 373(2):123-135.
1b。
• 晚期肺鳞癌患者一线化疗疾病进展后, 可选择的治疗方案有限。其中以多西紫杉醇化疗应用最广, 一直被认为是晚期肺鳞癌二线治疗的最有效方案。
• 非小细胞肺癌广泛表达程序性死亡配体1(programmed death ligand 1, PD-L1)。活化T细胞表达的程序性死亡1(programmed death 1, PD-1)受体与PD-L1、PD-L2相互作用, 抑制T细胞活化、促进肿瘤的免疫逃逸。
• Nivolumab 为人免疫球蛋白G4单克隆抗体, 可与PD-1受体结合, 阻断PD-1/PD-L1信号通路, 进而修复抗肿瘤免疫。Nivolumab用于既往曾接受治疗的晚期肺鳞癌患者的Ⅰ 、Ⅱ 期临床研究表明缓解率达15%, 甚至接近17%。中位生存期可达8.2~9.2个月, 1年和3年的生存率分别为41%和19%。
比较Nivolumab与多西紫杉醇对晚期肺鳞癌二线治疗的疗效, 评估Nivolumab的疗效及安全性。
• 研究条件:前瞻性, 多国家、多中心参与, Ⅲ 期随机对照临床试验。
• 研究时间:2012年10月到2015年1月。
• 研究对象:年龄≥ 18岁, Ⅲ B或Ⅳ 期肺鳞癌患者, 以铂类为基础化疗中或化疗后疾病进展, ECOG PS评分0或1, 有可提供的基线肿瘤组织标本用于生物学标志物分析。入选患者根据既往有无紫杉醇类药物化疗史和地域因素(美国/加拿大 vs. 欧洲 vs. 其他地区)分层。
• 干预措施:纳入272名患者, 随机分为两组, 135名患者接受Nivolumab治疗3 mg/kg, 每2周为1疗程, 137名患者接受多西紫杉醇治疗75 mg/m2, 每3周为1疗程。
• 评价指标:主要研究终点指标为总生存期, 次要终点指标包括:客观缓解率、无进展生存期、患者报告结局、肿瘤PD-L1表达差异相关的疗效以及安全性。
272名患者随机入组, 260名(96%)患者接受了研究药物的治疗, 其中131名进入Nivolumab组, 129名进入多西紫杉醇组, 最短随访期为11个月。中位年龄为63岁, 以男性、ECOG PS 1分、Ⅳ 期、现在或既往吸烟者居多。所有患者都曾接受含铂药物化疗, 34%患者曾接受多西紫杉醇化疗。两组间人口统计学及临床特征总体均衡性较好, 在女性、≥ 75岁、ECOG PS 1分的患者比例上略有差异。
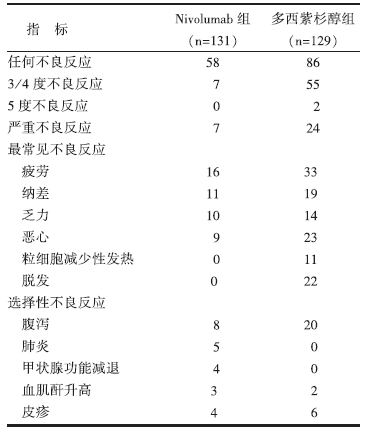
Nivolumab组和多西紫杉醇组的中位生存期分别为9.2个月和6.0个月。Nivolumab组总生存期较多西紫杉醇组长, 差异有统计学意义(P< 0.001)。Nivolumab组和多西紫杉醇组的客观缓解率分别为20%和9%, Nivolumab组客观缓解率高于多西紫杉醇组, 差异有统计学意义(P=0.008 3), Nivolumab组的中位无进展生存期为3.5个月, 多西紫杉醇组为2.8个月, 相较于多西紫杉醇组, Nivolumab组无进展生存期延长, 差异有统计学意义(P< 0.001)。具体见表1。
225名(83%)随机分组患者的肿瘤组织可定量检测PD-L1的表达情况。两治疗组间PD-L1阳性率基本均衡。按预先设定的表达水平(1%、5%、10%), PD-L1的表达不是任何疗效终点的预后或预测性因素。按PD-L1表达水平进行亚组分析, Nivolumab治疗组较多西紫杉醇组总生存期及无进展生存期长, 且比率与初始群体相似。无论患者肿瘤组织PD-L1阳性或阴性, Nivolumab组都较多西紫杉醇组客观缓解率更高。
Nivolumab组治疗相关的不良事件(58% vs. 86%)及严重不良事件发生率(7% vs. 24%)均低于多西紫杉醇组。Nivolumab组最常见的不良事件报告包括疲劳(16%)、纳差(11%)以及乏力(10%)。多西紫杉醇组最常见的不良事件报告包括粒细胞减少(33%)、疲劳(33%)、脱发(22%)以及恶心(23%)。见表2。
Nivolumab组因不良事件终止研究的发生率低于多西紫杉醇组(3% vs. 10%)。在Nivolumab组, 肺炎是导致研究终止的最常见不良事件(2%), 在多西紫杉醇组, 周围神经病(3%), 疲劳(2%)是导致研究终止的最常见不良事件。治疗相关性死亡事件在两组分别是0例(Nivolumab组)和3例(多西紫杉醇组)。
| 表1 两治疗组的疗效比较 |
| 表2 两治疗组的不良事件比较 % |
• 对以铂类为基础化疗中或化疗后发生疾病进展的晚期肺鳞癌患者, Nivolumab较多西紫杉醇治疗显著改善总生存期、客观缓解率和无进展生存期。
• Nivolumab 疗效与肺鳞癌患者肿瘤组织PD-L1表达水平无关。
新英格兰医学杂志于2015年5月31日在线发表了CheckMate 017研究的结果, 几乎与美国临床肿瘤学年会(ASCO)同步报道, 可见业界对该研究的重视。
一项Ⅲ 期随机临床试验提前终止通常发生在两种情况:一种是治疗组的疗效和安全性远远优于对照组, 不需要按照预定的设计方案完成整个试验也可以获得有统计学意义的明显差异, 另一种是对照组的临床结果远不如预期, 即不如其试验组。既往大多数提前终止的临床试验属于后者。而2015年1月独立评审委员会建议提前终止CheckMate 017研究, 理由是在肺鳞癌的二线治疗中, PD-1单抗Nivolumab治疗组的总生存期明显优于多西紫杉醇对照组, 死亡风险下降 41%。
CheckMate 017 是一项Ⅲ 期、随机、开放试验, 比较PD-1抗体Nivolumab 和多西紫杉醇对既往接受过治疗的晚期肺鳞癌的疗效和安全性。272例晚期肺鳞癌患者一线含铂化疗失败后, 按1∶ 1比例随机化, 其中135例患者接受根据Ⅰ 期临床研究推荐的Nivolumab治疗剂量(3 mg/kg q2w), 另外137例患者接受多西紫杉醇治疗(75 mg/m2 q3w)。该研究的主要终点指标是总生存期, 次要终点指标包括:客观缓解率、无进展生存期、PD-L1表达与临床疗效的相关性和安全性。两组在年龄、性别、疾病分期、体力状态、脑转移、既往使用紫杉醇、吸烟史和PD-L1表达水平等基线特征方面都较均衡。结果提示Nivolumab治疗组与多西紫杉醇治疗组的总生存期分别为9.2个月和6个月[风险比 0.59(95%可信区间 0.44~0.79), P=0.000 25]; 无进展生存期分别为3.5个月和2.8个月[风险比0.62 (95%可信区间0.47~0.81), P=0.000 4]; 客观缓解率分别为20%和9%(P=0.008 3), 且前者较后者的缓解持续时间更长; 但是肿瘤组织的PD-L1表达状态与临床疗效没有明显相关性; 在安全性方面, 无论是血液学或非血液学毒性, 前者均较后者更少和更安全。
这是一项高质量的随机临床试验, Nivolumab的主要终点指标和所有次要终点指标均优于多西紫杉醇, 结合先前的CheckMate 063等的研究结果[1], 最终推动美国FDA在2015年3月正式批准Nivolumab用于晚期肺鳞癌的二线治疗[2]。但该研究也提出了一些尚未解决的问题, 需要我们在临床实践中加以重视。
Nivolumab 获益不依赖于PD-L1 表达。该研究运用免疫组化方法对肿瘤标本的PD-L1表达进行检测, 并分别以1%、5%和10%三个PD-L1表达水平为判断标准进行分组分析。但所有组别都提示Nivolumab 获益与PD-L1 表达状态没有相关性。早期临床研究曾提示, 肿瘤细胞PD-L1表达水平与针对PD-1或PD-L1治疗的疗效相关, PD-L1高表达患者的缓解率可达80%, 但同时发现PD-L1低表达患者也可以从相应治疗中获益[3]。CheckMate 017研究者对于该研究未发现两者有相关性的解释是, 检测结果来源于既往保存下来的标本, 不能反映患者治疗时的PD-L1状态, 另外仅有83%(225/272)的患者可以进行PD-L1检测。笔者认为, 肿瘤细胞与免疫系统间的关系十分复杂, 单独的PD-L1表达水平是否能帮助选择获益人群仍需要探索。另外, 免疫组化是否是最佳的检测方法, 是否会存在类似既往EGFR的FISH检测与EGFR的突变检测之争, 肿瘤细胞PD-L1状态是否会动态变化。在肠癌中发现错配修复(MMR)基因缺陷与PD-1抑制剂疗效密切相关, 在肺癌中是否也会有相似的结果, 这些都需要进一步研究加以阐明。但是, 在今年ASCO上又有报道提示其他公司的类似产品疗效与 PD-L1的表达有关。当前有关 PD-L1免疫组化检测尚没有统一标准, 不同研究采取不同抗体, 未来需要标准统一的方法。
RECIST评估标准是否适用于免疫治疗的疗效评估尚属争议。在该研究的无进展生存曲线中, Nivolumab治疗组与多西紫杉醇治疗组在1.5个月之前, 两条生存线是粘合在一起的, 并无差别。在Nivolumab治疗组中, 28例患者在初次Nivolumab治疗进展、继续运用Nivolumab后, 仍有19例患者能继续获益。因此, 为化疗量身定做的RECIST标准能否准确地评估免疫治疗的疗效, 值得临床医师给予关注。可能需要建立更准确的免疫治疗评估体系。
在CheckMate 017中, 总体上Nivolumab较多西紫杉醇的治疗毒性反应更小。但是, 临床医师也需要注意到, Nivolumab治疗组中也有3例因为不良事件发生而终止治疗, Nivolumab治疗组的肺炎发生率要高于多西紫杉醇治疗组。这可能是由于间质性肺炎的产生和自身免疫反应相关。而中国是结核和乙型肝炎高发国家, 未来在中国进行的临床研究更需关注此类反应。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|