| 徐卫, 女, 医学博士, 南京医科大学第一附属医院(江苏省人民医院)血液科副主任, 教授、主任医师、博士研究生导师, 淋巴瘤首席专家; 国家临床重点专科、兴卫工程重点学科(共建)、江苏省高校优秀科技创新团队及医院淋巴肿瘤研究创新团队的主要学科负责人、学术带头人。目前任中国抗癌协会血液肿瘤专业委员会委员兼秘书长、中华医学会血液学分会实验诊断组委员、CSCO中国抗淋巴瘤联盟委员、中国病理生理学会实验血液学专业委员会委员、江苏省抗癌协会血液肿瘤专业委员会副主任委员、江苏省抗癌协会淋巴瘤专业委员会常委、江苏省血液学会委员兼秘书、南京市血液学会委员; 江苏省“ 兴卫工程” 优秀医学重点人才, 江苏省“ 333工程” (第二层次)、“ 六大人才高峰” 、“ 青蓝工程” 中青年学术带头人培养对象; 《中华血液学杂志》、《中国实验血液学杂志》、《国际输血和血液学杂志》、《白血病· 淋巴瘤》和《南京医科大学学报》编委。以第一作者/通讯作者发表SCI论文70余篇(IF> 5分12篇), 主持完成或正在进行的科研项目包括国家自然科学基金(面上项目3项)10余项; 获省部级奖4项。 |
Rummel MJ, Niederle N, Maschmeyer G, et al. Bendamustine plus Rituximab versus CHOP plus Rituximab as first-line treatment for patients with indolent and mantle-cell lymphomas: An open-label, multicentre, randomised, phase 3 non-inferiority trial[J]. Lancet, 2013, 381(9873):1203-1210.
1b。
利妥昔单抗联合包含环磷酰胺、阿霉素、长春新碱和泼尼松的R-CHOP方案是目前治疗进展期惰性非霍奇金淋巴瘤(indolent non-Hodgkin´ s lymphoma, iNHL)和套细胞淋巴瘤(mantle cell lymphoma, MCL)常用的一线方案。
研究表明, 苯达莫司汀单药或联合利妥昔单抗(Bendamustine plus Rituximab, BR)治疗复发难治淋巴恶性肿瘤具有良好的疗效及较低的毒性反应。
一线选择BR方案对于iNHL和MCL的长期疗效及安全性尚存在争议。
比较BR方案和R-CHOP方案作为一线治疗iNHL和MCL患者的有效性及安全性。
• 研究条件:来自德国的81个中心。
• 研究时间:2003年9月至2008年8月。
• 研究方法:开放性、多中心、随机、对照、非劣效性、Ⅲ 期临床试验。
• 研究对象:> 18岁, PS≤ 2, 组织学确诊为CD20阳性的MCL或iNHL, 包括1或2级滤泡淋巴瘤(follicular lymphoma, FL)、淋巴浆细胞淋巴瘤(lymphoplasmacytic lymphoma, LPL)(华氏巨球蛋白血症)、小淋巴细胞淋巴瘤(small lymphocytic lymphoma, SLL)以及边缘区淋巴瘤(marginal zone lymphoma, MZL)。所有患者既往均为Ⅲ /Ⅳ 期未接受治疗的MCL或iNHL, iNHL必须具有以下指征之一:①造血系统受累(血红蛋白< 100 g/L, 中性粒细胞计数< 1.5× 109/L, 或血小板计数< 100× 109/L); ②B症状; ③高肿瘤负荷(3个累及区域> 5 cm或1个区域> 7.5 cm), 大肿块影响脏器功能, 6个月内肿瘤体积增大50%, 高粘滞综合征。
• 干预措施:随机接受R-CHOP或BR方案治疗, 试验方案设计见图1。
• 评价指标:主要终点指标为无进展生存时间(progression-free survival, PFS); 次要终点指标包括总缓解率(overall response rate, ORR)、完全缓解率(complete response, CR)、急性和迟发毒性、总生存期(overall survival, OS)、至下一次治疗时间、无事件生存期(event-free survival, EFS)。
中位随访时间45个月(范围29~57个月), BR组的PFS显著长于R-CHOP组(69.5个月vs. 31.2个月, P< 0.000 1), 进一步亚组分析各类型淋巴瘤, 除MZL外, BR组的PFS均显著长于R-CHOP组。两组ORR相似(93% vs. 91%), 而BR组的CR显著高于R-CHOP组(40% vs. 30%, P=0.021), 至下一次治疗时间BR组也明显长于R-CHOP组(P< 0.000 1)。BR组43人死亡, R-CHOP组45人死亡, 两组OS无显著差异。
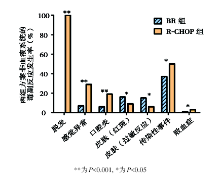
R-CHOP组的严重毒副反应发生率为29%, 明显高于BR组的19%, 3/4级白细胞及中性粒细胞减少发生率也显著高于BR组(P< 0.000 1)。两种方案非血液系统的其他毒副反应发生率比较见图2。
BR一线治疗iNHL及MCL较R-CHOP方案的PFS更佳、毒性更小, 而OS无显著差异, 因此BR方案不劣于R-CHOP方案, 且具有更小的毒副反应。
iNHL占所有非霍奇金淋巴瘤(NHL)的30%~40%, 恶性程度低, 发展缓慢, 多次复发并可进展为侵袭性淋巴瘤, 常规化疗可在一定程度上获得缓解, 但长期随访OS并无显著改善。MCL作为一种侵袭性极强的淋巴恶性肿瘤, 进展迅速, 对化疗敏感但最终难免复发。近年来, 淋巴瘤治疗方案不断优化, 对于年轻患者, 着重于加大化疗强度, 提高治疗有效率; 对于年老体弱的患者, 强调低强度化疗, 应用分子靶向药物替代高强度化疗, 延长缓解时间。由于iNHL及MCL好发于老年患者, 选择合适的化疗方案、最大限度地降低化疗的毒副作用、延长患者的生存时间、提高患者的生活质量成为研究重点。
苯达莫司汀单药或联合利妥昔单抗在复发难治iNHL及MCL中显示出良好的疗效及安全性。因此, 来自德国的多中心前瞻性研究比较了一线R-CHOP方案与BR方案治疗iNHL及MCL的疗效和安全性。共入组549例确诊为iNHL或MCL患者, 275例接受6周期R-CHOP方案, 274例接受6周期BR方案, 最终结果显示BR方案的中位PFS以及至下一次治疗时间均显著长于R-CHOP组, CR也显著高于R-CHOP组, 而OS无显著差异。进一步分析其他危险因素, 无论患者年龄> 60岁或≤ 60岁, BR均较R-CHOP显著延长PFS; 而在FL中, 无论FLIPI评分高低, BR组的PFS均较长。该研究另一结论为BR方案的3/4级血液学毒性及重度感染的发生率显著低于R-CHOP组; 此外, 在BR组中没有1例患者出现脱发, 而在R-CHOP组脱发的发生率为100%, 虽然化疗引起的脱发并不是影响寿命的副反应, 但却严重影响患者的生活质量。两组第二肿瘤发生率相似, 但由于较短的随访时间及较少的样本量, 并不能判断BR是否会引起第二肿瘤的发生率增高。
近期, 另一项来自加拿大的BRIGHT多中心临床试验同样比较了BR与R-CHOP(R-CVP)治疗初诊iNHL和MCL的疗效, BR组的CR显著高于R-CHOP组(40% vs. 26%, P=0.033), R-CHOP组的3/4级中性粒细胞减少及周围神经病变发生率高于BR组, 而感染的发生率并未较BR组高。因而BR的疗效不劣于R-CHOP, 而毒副反应尚可接受, 该结论与评价文章相似。
该研究也同样存在一些不足, 如并未在诱导缓解后给予患者巩固维持治疗, 使得R-CHOP组患者的疗效差于同类临床试验结果, 同时中位随访时间较短, 病例数量较少等也限制了该研究结果的说服力。
总之, 从目前的证据来看, R-CHOP方案的疗效并不优于BR方案, 反而增高了严重不良事件的发生率, 对于老年或体能状态较差的患者更加倾向于选择BR方案。随着随访时间的延长以及更多大样本临床试验的开展, 可以帮助研究者更好地选择适合不同患者的个体化治疗方案。
The authors have declared that no competing interests exist.