| 朱正飞, 肿瘤学博士, 副主任医师, 复旦大学硕士研究生导师。复旦大学附属肿瘤医院放疗科。中国抗癌协会肺癌专业委员会放疗学组委员, 中国抗癌协会食管癌专业委员会委员, 世界华人肿瘤医师协会放射治疗协作组常委, 上海市抗癌协会胸部肿瘤专业委员会委员, 上海市医师协会肿瘤科医师分会委员, 《Journal of Thoracic Disease》杂志审稿专家, JCO中文版编委会青年委员。主要从事胸部肿瘤放射治疗及综合治疗相关的临床与基础工作。2012年3月至2014年3月在美国MD Anderson肿瘤中心放疗科以访问学者身份学习2年。2015年入选上海市浦江人才计划, 以项目负责人身份承担国家自然科学基金(面上项目)、教育部留学回国人员科研启动基金、上海市自然基金、上海市卫计委课题(面上项目)等项目共6项。发表论文40余篇, 其中第一作者/通讯作者文章16篇, 第一作者/通讯作者SCI收录论文9篇。 |
Johung KL, Yeh N, Desai NB, et al. Extended survival and prognostic factors for patients with ALK-rearranged non-small-cell lung cancer and brain metastasis[J]. J Clin Oncol, 2016, 34(2):123-129.
2A。
• 中枢神经系统转移在晚期肺腺癌的发生率约为30%, 中位总生存期(overall survival, OS)为3~14.8个月。
• 约5%的非小细胞肺癌(non-small cell lung cancer, NSCLC)患者可发生ALK基因重排, 其靶向药克唑替尼对颅内病灶控制不理想。
• 脑转移局部治疗手段有全脑放疗(whole-brain radiotherapy, WBRT)、立体定向放射外科手术(stereotactic radiosurgery, SRS)治疗和外科切除; 但并无对ALK重排脑转移NSCLC患者的详细报道。
明确ALK基因重排伴有脑转移的NSCLC患者的生存情况及预后相关因素。
• 研究条件:病例来自美国6家机构, 包括科罗拉多大学(n=33)、耶鲁大学(n=17), 纪念斯隆凯瑟琳癌症中心(n=14)、俄亥俄州立大学(n=11)、达纳-法伯癌症研究所(n=9)和范德堡大学(n=6)。
• 研究起止时间:2007-2014年。
• 研究方法:多中心回顾性临床研究。
• 研究对象:ALK重排伴脑转移NSCLC患者, 评估为需放射治疗。
• 干预措施:收集患者的年龄、KPS评分、吸烟史、诊断时的疾病分期、到发生脑转移的时间、脑转移灶的数目和颅外转移等基本情况, 并收集患者的治疗时间、随访情况、中枢神经系统疾病控制情况和放疗的特征、化疗、TKI治疗和神经外科干预情况等。脑转移时的全身疾病状态分为:稳定、寡进展(≤ 4个部位颅外转移灶恶化)和进展。
• 评价指标:OS、颅内病灶的中位无进展生存期(progression-free survival, PFS)。OS定义为从诊断脑转移到死亡的时间, 颅内进展是指从诊断脑转移到第一次脑内进展的时间。并通过多因素分析鉴别独立的OS预测因素, 应用Kaplan-Meier 分析法计算中位OS和2年生存率。
(1)共90例ALK重排的NSCLC发生脑转移的患者纳入研究, 脑转移后的中位OS为49.5个月[95%可信区间(confidence interval, CI)29.0个月~未达到], 颅内病灶的中位PFS为11.9个月(95%CI 10.1~18.2个月)。
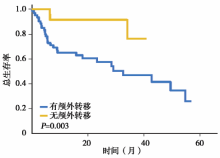
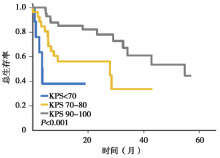
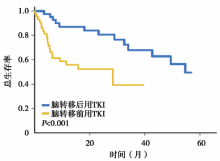
(2)无颅外转移、KPS评分≥ 90以及脑转移前未使用过TKI为好的预后因素, 见图1~图3。而单发脑转移以及给予SRS或WBRT则不是。
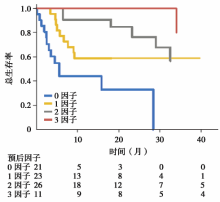
(3)KPS< 90、颅外转移和既往用过TKI的患者的2年生存率为33%; 同时具备1、2和3个好的预后因子患者的2年生存率分别为59%、76%、100%。见图4。
• SRS/WBRT及TKI的应用, 延长了ALK重排伴脑转移的NSCLC患者的OS;
• 无颅外转移、KPS评分≥ 90以及脑转移前未使用过TKI为ALK重排伴脑转移NSCLC患者好的预后因素。
近年来对于实体肿瘤脑转移的局部治疗策略逐渐发生了一些变化, 主要体现在SRS的地位得以确立[1, 2]; 在能够实施SRS治疗的患者中不建议WBRT早期参与[3, 4, 5]; 对脑部转移灶个数超过3个或4个的患者若技术条件允许也可考虑进行SRS治疗[6]。对NSCLC脑转移而言, 除上述局部治疗策略的变化以外, 对有EGFR基因敏感突变或者ALK阳性患者的整体治疗策略也在发生着变化:尤其对于那些无神经系统症状或者症状轻微能被糖皮质激素等药物很好控制的患者, 不少学者推荐首先进行相应靶点TKI药物的治疗而脑部局部治疗暂缓。
本研究虽属回顾性分析, 但它确给我们提供了不少有用的信息:第一, 这项研究第一次告诉了我们在真实世界中ALK阳性NSCLC脑转移患者的总体生存水平, 这是在去年所发表的基于PROFILE 1005和1007两项前瞻性研究的后续分析数据[7]中所没能提供的。第二, 传统的预后评分系统, 如GPA, 在ALK阳性患者中可能并不能胜任, 这类患者的生物学特性不同于其他患者。第三, 验证了去年发表的研究中[7]所显示的, ALK阳性脑转移患者经ALK-TKI参与治疗后患者颅内病灶有较好的控制率。这些均为以后相关前瞻性临床试验设计中终点指标的预设、分层因素的选择等提供了很有价值的参考。
诚然, 这项研究也有它作为回顾性分析本身的局限性。第一, 患者脑转移的诊断技术没有标化。虽然98%的患者采用MRI作为诊断脑转移的工具, 但不同的MRI技术条件本身会对脑转移诊断的准确性有较大的影响, 尤其是对较小转移灶诊断的敏感性[8]。本研究纳入的患者来自6个中心, 不同中心甚至同一中心不同患者所采用的MRI技术不可能完全一致。因此个人认为, 在本研究中所发现的单个与多个脑转移灶患者总生存无差别并不能单纯归结于ALK患者本身生物学特性的原因, 也可能部分与诊断技术带来的选择性偏倚有关。第二, 本研究显示, 在ALK-TKI使用之前已行过脑部放疗的患者生存时间延长, 这可能与脑部放疗对于转移灶本身的控制效应以及放疗对于血脑屏障的破坏从而增强了药物疗效有关。然而, 在本研究中放疗与否及其所采用的技术如何选择并没有统一的标准, 选择的主观因素较强, 因此并不能以此研究明确在ALK阳性脑转移患者中放疗该如何参与。第三, 在这项研究中, WBRT的使用有提高颅内病灶控制率的趋势, 但作为首次脑部放疗参与时所采用的技术, SRS与WBRT治疗患者的总生存并无差别, 这可能与后续脑部挽救性局部治疗的积极参与有关。正如原文讨论部分所提, 本研究缺少患者生活质量以及神经认知功能评估的数据, 因此难以确立一线脑部放疗技术的取舍。
本研究结果显示ALK阳性的NSCLC脑转移患者经过脑部放疗及ALK抑制剂参与治疗后的中位生存时间可达到49.5个月, 这也再次证实脑转移患者是个异质性很强的群体, 其中部分患者经过合理的治疗后可获得较长期的生存甚至有潜在治愈的可能。对于预后好的脑转移患者, 在治疗方案的选择时需要更加注重脑部局部治疗手段对于患者神经认知功能以及总体生活质量的影响, 如WBRT时机的选择, WBRT中对于神经认知功能保护措施的使用等等, 但重要前提是, 我们需要有一个准确的预后评分系统来预测患者的预后。在乳腺癌脑转移的GPA预后系统中已把乳腺原发病灶的激素受体与HER表达状况纳入其中[9], 在NSCLC分子靶向治疗已取得很大进步的今天, 如何把相应的分子生物学信息纳入预后评分系统中是值得去研究的方向。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|