编者按: 疾病的正确诊断和合理治疗是患者和医务工作者共同的心愿。在广东省人民医院肿瘤中心,吴一龙教授指导临床医生应用循证医学理论进行肿瘤的多学科综合治疗,开展临床病例讨论。讨论会上各学科共同围绕一个病例或一个病种进行会诊,临床、病理、B超、放射影像等资料齐全,除相关科室提前准备的中心性发言外,到会人员各抒己见,气氛热烈。参会人员受益匪浅,提高了对疑难病例的诊治水平。为了将他们的诊治经验传播出去,让更多的临床医生获益,我刊开辟“循证病例讨论”栏目,希望广大医务工作者关注此栏目。
患者, 男, 55岁, 已婚, 因“ 纳差呕吐半月余, 头晕、右侧面部麻木感1周” 入院, PS=2分。查体:生命体征平稳。皮肤巩膜稍黄染, 左侧鼻唇沟变浅, 伸舌居中。双侧咽反射正常。四肢肌力4级。既往有2型糖尿病、高血压病史, 无吸烟、饮酒史。
2014-12-02血液检查:血小板计数16.4× 109/L, 血红蛋白浓度 98.2 g/L, 白细胞计数 14.17× 109/L, 丙氨酸氨基转移酶18 U/L, 门冬氨酸氨基转移酶105 U/L, 总胆红素35.38 μ mol/L, 乳酸脱氢酶4 570 U/L, 铁蛋白> 15 000 ng/L, 甘油三酯2.65 mmol/L; CEA 26.5 ng/mL, CA-125 63 U/mL, CA19-9 460 U/mL; D-二聚体(比浊法) > 20 000 μ g/L ↑ , 活化部分凝血活酶时间75.2 sec ↑ , 血浆纤维蛋白原含量1.22 g/L ↓ , 血浆凝血酶原时间测定22.3 sec ↑ ; 凝血酶原活动度39% ↓ , 鱼精蛋白副凝试验弱阳性 。
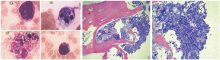
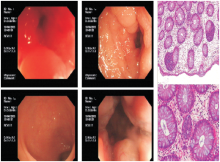
2014-12-04骨髓涂片:骨髓增生减低, 红系减低为主, 分类不明细胞占3%, 噬血细胞占2%, 可见噬血现象。2014-12-09骨髓活检示:转移性腺癌, 结合免疫表型提示肺或下消化道来源, 见图1。
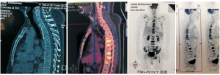
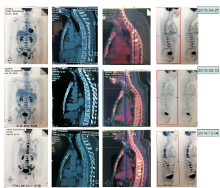
2014-12-04 PET/CT提示乙状结肠癌合并腹腔淋巴结、全身骨髓转移可能, 见图2。
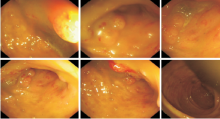
2014-12-08结肠镜检查提示:循腔进镜顺利抵距肛门约20 cm, 考虑结肠肿物, 见图3。因患者凝血功能差、血小板低, 未活检。
患者急性病情, 出现乏力、发热, 血小板、血色素减少, 铁蛋白、甘油三酯、乳酸脱氢酶升高, 肝功能胆红素异常, 凝血功能明显异常, 骨髓涂片可见噬血现象, PS=3分, 诊断噬血细胞综合征, 予输血小板、血浆、纤维蛋白原纠正止凝血障碍、降糖、止血、激素、免疫球蛋白等对症处理, 效果不佳。
杨冬阳(肿瘤内科主治医师):病例汇报略。提出讨论要点:(1)评价病例的诊断和鉴别诊断。(2)晚期肠癌噬血综合征的治疗策略。
马冬(肿瘤内科主任医师):血液肿瘤引起噬血综合征多见, 噬血综合征在实体瘤罕见, 在结直肠癌尚未查到文献报道, 现就我科1例结肠癌合并噬血综合征进行探讨。该患者入院检查提示噬血综合征, 骨髓活检为腺癌, 对于考虑肠癌实体瘤合并噬血表现的患者, 在治疗原发病时, 如何针对明显异常的血液指标及症状进行诊断和治疗?
杨冬阳:患者发热、骨髓活检和骨髓涂片提示噬血现象, 骨髓活检提示腺癌。血小板下降, 凝血功能异常。甘油三酯升高, 肝功能胆红素异常等, 提示噬血综合征。下面请血液科陆泽生主任为我们讲解噬血综合征的诊断和治疗方法。
陆泽生(血液科副主任医师):噬血综合征为未明确原发病的一组表现, 分原发和继发, 该患者入院的相关检查、体征提示有噬血现象, 已达到诊断的标准[1] , 患者已明确考虑结肠转移癌, 倾向考虑为转移性腺癌影响骨髓继发的血液学表现, 因为噬血综合征的死亡率高, 应尽快实施治疗, 改善病情, 防止进一步恶化危及生命, 治疗方法主要以阻断异常的免疫激活如激素、化疗等, 有明确病因的以治疗原发病为主。
旁述:国际组织细胞协会制定的2004年诊断标准, 满足以下2条之一即可建立噬血综合征诊断:(1)符合噬血综合征的分子诊断:PRF1、UNC13D、Munc18-2、Rab27a、STX11、SH2D1A或BIRC4等基因突变; (2)满足以下8条中的5条诊断标准:①发热; ②脾大; ③血细胞减少(影响2或3系外周血细胞):血红蛋白< 90 g/L(新生儿血红蛋白< 100 g/L), 血小板< 100× 10/L, 中性粒细胞< 1.0× 10/L; ④高三酰甘油血症和(或)低纤维蛋白原血症:空腹甘油三酯≥ 3.0 mmol/L(≥ 2.65 g/L), 纤维蛋白原≤ 1.5 g/L; ⑤骨髓、脾或淋巴结中发现噬血细胞现象而非恶变证据; ⑥NK细胞活性减低或缺乏(根据当地实验室指标); ⑦铁蛋白≥ 500 μ g/L; ⑧可溶性CD25(sIL-2R)≥ 2 400 U/mL。
杨冬阳:该患者PET/CT提示乙状结肠癌并腹腔淋巴结、全身骨髓转移可能。结肠镜检查提示:循腔进镜顺利抵距肛门约20 cm, 考虑结肠肿物。因患者凝血功能差、血小板低, 未活检。骨髓活检示:转移性腺癌, 结合免疫表型提示肺或下消化道来源。患者在病因未明的情况下行PET检查使我们对病情有进一步的了解, PET在骨转移和骨髓转移的表现及鉴别的相关评判, 请核医学科为我们讲解。
侯庆仪(核医学科副主任医师):该患者结合PET代谢及CT图像肠癌诊断是明确的。局部肠壁增厚, 考虑为结肠癌, 淋巴结CT图像考虑转移淋巴结, 骨髓代谢异常增高, 从整体角度考虑为多发性骨髓转移, 患者PET的病变结构跟临床的症状时常不一致, 有噬血综合征表现的淋巴瘤较多。骨表象可以是多发或单发的, 代谢不是很高, 可弥漫性分布、对称分布或均匀分布。对于该患者, 我们找到了结肠癌的原发灶。存在骨转移, 虽然没看到骨破坏, 也有可能是破坏前的转移。同时需对病灶的形态、整个骨髓的浸润、骨髓强化的方式等进行判断。一般PET可以比骨扫描更早发现病灶, 即使没有看到骨髓破坏, 骨质微小改变结合病情亦可提示[2]。
吴一龙(肿瘤学教授):在患者未诊断噬血综合征时, 影像学能诊断出来吗?影像学是否可以比较清楚地鉴别骨髓转移和骨转移?
侯庆仪:我们不能报告诊断噬血综合征, 要参考临床, 如能找到原发肿瘤最好, 或是有其他提示血液系统的检查、感染等。PET骨髓扫描比骨扫描、CT可以更早、更敏感地发现骨髓浸润的表现。对于成骨的骨转移, 骨扫描更敏感一些。
李文瑜(淋巴瘤科主任医师):骨转移实体瘤主要看骨质的破坏, 骨髓转移时代谢增高, 弥漫性浸润多认为骨髓转移。
马冬:结直肠癌骨转移较少出现, 单独的骨转移更少[3], 是否需要有了骨穿刺报告的结果才考虑做PET?
陆泽生:PET检查出现骨髓转移的报道数据比较少, 没有大样本量的分析报道。
吴一龙:影像学能否区分出骨髓转移和骨转移?在我印象中, 很难。骨髓转移必须骨穿找到癌细胞, 是这样的概念, 局部侵犯就不同。
杨冬阳:该患者诊断乙状结肠恶性肿瘤CTxNxM1, 骨髓转移, 骨转移?因骨髓活检病理不能检测RAS, 未知RAS状态。患者仍乏力、纳差、发热、疲惫, 腹部及臀部注射部位大面积瘀斑, 病情重, PS评分3分。内科抗感染、输血小板、输红细胞、止血、改善凝血功能等治疗效果不佳, 下一步该如何诊治?
陆泽生:该患者明确原发病是恶性肿瘤, 如果参考白血病或者淋巴瘤, 应在积极支持治疗的前提下化疗, 如原发病不控制是很难治疗症状的, 应根据具体病情制定化疗原则。
马冬:借鉴此办法, 因患者不能口服用药, 选择标准FOLFOX一线治疗, 对结肠癌化疗中度敏感, 考虑患者PS评分差, 联合化疗难以耐受, 但单药有效率低, 将标准FOFOXL方案的同时用药变成序贯, 先5-FU静脉持续滴注, 密切观察, 如患者病情能耐受, 再加用奥沙利铂化疗。
旁述:根据NCCN 2015年肠癌治疗指南, 治疗多发转移结直肠癌的药物既可联合应用也可单独应用, 包括 5-FU/LV、卡培他滨、伊立替康、奥沙利铂、贝伐单抗、西妥昔单抗、帕尼单抗、阿柏西普和瑞格菲尼。治疗选择依据治疗目的、既往治疗类型和时间、治疗药物毒性。若患者体力状态等能耐受较强化疗, 推荐如下五个方案之一:FOLFOX、FOLFIRI、CapeOX、5-FU/LV 或 FOLFOXIRI。
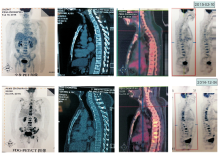
杨冬阳:2014-12-11 开始予5-FU/CF单药晚期一线化疗。2014-12-15患者精神、临床症状均改善, 无发热, 无便血, 脐周及右侧臀部瘀斑减轻, PS评分1分, 2014-12-15改为FOLFOX晚期一线化疗, 至2015-02-09化疗4周期, 患者现PS评分0分, 精神、体力、进食正常。血液检查提示三系减少、凝血功能障碍、肿瘤指标明显改善, 见图4。4周期化疗后PET提示:乙状结肠病变处肠管管壁较前稍变薄, 糖代谢较前稍减低; 多发骨质破坏, 糖代谢较前明显减低。疗效评价为部分缓解, 见图5。期间有Ⅲ 度中性粒细胞减低、Ⅰ 度血小板减低骨髓抑制, 对症治疗后骨髓抑制改善。2014-12-24复查骨髓图片未见转移癌细胞团, 分类不明细胞1%。骨髓活检示:骨髓腔内纤维明显增生, 散在挤压变形的造血细胞。 2015-02-11骨髓涂片示骨髓增生减低, 以红系及巨核细胞减低为主, 血小板少见(外周血可见), 全片观未发现转移癌细胞团。骨髓活检示:骨髓增生极度活跃, 脂肪约占髓腔面积5%; 间质见灶性含铁血黄素沉积。未见肿瘤。下一步的治疗应怎样选择?
陆泽生:肠癌实体瘤很少发现噬血。噬血发生的机制就是细胞的过度激活, 骨髓转移激发相关细胞分泌各种很高的炎症因子, 引起噬血。整个脊髓炎症细胞很活跃, 随着炎症细胞活跃导致肿瘤代谢生长活跃, PET/CT代谢是高的, 化疗后受到抑制, 局部代谢减慢, 代谢下降, 治疗是有效的, 可考虑继续化疗。
马冬:结肠癌转移变成噬血症状, 哪些检测指标可以预测患者会出现骨髓转移?
李文瑜:实体瘤跟淋巴瘤不一样, 难预测。一般来讲实体瘤很少发生单纯骨髓转移, 只能从肿瘤生物学特性、遗传学特征是否有不一样等进一步做分析解释。
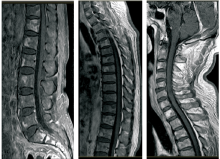
杨冬阳:基于该患者有比较好的疗效, 继续化疗, 从2014-12-15至2015-04-27 FOLFOX晚期一线化疗共8周期, 患者现在PS评分0分, 精神、体力、进食正常。2015-04-10肠镜提示肿块明显改善, 肠镜无法通过去, 病理提示乙状结肠腺癌, 见图6, 我们一直考虑骨质破坏的问题。单纯的骨髓和骨转移治疗是不一样的。2015-04-11进一步椎体MRI:C2、3、5、7, T1、2、4-12及L1-5椎体多发转移瘤。C3/4-C5/6椎间盘突出, L4/5-L5/S1椎间盘膨出, 见图7。8周期PET评估颈椎部分骨代谢增高, 与2月10日比较代谢出现新的变化, 见图8, 下一步应怎样治疗?
马冬: 影像学图像是否提示骨髓有转移再次进展的趋势?肠镜原发灶无法通过, 未来有梗阻可能, 是否需要把握时机行手术切除?
曹小龙(肿瘤内科主任医师):患者进一步的治疗能否考虑放疗干预, 靶向治疗是否也可以考虑?
马冬:患者因一开始异常凝血、出血的病情并有原发灶的表现, 未使用贝伐珠单抗。再次肠镜病理检查RAS状态检测未出, 后续治疗考虑加用靶向治疗。
吴一龙:治疗到现在, 经验体会是什么?长处?短处?下一步策略怎样?
马冬:该患者治疗如按常规肠癌化疗, 可能无法耐受, 开始借鉴血液科经验, 小剂量化疗, 治疗有效, 患者渡过噬血综合征的危险期, 又能耐受化疗, 改善器官功能、改善严重并发症, 使其得到进一步治疗的机会, 可使用标准的两药方案进行治疗, 但一般肠癌一线治疗无进展生存期在10个月内, 该患者也面临治疗失败的瓶颈, 现在已看到进展的趋势, 注意把握原发灶干预的时机, 并进一步选择使用靶向药物。
吴一龙:这个患者有一些基本规律还是可以总结的。第一, 起病时间短, 病情风险极高。第二, 不是实体瘤症状表现, 而是全身症状表现。第三, 有些依据提示化疗有效。5-FU+LV两个配合起来解读, 5-FU是个体化明显的古老药, 可以建立成多种化疗方法, 一个单药效果那么好, 是有内在原因的。从5-FU的代谢酶来看, 是否这患者有特别地方?我们可以探究一下个体化的原因在什么地方。第四, 整个治疗过程使用了FOLFOX方案, 需总结一下, 主要是5-FU起作用还是其他药物起作用?我认为5-FU起主要作用。这个患者单药一直用下去可能也会有效果。假如对5-FU酶能进行检测, 对5-FU可以用得更好。第五, 患者疗效如我们预期, 见效快, 8个周期化疗, 4个月有效期比预期短。不换方案也好, 起码可考虑将靶向药加进去。肠癌原发病灶遗留的问题, 会不会像老特务, 时不时放种子, 在病情相对稳定的情况下让外科把病灶去掉。希望尽快找到 5-FU敏感的原因, 解决了这个问题, 就能解决以后碰到的类似问题!
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|