作者简介:秘营昌,主任医师,博士研究生导师。1990年毕业于山东医科大学,获医学学士学位。1998年毕业于中国协和医科大学,获医学博士学位。2000年11月至2003年1月在美国路易威尔大学做博士后研究。多年来一直从事白血病的临床和基础研究。参与起草我国急性髓系白血病诊断治疗指南、成人急性淋巴细胞白血病诊断治疗指南。 现为国家卫生计生委抗肿瘤药物合理用药专家组成员,中国抗癌协会血液肿瘤专业委员会天津分会副主任委员。中华血液学杂志、中国实验血液学杂志、实用内科杂志编委。
Rollig C, Serve H, Hü ttmann A, et al. Addition of Sorafenib versus placebo to standard therapy in patients aged 60 years or younger with newly diagnosed acute myeloid leukaemia (SORAML): A multicentre, phase 2, randomised controlled trial[J]. Lancet Oncol, 2015, 16(16): 1691-1699.
1b。
• 目前急性髓系白血病(acute myeloid leukemia, AML)的标准治疗方案是阿糖胞苷联合蒽环类或者蒽醌类药物, 然而即使在年龄小于60岁的年轻AML患者其长期生存率也仅约为50%。
• 索拉非尼(Sorafenib)是一种多激酶抑制剂, 可以阻断与AML发生、进展相关的多个信号途径, 如RAS/RAF、c-KIT、VEGF受体、PDGF受体和FLT3。临床前资料和临床试验的结果均表明索拉非尼是很有前景的AML治疗药物, 目前已有30余篇报道, 但多是一些病例报告、少数早期或非随机的临床研究报告。
• 白血病研究联盟2013年报道了一项随机临床试验的结果[1], 该临床试验旨在评价标准化疗联合索拉非尼治疗60岁以上新诊断的老年AML患者, 对照组为标准化疗组。结果显示, 索拉非尼联合标准强烈化疗方案治疗该年龄段的AML患者并未增强抗白血病作用, 反而增加了并发症。
• 年轻和老年AML患者的基因突变特点、治疗反应和预后等存在差异, 年轻患者对药物的耐受性可能要好于老年患者。
探讨索拉非尼联合标准化疗方案对初治、≤ 60岁AML患者的疗效和耐受性。
• 研究条件:白血病研究联盟设计的SORAML研究, 德国的25个中心参加。
• 研究方法:随机、双盲、安慰剂对照, Ⅱ 期临床试验。
• 研究时间:2009年3月27日至2011年11月28日。
• 研究对象:年龄18~60岁、符合WHO诊断标准的新诊断原发或继发性AML。入组标准为临床体力状态评分0~2分、肝肾功能正常。排除标准为:急性早幼粒细胞白血病, 临床相关的心脏病(纽约心脏协会分级Ⅲ ~Ⅳ 级), 不稳定型心绞痛, 心律失常, 未能控制的高血压, 新近的创伤及大手术, 或者最新用过羟基脲治疗超过5天的AML。
• 干预措施: 患者随机分组后分别接受索拉非尼联合标准DA [柔红霉素(DNR) 联合阿糖胞苷(Ara-C)]方案(试验组)或安慰剂对照联合DA方案(对照组)进行诱导治疗。DA方案:DNR 60 mg/(m2∙ d), d3~d5; Ara-C 100 mg/(m2∙ d), d1~d7。大剂量阿糖胞苷(HDAC)方案: DNR 3 g/m2, q12h, d1、 d3、d5。HAM方案为大剂量阿糖胞苷加米托蒽醌(10 mg/m2, d3~d5)。
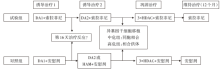
索拉非尼:400 mg, Bid用药, 第1~2疗程的10~19天, 巩固治疗的第8天开始(至下一疗程开始前3天)。维持治疗自最后1个疗程巩固后开始, 共12个月。治疗流程见图1。
• 评价指标:主要评价指标为无事件生存率(event-free survival, EFS); 次要评价指标为无复发生存率(relapse free survival, RFS)、总生存率(overall survival, OS)、完全缓解率( complete response, CR)和3级以上不良反应发生率。
共入组276例患者, 267例纳入分析(对照组133例, 试验组134例), FLT3-ITD阳性46例(占17%)、NPM1阳性86例(占32%)。对照组CR 59%(78例)、试验组CR 60%(81例)。试验组和对照组接受异基因干细胞移植的患者比例分别为31%和26%。中位随访36个月, 对照组中位无事件生存期 9个月[95%可信区间(convidence interval, CI)4~15个月]、试验组中位无事件生存期为21个月(95%CI 9~32个月)。试验组3年EFS、RFS较对照组高, 两组的3年OS差异无统计学意义, 见表1。
| 表1 两组的疗效评价 |
FLT3-ITD阳性患者46例(每组23例):中位无事件生存期试验组为5个月、对照组为6个月, 无差异; 中位无复发生存期分别为18个月和6个月, 总生存期分别为NR(未达)和19 个月, 试验组均优于对照组, 但差异无统计学意义。除外FLT3-ITD阳性患者后, 试验组的EFS、RFS显著优于对照组。
试验组3级及以上的不良反应明显多于对照组, 相对危险度分别为发热1.54(95%CI 1.04~2.28)、恶心7.89(95%CI 2.94~25.2)、出血3.75(95%CI 1.5~10.0)、心脏事件3.46(95%CI 1.15~11.8)、手足皮肤反应和皮疹4.06(95%CI 1.25~15.7)。
60岁以下的AML患者予标准化疗加用索拉非尼可以增强抗白血病作用, 但是毒副作用增加。尚需更长的随访时间比较总生存的差异, 需要探讨减轻索拉非尼毒副作用的AML治疗方案。
| 表2 部分AML临床研究结果 |
AML是成人最常见的急性白血病, 是一组遗传学背景各异的髓系肿瘤, 白血病克隆具有演化的潜能。AML的疗效受多种因素影响, 如年龄、并发症、体能状态、疾病的生物学特征, 其中最重要的还是遗传学特点。根据遗传学(包括细胞遗传学和分子学)特点的异质性可以将AML分为不同的预后危险组, 不同的危险组采用不同的治疗策略; 目前关于AML治疗方案的探讨离不开遗传学的分组分析。随着二代测序技术(next generation sequencing, NGS)应用的普及, AML基因表达谱的特点及意义研究越来越凸显出重要性。NGS可以在相对短的时间内同时检测多种基因突变和突变类型, 从研究的角度讲其临床意义无法估量, 在AML中确定了多种以前预后意义未知的基因, 如IDH1/2、DNMT3A等。AML分子学异常大致可分为以下几类:(1) Ⅰ 类, 与信号转导有关, 如FLT3、KIT、JAK2、PTPN11等。(2)Ⅱ 类, 与细胞分化有关, 如RUNX、CBFβ 、NPM1、MLL、RARA等。(3)Ⅲ 类, 与表观遗传学调控有关, 如TET2、IDH/IDH2、DNMT3A、ASXL1、EZH2等。(4)其它, 与肿瘤抑制有关, 如WT1、TP53。另外, 还有一些基因异常高表达(如BAALC、EVI等)。因此, AML的发病机制十分复杂, 一个患者往往同时发生多种基因异常, 涉及多种信号通路[2, 3]。
非急性早幼粒细胞白血病患者的经典治疗方法仍然是以化疗为基础的治疗。目前, 国际上最通用的AML诱导缓解治疗方案(美国癌症综合网NCCN和欧洲白血病网ELN指南均作为首选推荐)仍然是蒽环类药物(主要是柔红霉素或去甲氧柔红霉素)联合阿糖胞苷(Ara-C), 即DA“ 3+7” 方案。阿糖胞苷常用剂量(标准剂量)一般为100~200 mg/(m2∙ d), 7天连续输注; 去甲氧柔红霉素(IDA) 12 mg/(m2∙ d)或DNR 60~90 mg/(m2∙ d)× 3天。完全缓解后的治疗主要是贯彻根据危险度分组(主要依据是细胞遗传学和分子学)的分层治疗理念, 预后良好组以化疗为主、预后中高危的患者首先推荐异基因干细胞移植; 主要的化疗方案是以中大剂量阿糖胞苷为基础的方案[4, 5, 6]。表2列举了近年国际上报道的AML临床研究的结果。从这些临床研究的结果可以看出, 再针对化疗药物的剂量、药物组合进行优化, AML化疗的效果也难以有更大的突破, 必须寻找新的药物、新的治疗理念。
遗传学研究(尤其是NGS的应用)的进展促成了“ 精准医学(precision medicine)” 概念的产生。精准医学的目标是根据患者的个体化特点实施个体化的治疗、在正确的时间选择正确的治疗方法, 即根据患者特异的基因突变和信号途径异常、体外药敏和耐药检测、高度敏感的微小残留病检测等给予针对性的医疗, 其中根据特殊靶标的靶向治疗是重要的一方面[3]。FLT3是一种受体酪氨酸激酶, 在AML中常常发生突变, 文献报道的突变率为15%~30%。FLT3突变最常见的有两种:近膜区的内部串联重复(ITD)和酪氨酸激酶区的点突变(TKD)。目前FLT3-ITD突变已明确被NCCN、ELN作为预后危险度分组的重要分子标志; 而针对FLT3-ITD突变的靶向治疗也陆续有报道。NCCN自2015年开始在难治/复发AML的挽救治疗中将去甲基化药物+索拉非尼作为FLT3-ITD阳性患者的挽救治疗方案。
本研究是一项随机、双盲、安慰剂对照的多中心Ⅱ 期临床试验, 是在前期临床试验的基础上开展的。研究对象为60岁及以下的初诊AML, 治疗方案是在标准DA“ 3+7” 方案[DNR 60 mg/(m2∙ d)]的基础上联合索拉非尼或安慰剂, 完成巩固治疗后又给予了12个月的维持治疗。两组的CR分别为60%和59%, 低于前期的文献报道; 但是生存率和其它临床研究相似。研究中也发现和索拉非尼相关的毒副反应明显增加, 降低了患者对治疗的耐受性, 可能会影响试验组的疗效。和想象有一定出入的是FLT3-ITD阳性AML患者的疗效, 索拉非尼的应用没有改善EFS(而没有FLT3-ITD突变患者的EFS、RFS均明显提高), 但是改善了RFS和OS。
和索拉非尼在老年AML中的结果不尽一致, 本研究中60岁以下的AML患者采用标准化疗加用索拉非尼增强了抗白血病作用, 但是毒副作用同样增加。因此, 在年轻AML患者同样需要探讨减轻索拉非尼毒副作用的AML治疗方案。另外, 研究结果也提示, 作为一个多种激酶的抑制剂, 哪些AML患者(涉及RAS/RAF、c-KIT、VEGF受体、PDGF受体和FLT3中的哪个基因)更有可能从索拉非尼的用药中获益十分重要, 可以更好地做到治疗精准化。另外, 出现FLT3-ITD突变这种高危分子学异常的患者, 尽管可以试用靶向药物, 但目前阶段提高疗效的根本措施依然是异基因干细胞移植。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|