编者按: 疾病的正确诊断和合理治疗是患者和医务工作者共同的心愿。在广东省人民医院肿瘤中心, 吴一龙教授指导临床医生应用循证医学理论进行肿瘤的多学科综合治疗, 开展临床病例讨论。讨论会上各学科共同围绕一个病例或一个病种进行会诊, 临床、病理、B超、放射影像等资料齐全, 除相关科室提前准备的中心性发言外, 到会人员各抒己见, 气氛热烈。参会人员受益匪浅, 提高了对疑难病例的诊治水平。为了将他们的诊治经验传播出去, 让更多的临床医生获益, 我刊开辟“循证病例讨论”栏目, 希望广大医务工作者关注此栏目。
患者男性, 68岁, 因“ 反复右肩不适3个月” 于2016-07-18入院。患者3个月前无明显诱因出现右肩不适, 1个月前自觉右肩包块, 不伴肢体疼痛、乏力, 于当地医院就诊, 查甲胎蛋白(alpha fetal protein, AFP)> 3 000 ng/mL, 上腹MRI示肝左外叶下段团块状病变, 考虑肝癌可能。右肩胛CT示右侧肩胛骨下角骨质破坏伴较大软组织肿块影, 考虑转移瘤可能。患者一般情况良好, 2016-07-19入院后做进一步的检查。AFP > 54 000 ng/mL; HBV-DNA 1 867.12 IU/mL; PET-CT示肝S3异常强化灶, 考虑肝左叶恶性病变; 右侧肩胛骨软组织肿块, 考虑转移性病变。请介入科、骨科、肝胆外科、感染科会诊, 会诊意见:先行右肩胛骨病灶穿刺活检, 如果是两个独立的肿瘤, 可以分别行外科切除; 如果是肝癌伴肩胛骨转移, 肝内病灶不考虑手术切除。
2016-07-28病理诊断为肩胛骨病灶支持转移性肝细胞癌。最后诊断:肝细胞癌并右肩胛骨转移(BCLC C期 Child-pugh A级)。再次进行多学科会诊, 肝胆外科考虑肝癌已经有肝外转移, 肝内病灶不建议手术切除, 可选择局部消融治疗; 骨科建议右肩胛肿块行手术切除, 但患者不同意手术。2016-07-28在CT引导下行经皮穿刺左肝病灶微波消融术, 术后第4天行右侧上肢动脉造影术+右旋肩胛动脉栓塞术。
2016-08-29(术后1个月)第二次入院复查, AFP 2 807.24 ng/mL, 较前明显下降; HBV-DNA定量< 500 IU/mL。增强CT示肝S3病灶未见异常强化, 疗效评价为完全缓解; 右肩胛骨病灶呈碘化油栓塞术后改变, 病灶较前缩小, 疗效评价为疾病稳定。
2016-08-30行经皮穿刺右肩胛骨病灶微波消融术。
2016-10-08(首次治疗后67天)第三次入院复查, AFP 4 359 ng/mL, 较前略有升高。PET-CT示肝内病灶未见复发; 右侧肩胛骨转移灶较前缩小, 仍见部分病灶葡萄糖代谢增高。
患者现精神、胃纳可, 大小便正常。
既往史:“ 乙肝小三阳” 病史10余年, 有慢性阻塞性肺病史, 长期予舒利迭治疗。2014-06-24行“ 左侧输尿管结石取石术” 。无肿瘤病史; 无饮酒史; 无过敏史; 无输血及血制品史。
个人史、家族史等无特殊。
体格检查:T36.5℃, P76次/分, R19次/分, BP122/68 mmHg。神志清, 坐位, 全身浅表淋巴结未触及。呼吸平顺, 双肺呼吸音稍粗, 可闻及少量干性啰音。心律齐, 各瓣膜听诊区未闻及病理性杂音。腹平软, 无压痛反跳痛。肝脾肋下未触及, 肠鸣音4次/分。双下肢未见浮肿。双侧足背动脉搏动可。肌力、肌张力正常, 生理反射存在, 病理反射未引出。右肩胛骨下角可触及质硬包块, 大小约9 cm× 10 cm, 无压痛。
辅助检查:
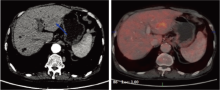
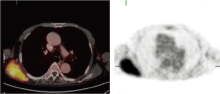
2016-07-20 PET-CT提示肝S3异常强化灶, 局部葡萄糖代谢增高, 考虑肝左叶恶性病变, 见图1; 右侧肩胛骨骨质破坏, 局部葡萄糖代谢增高, 考虑转移性病变, 见图2。
2016-08-29肩关节增强CT提示右侧肩关节结构关系正常, 右后侧胸壁肩胛冈下缘见团块状肿块影, 边界不清, 弥漫点状高密度结节。增强扫描不均匀强化, 右侧肩胛骨下角骨质破坏。
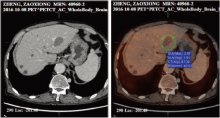
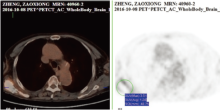
2016-10-08 PET-CT提示肝内病灶未见复发, 见图3; 右侧肩胛骨转移灶葡萄糖代谢稍增高(范围约8.2 cm× 3.1 cm; SUVmax:5.5), 与前片比较糖代谢减低, 肩胛骨肿物有所缩小, 见图4。
萧炜亮(介入治疗科医师):汇报病史特点(略)。提出讨论要点:(1)肝癌伴肩胛骨转移的相关问题; (2)对既往治疗经过的回顾性评价; (3)进一步诊疗方案:手术?放疗?靶向治疗?
陈晓明(介入治疗科主任医师):众所周知, 肝癌骨转移比较常见, 但以椎体转移最多见, 再者为骨盆、长骨, 肩胛骨转移非常罕见, 针对肝癌肩胛骨转移的相关报道比较少, 在此我们先进行肝癌肩胛骨转移的文献复习。
王一焯(介入治疗科医师): 复习相关文献我们知道, 肝外转移途径中血行转移最常见(84.6%), 其次为淋巴转移(35%), 腹膜种植性转移较少见(18.6%), 骨转移主要通过血行转移实现。肝癌骨转移最常见部位依次为:脊柱、骨盆、肋骨。肝癌肩胛骨转移的病例报道仅检索到3例, 最早的报道是在1986年。总结相关病例特点发现, 肝癌肩胛骨转移发病年龄多为中老年男性, 有病毒性肝炎病史、酗酒等肝癌高危发生因素, 3例均因肩部不适而就诊; 实验室检查AFP升高1例, 其余2例未描述, 本例AFP明显升高; 影像学检查肝内病灶2例为多发病灶, 1例未描述, 本例为肝内单发小病灶; 肩胛骨转移灶2例最大直径均> 7 cm, 呈溶骨性改变, 1例未描述, 本例肩胛骨转移灶直径为8 cm。治疗与转归方面, 3例患者均接受姑息治疗, 其中1例随访1个月去世, 另2例未描述, 本例患者继续随访中。
周雨(肝胆外科博士):对于肝癌肩胛骨转移的文献报道比较少, 且分析报道的肝癌骨转移病例一般都是肝癌孤立性骨转移、或者以骨转移为首发症状的病例。对于孤立转移灶的病例报道, 肩胛骨转移的文献只有3篇, 其他骨转移更多是重要或功能部位的转移, 比如颌骨和颧骨转移, 这些部位的转移会影响患者进食、吞咽、呼吸等功能并引起疼痛。关于治疗策略, 手术治疗超过一半(57%), 手术治疗目的主要是缓解症状、改善功能, 生存时间从1~6个月不等。
陈晓明:回顾之前的治疗过程, 对于肝内病灶, 我们选择局部消融治疗, 术后复查证实肝内病灶疗效为完全缓解, 那么肝内病灶应该进行外科手术切除还是其他治疗方法更能使患者获益?
金浩生(肝胆外科副主任医师):肝内的病灶, 根据2011年卫生计生委肝癌诊疗规范, 肝内病灶大小约3 cm, 在不考虑手术切除的情况下, 可首选局部消融, 比如射频消融, 所以行消融治疗符合指南的原则。事实上, 该例患者肝病灶消融后疗效达到完全缓解, 也证明我们的治疗选择是正确的。肝癌切除一定要做根治性切除, 不做姑息性切除, 但患者是一个整体, 患者已出现转移灶, 应该从全身考虑, 以局部治疗为主, 同时加索拉非尼进行全身治疗。
旁述:实体肿瘤疗效评价标准(RECIST 1.1版):
完全缓解(CR):所有靶病灶消失; 病理性淋巴结短径< 10 mm;
部分缓解(PR):靶病灶长径总和缩小至少30%;
疾病稳定(SD):靶病灶长径总和有缩小但未达部分缓解或有增加但未达疾病进展;
疾病进展(PD):靶病灶长径总和增加20%以上, 并且其绝对值增加超过5 mm, 或出现新病灶。
卫生部肝癌诊疗规范(2011年)
……
局部治疗
局部消融治疗是借助医学影像技术的引导对肿瘤靶向定位, 局部采用物理或化学的方法直接杀灭肿瘤组织的一类治疗手段。主要包括射频消融(RFA)、微波消融(MwA)、冷冻治疗(Cryoablation)、高功率超声聚焦消融(HIFU)以及无水乙醇注射治疗(PEI), 具有微创、安全、简便和易于多次施行的特点。
……
局部消融治疗的适应证:通常适用于单发肿瘤, 最大径≤ 5 cm; 或肿瘤数目≤ 3个, 且最大直径≤ 3 cm; 无血管、胆管和邻近器官侵犯以及远处转移。肝功能分级为Child-Pugh A或B级, 或经内科护肝治疗达到该标准。有时, 对于不能手术切除的直径> 5 cm的单发肿瘤, 或最大直径> 3 cm的多发肿瘤, 局部消融可以作为姑息性综合治疗的一部分, 但是需要严格掌握。
因此该病例虽然伴远处转移, 但肝内病灶较小, 且只有右侧肩胛骨孤立转移灶, 在不考虑手术切除的前提下, 肝内病灶进行微波消融符合肝癌诊疗规范局部消融治疗原则。
陈晓明:关于肝外转移灶, 骨科当时建议首选手术切除, 请问选择手术切除的依据是什么?切除的时机和需要具备的条件是怎样的?
马元琛(骨科副主任医师):通常肝癌骨转移手术难度较大, 容易出血, 且出血量大, 手术彻底切除非常困难, 且肝癌骨转移手术切除患者生存率较低。但该病例有其特殊之处, 第一, 该患者经穿刺病理活检提示转移性肝细胞癌, 诊断明确, 肝内原发病灶小, 容易控制; 第二, 右侧肩胛骨转移灶大小约8.7 cm× 5.2 cm, 位于背侧, 影响肢体活动, 肩胛骨属于游离的骨头, 与肩关节和肩锁关节无相连, 且肿物位于肩胛骨最尾端, 未浸润皮肤和胸壁, 周围无重要的血管、神经及肌肉等, 肿物主要以旋肩胛动脉供血, 可术前行肿瘤血管栓塞, 术中控制出血较容易; 第三, 肩胛骨完整切除对患者的机体功能影响较小。因此在原发灶控制的前提下, 没有其他大的骨转移灶, 可以同期或者第二期完整切除肩胛骨转移灶, 就目前来说, 如果患者愿意手术切除转移灶, 仍然可以进行手术切除。
陈晓明:近年来, 肝癌NCCN指南中增加了不少关于肝癌放疗的内容, 该患者肩胛骨转移灶是否适合放疗?
谢松喜(放疗科副主任医师):肩胛骨放疗可以作为一种姑息性治疗。有文献报道200多例肝癌孤立骨转移进行外照射的预后分析, 转移灶给予放疗, 放疗剂量50 Gy以上, 完全缓解率达到46.7%, 部分缓解率达53.3%, 剂量高低并不影响患者预后, 肝内病灶控制良好患者的预后比肝病灶控制不佳患者的预后好, 中位生存期7.4个月。还有文献报道, 经过放疗后, 疼痛缓解率在72.7%~99.5%, 生存期为5~7.4个月。总之, 肝癌骨转移行外照射可以缩小肿瘤, 缓解疼痛症状, 且剂量越高, 完全缓解率也越高, 但放疗剂量的高低不影响生存率。
潘燚(放疗科副主任医师):患者一般情况良好, 预后较好, 但对于8 cm的肩胛骨转移灶, 经放疗达到完全缓解比较困难, 可能是部分缓解。相对于肩胛骨切除, 放疗创伤会更小, 且进行调强治疗不会出现放射性肺损伤。
吴一龙(肿瘤学教授):该病例为肝癌伴孤立肩胛骨转移, 其实是一个肿瘤寡转移病例, 原发病灶经局部治疗后获得很好的疗效。那么我们如何认识这种寡转移的全身治疗?应不应该进行靶向治疗?
金浩生:该病例的特点主要是肝癌孤立性骨转移, 原发灶较小, 不同于大部分肝癌晚期患者伴发外周转移。根据BCLC分期、欧洲肝脏病协会、NCCN指南, 该病例均属于肝癌晚期, 指南推荐索拉非尼及最佳对症支持治疗。我国学者曾报道了1例索拉非尼治疗肝癌伴椎骨转移的病例, 按指南给予索拉非尼 200 mg bid治疗, AFP由22 000 ng/mL迅速下降并一直保持在正常水平, 获得长达5年的无进展生存期。虽然单个病例报道不能够作为较高质量的循证医学证据来指导临床治疗, 但结合临床指南和该病例报道, 靶向治疗应该是本例患者较好的一个治疗选择。
马冬(肿瘤内科主任医师):无论手术还是放疗, 该患者病灶小, 侵犯部位少, 一般状况好, 局部治疗确实能够获得很好的疗效, 但该患者有肝外转移, 属于BCLC C期, 要取得最大获益应该加上全身治疗。该病例介入治疗后AFP有明显下降, 但仍较高, 复查PET-CT提示右肩胛骨有残余活癌, 如果肩胛骨病灶不考虑手术切除, 选择放疗, 则应该同时口服索拉非尼, 提高治疗效果; 如果选择手术切除, 术后AFP仍高, 也应该加上索拉非尼进行全身治疗。
旁述:根据巴塞罗那肝癌临床分期, 本例患者PS评分=1, 肝功能为Child-pugh A-B级, 伴远处转移, 肝癌分期为BCLC C期, 推荐口服索拉非尼全身治疗。
吴一龙:总结今天的病例讨论, 大家应该重视肿瘤寡转移的治疗。寡转移是最近两三年临床肿瘤学提出来的一个重要话题, 首先提出来的是前列腺癌, 临床观察发现部分前列腺癌只转移到某个特定器官或组织, 第二是乳腺癌, 第三是肺癌。对此临床肿瘤学给了很多解释, 100多年前乳腺癌鼻祖Halsted发展了乳腺癌扩大根治术, 主要根据是肿瘤转移从局部、淋巴管、血管, 最后转移至全身, 因此局部治疗显得格外重要。后来到上个世纪50年代, 学者们发现很早期乳腺癌也发生全身转移, 并提出乳腺癌是一种全身性疾病, 局部治疗地位逐渐降低, 更重视全身治疗, 在该理论指导下乳腺癌治疗越来越精细; 上世纪90年代, 另一理论出来, 发现肿瘤细胞是由不同的克隆组成, 不同的克隆有其特殊的转移潜能, 即“ 光谱学说” , 每个克隆就像一束光谱, 这一理论认为肿瘤治疗应局部治疗和全身治疗并重, 且取决于对每一个克隆的认识, 并提出寡转移概念。根据这种光谱学说, 局部治疗非常重要, 在原发灶控制的前提下, 应对转移灶进行最佳局部治疗, 前列腺癌和乳腺癌取得非常大的成功。回归本病例, 本病例非常符合寡转移的情况, 原发病灶控制良好, 只有一个孤立转移灶, 局部治疗非常重要, 局部治疗应该选手术切除还是放疗, 就应该由骨科和放疗科从治疗彻底性、安全性、并发症、术后长期影响等方面进行对比, 通过讨论, 我们认为相比于放疗, 手术切除应该是一个更好的选择。对于该患者的靶向治疗, 则应该从靶向治疗的有效性、患者经济状况及我国肝癌人群特点等方面进行综合评估。
The authors have declared that no competing interests exist.