作者简介: 廖金瑶(1984-),男,广东五华人,医学学士,从事感染性疾病的研究工作。
目的 探究使用恩替卡韦治疗96周后序贯聚乙二醇干扰素α-2a对慢性乙型肝炎的治疗中基线Anti-HBc在HBeAg血清学转换的预测作用。方法 纳入103例经恩替卡韦单药治疗的慢性乙型肝炎患者并将其随机分为对照组和试验组,其中试验组56例,在恩替卡韦治疗基础上序贯聚乙二醇干扰素α-2a,12周后改为单药使用聚乙二醇干扰素α-2a;对照组47例,持续接受单药恩替卡韦治疗。每12周进行血常规、甲状腺功能、肝功能检测;采用电化学发光法检测HBsAg、Anti-HBs、HBeAg、Anti-HBe含量,ELISA检测Anti-HBc,荧光定量PCR法检测HBV DNA含量,并比较治疗48周后两组HBeAg血清转换率和HBsAg消失率。结果 治疗12周,对照组HBsAg的中位数值相对稳定,试验组呈下降趋势;治疗48周,试验组较对照组HBeAg血清转换率和HBsAg消失率皆有所提高。结论 结合基线Anti-HBc定量和HBsAg可作为预测疗效的指标,观察远期疗效。
: Objective To investigate the performance of baseline Anti-HBc as a predictor for HBeAg seroconversion in chronic hepatitis B(CHB) patients treated with Peginterferon Interferons α-2a (Peg-IFNα-2a) sequentially after Entecavir (ETV) treatment for 96 weeks. Method 103 CHB cases treated with ETV singly were included into this study and divided into control group and experimental group randomly. Among those, 56 cases in experimental group received sequential treatment of Peg-IFNα-2a on the basis treatment of ETV for 12 weeks, then treated with Peg-IFNα-2a alone; 47 cases in control group treated with ETV alone continuously. For all patients, examination of blood routine, thyroid and liver functions were performed every 12 weeks; meanwhile, the levels of HBsAg, Anti-HBs, HBeAg and Anti-HBe were detected by electrochemiluminescence assay, the level of Anti-HBc was detected by ELISA, the level of HBV DNA was detected by fluorescent quantitative PCR; and the HBeAg seroconversion rate and HBsAg disappearance rate of CHB were compared between the two groups after 48 weeks treatment. Results After treatment for 12 weeks, the median of HBsAg level in the control group was relatively stable, and decreased in experimental group. After treatment for 48 weeks, compared with the control group, the rates of HBeAg seroconversion and HBsAg disappearance in the experimental group both increased. Conclusion Baseline Anti-HBc for fixed quantity of HBsAg can be used as an index for predicting the curative effect, and observe the long term efficacy.
随着核苷(酸)类药物[nucleos (t) ide analogues, NAs]的广泛应用, 临床出现众多的NAs经治慢性乙型肝炎(chronic hepatitis B, CHB)患者, 这类患者的后续治疗方案已成为临床研究热点。2015年《中国慢性乙型肝炎防治指南》对CHB的抗病毒联合治疗的建议是使用NAs降低病毒载量后联合或序贯聚乙二醇干扰素(Peginterferon Interferons, Peg-IFN)α 的方案, 较NAs单药在HBeAg下降方面有一定的优势[1]。临床医生也一直在探索提高NAs治疗CHB患者的HBeAg血清转换率的方案及预测指标。本研究评估了长期使用恩替卡韦(Entecavir, ETV)治疗的HBeAg阳性CHB患者序贯Peg-IFNα -2a治疗的疗效, 同时分析基线Anti-HBc及HBsAg在治疗应答中的预测作用。
收集2012年7月至2014年3月广东省人民医院感染科收治的HBeAg阳性CHB患者。病例纳入标准:(1)年龄18~60岁, HBsAg阳性6个月以上, 符合CHB诊断标准[2]; (2)均经ETV单药初始治疗, 且治疗96周后达HBV DNA< 100 IU/mL, 0.227 PEIU/mL< HBeAg≤ 50 PEIU/mL。病例排除标准:(1)同时感染除CHB外其它类型肝炎病毒或人类免疫缺陷病毒; (2)合并其它肝脏疾病患者, 如肝癌、肝硬化、代谢性肝病等; (3)妊娠期或哺乳期患者; (4)酗酒、吸毒或癫痫患者; (5)伴有其它严重疾病, 如严重心血管疾病、肺部疾病、肾脏疾病、消化系统疾病、恶性肿瘤、精神疾病、代谢疾病等; (6)治疗前血常规检查结果提示中性粒细胞数量少于1.0× 109/L或血小板数量少于50.0× 109/L。本研究经医院伦理委员会批准, 所有入选患者均签署知情同意书。
接受ETV治疗96周后达HBV DNA< 100 IU/mL, 0.227 PEIU/mL< HBeAg≤ 50 PEIU/mL的CHB患者随机分为试验组和对照组, 试验组接受ETV序贯Peg-IFNα -2a 12周后改为Peg-IFNα -2a单药治疗, 对照组持续接受ETV单药治疗。Peg-IFNα -2a 180 μ g, 1次/周, 皮下注射, 上海罗氏制药有限公司; ETV 0.5 mg, 1次/d, 口服, 中美上海施贵宝制药有限公司。
研究开始前的检查评估项目包括询问病史、常规体检、血常规、血清生物化学、血清HBV标志物、HBV DNA定量、育龄妇女妊娠检查。研究开始后每12周进行检测, 内容包括血常规、甲状腺功能和肝功能检测[谷丙转氨酶(alanine transaminase, ALT)和谷草转氨酶(aspartat aminotransferase, AST)]。HBsAg定量、Anti-HBs定量、HBeAg半定量、Anti-HBe半定量采用MOUDULAR E170系统电化学发光法检测, ElecsysⅡ 检测系统及配套试剂盒购自上海罗氏公司, HBsAg定量下限0.05 IU/mL, HBeAg半定量下限0.227 PEIU/mL。Anti-HBc定量采用双抗原夹心法酶联免疫吸附法, 试剂购自北京万泰生物药业股份有限公司。HBV DNA定量采用荧光定量PCR法检测, 检测下限为100 IU/mL, 试剂购自中山大学达安基因公司。
主要疗效指标:治疗48周时HBeAg血清转换率和HBsAg消失率(HBeAg血清学转换:既往HBeAg阳性的患者HBeAg阴转、出现Anti-HBe。HBsAg消失:既往HBsAg阳性的患者HBsAg阴转)。Anti-HBc定量在HBeAg血清转换的预测作用。次要疗效指标:治疗期间HBsAg变化趋势。
使用SPSS 19.0统计学软件对数据进行处理。计数资料以百分比(%)表示, 组间比较采用卡方(χ 2)检验, 计量资料以平均值 ± 标准差(\(\bar{x}\)± s)表示, 组间比较采用t检验。P≤ 0.05表示差异有统计学意义。
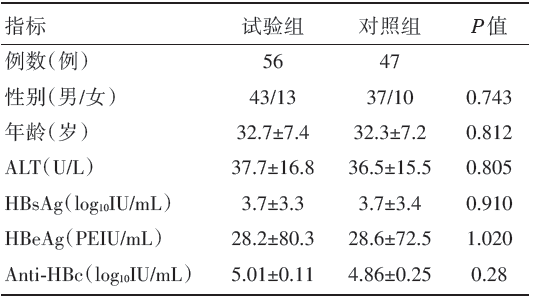
共收集经ETV单药初始治疗96周的HBeAg阳性患者180例, 剔除HBV DNA≥ 100 IU/mL患者3例, 74例因HBV DNA< 100 IU/mL但 HBeAg > 50 PEIU/mL而继续ETV单药治疗, 有103例患者达到HBV DNA< 100 IU/mL且0.227 PEIU/mL< HBeAg≤ 50 PEIU/mL纳入研究。将103例患者随机分为试验组和对照组, 其中试验组56例, 男性43例, 女性13例, 年龄19~49岁; 对照组47例, 男性37例, 女性10例, 年龄21~47岁。两组患者的基线特征见表1。
| 表1 两组患者的基线特征 |
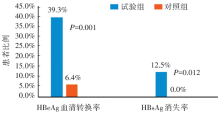
治疗48周, 试验组HBeAg血清学转换率为39.3%(22/56)高于对照组的6.4%(3/47), 差异有统计学意义(P=0.001); 试验组HBsAg消失率为12.5%(7/56)高于对照组的0%(0/47), 差异有统计学意义(P=0.012), 见图1。
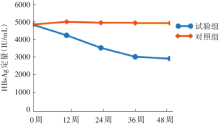
试验组治疗期间HBsAg中位数呈下降趋势, 对照组变化不明显。在36周和48周时试验组HBsAg中位数明显低于对照组, 差异有统计学意义(P=0.049和P=0.025), 见图2。
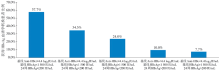
将基线Anti-HBc、HBsAg定量, 结合治疗24周HBsAg定量的cut off值, 分成不同组合模式分析CHB患者治疗48周时HBeAg血清学转换率。基线Anti-HBc≥ 4.4 log10IU/mL + 基线HBsAg < 1 500 IU/mL+24周HBsAg≤ 200 IU/mL的患者治疗48周HBeAg血清学转换率高达57.7%; 而基线Anti-HBc < 4.4 log10IU/mL + 基线HBsAg≥ 1 500 IU/mL+24周HBsAg > 200 IU/mL患者治疗48周HBeAg血清学转换率仅7.7%, 见图3。
治疗过程中, 两组103例患者无1例退出。共22例出现不良反应, 均为试验组患者。其中包括一过性发热16例, 疲乏12例, 头痛3例, 肌肉痛3例, 脱发9例, 皮疹2例; 1例患者出现甲状腺功能异常, 通过密切检测完成治疗; 无抑郁症; 5例患者有一过性ALT升高、中性粒细胞减少和血小板减少, 通过调整剂量完成治疗; 未发生肝功能失代偿情况。不良反应由α 干扰素治疗导致, 均在预期内。
CHB在我国流行范围广、发病率高, 我国现有的慢性乙型肝炎病毒(hepatitis B virus, HBV)感染者约9 300万人, 其中CHB患者约2 000万例, 每年因HBV导致的肝硬化和肝癌死亡约30余万例, 新发乙型肝炎病例约50~100万例[3, 4]。CHB治疗时间长且易反复, 对感染者身心健康影响很大, 严重的会危及患者生命安全。CHB的治疗在我国受到广泛重视, 历经十多年的探索和发展, 临床医师和研究人员逐步认识到, CHB的抗病毒治疗过程不仅仅是对病毒复制的抑制, 而应更深入地从发病机制上来认识和治疗[5]。CHB为免疫介导疾病, 因此如何找到一种治疗方法充分调动机体免疫系统、清除HBV是治疗的关键[6]。2012年, 欧洲肝脏研究学会指南强调停药后持久应答是CHB满意的治疗终点, 即指停药后持久的病毒学应答、HBeAg血清学转换和生物化学应答[7]。
CHB的抗病毒治疗, NAs长期治疗面临耐药风险, 且获得血清学转换几率低, 干扰素有助于减少长期NAs治疗的耐药发生几率, 增加血清学转换机会[8]; NAs维持期治疗可强效抑制病毒血症, 避免HBVcccDNA回补[9]; 有效恢复CD8+T细胞功能[10], 为再次启动干扰素治疗提供条件。因此, 在本研究中我们对ETV经治96周的CHB患者序贯Peg-IFNα -2a治疗, 并观察其治疗应答和疗效。
HBsAg和HBeAg分别为乙肝病毒的外壳蛋白和核心颗粒蛋白, 其中HBsAg是判断HBV感染的敏感和特异性指标, HBeAg是人体感染HBV后跟随HBsAg出现的第二个血清学抗原标志物, 两者在临床诊断和流行病学调查中广泛应用。本研究中我们发现, 在序贯Peg-IFNα -2a治疗ETV经治96周未获得HBeAg血清学转换的HBeAg阳性CHB患者中, 试验组治疗48周的HBsAg消失率为12.5%, 高于对照组的0.0%, 差异有统计学意义(P< 0.05); 试验组治疗48周的HBeAg血清学转换率为39.3%, 显著高于对照组的6.4%, 差异有统计学意义(P< 0.05)。以上结果表明序贯Peg-IFNα -2a治疗ETV经治的CHB可以提高HBeAg血清学转换率和HBsAg消失率, 这也与国内外多项研究结果趋势一致[11, 12, 13, 14, 15, 16, 17, 18, 19]。例如, 国内Li等[11]曾有研究发现CHB患者使用ETV序贯Peg-IFNα -2a治疗48周后, 联合组患者HBeAg血清学转换率为44%, 高于持续使用ETV治疗患者6%的转换率。李爱新等[12]的一项回顾性研究结果显示, 采用ETV序贯Peg-IFNα -2a治疗CHB时, 患者HBsAg清除率为24%, HBeAg血清学转换率为16%; 2016年任成俭等[13]的研究也发现:对于HBeAg阳性CHB患者, 联合Peg-IFNα -2a和ETV长期治疗可明显提高CHB患者HBeAg和HBsAg血清学转换率; 国外Boglione等[14]的一项队列研究结果也同样表明, ETV组合Peg-IFNα -2a治疗组HBeAg血清学转换率和HBsAg损失分别为68.2%和33.3%, 明显高于单独用药组; 此外, 有研究还发现ETV联合Peg-IFNα -2a治疗还能降低肝纤维化, 缓解肝炎病症, 改善肝功能[15, 16]。
同时, 在研究过程中, 我们还观察到试验组患者治疗过程中HBsAg水平持续下降, 特别是HBeAg达血清学转换者HBsAg下降幅度更高, 至36周和48周时HBeAg达血清学转换者HBsAg下降幅度与HBeAg未达血清学转换者比较, 差异有统计学意义(P< 0.05); 而对照组整个治疗过程中HBsAg变化不明显。治疗进行到36周时, 试验组与对照组HBsAg水平比较差异有统计学意义(P< 0.05), 提示Peg-IFNα -2a序贯治疗方法的HBsAg清除能力更强, 疗效更好。先前的研究中, 肖作汉等[20]曾发现治疗24周后, 当CHB患者HBsAg水平< 1 500 IU/mL, 下降幅度≥ 1 lgIU/mL, 其持续病毒学应答率会明显升高; 赵翀[21]在研究HBsAg水平检测意义时提到, Peg-IFN治疗CHB过程中, HBsAg≤ 1 500 IU/mL组患者在24周和48周时病毒学完全应答率明显高于HBsAg> 1 500 IU/mL组; He等[22]研究发现, Peg-IFNα -2a联合ETV治疗CHB第48周时的HBeAg血清转化率高于ETV单独使用的CHB患者, 同时在Peg-IFNα -2a组中, 基线HBsAg水平< 1 500 IU/mL患者的HBeAg血清转换率和HBsAg损失率高于HBsAg水平≥ 1 500 IU/mL(HBeAg血清学转换:62.5% vs. 17.86%, P=0.007; HBsAg损失率:41.67%vs. 6.25%, P=0.016); 日本一项研究表明, 23例长期接受ETV治疗的CHB患者接受Peg-IFNα -2a治疗72周后, HBeAg血清转化率为25%, HBsAg水平明显降低, 研究者认为, HBeAg阴性和基线HBsAg水平< 2 000 IU/mL的患者临床适应证最佳[23]。本研究的结果表明, 与单独用药相比较, 联合使用Peg-IFNα -2a治疗CHB将大大提高HBsAg清除率和治疗效果, 且治疗时间越长, HBsAg水平降低越明显, 同样提示基线HBsAg水平与药物治疗应答联系密切。即ETV联合Peg-IFNα -2a治疗CHB过程中, HBsAg下降是Peg-IFNα -2a治疗应答最重要的预测因素, 基线HBsAg水平与药物治疗应答有关。
此外, Anti-HBc是HBV感染后的一个重要的血清病毒标志物。尹乃宁等[24]的研究显示, Anti-HBc滴度是HBV感染和复制的良好指标, 是HBsAg和HBV DNA检测的重要补充。2015年, Yuan等[25]报道Anti-HBc定量可用于预测慢性HBV感染者抗病毒治疗的疗效。Fan等[26]的研究提示Anti-HBc基线水平可作为HBeAg血清学转换的有效预测指标。国内外多个研究者在分析中将基线Anti-HBc定量的cut off 值定为4.4 log10IU/mL。基于患者基线特征及治疗中应答进行个体化治疗是提高Peg-IFNα 疗效的关键, 尤其对于NAs经治的CHB患者序贯Peg-IFNα 更需要探讨更多预测疗效的指标。本研究将基线Anti-HBc、HBsAg定量, 结合治疗24周HBsAg定量的cut off值, 分成不同组合模式分析CHB患者治疗48周HBeAg血清学转换率。结果提示基线Anti-HBc≥ 4.4 log10IU/mL和基线HBsAg< 1 500 IU/mL以及治疗24周时HBsAg< 200 IU/mL的CHB患者治疗48周HBeAg血清学转换率高达57.7%。因此基线Anti-HBc定量或可作为预测Peg-IFNα 治疗应答的新指标。
综上所述, 对于长期使用ETV治疗未获得HBeAg血清学转换的HBeAg阳性的CHB患者, 采用序贯Peg-IFNα -2a治疗, 根据基线Anti-HBc定量, 结合基线、治疗中HBsAg定量作为预测疗效的指标, 可用于优化CHB抗病毒治疗。以后研究需继续增加病例数进行观察同时加强长期随访, 观察远期疗效。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|