作者简介:周雨(1987-),男,山东淄博人,医学博士,从事肝胆胰恶性肿瘤的外科与综合治疗研究。
目的 系统评价治疗前外周血血小板水平作为胰腺癌患者预后指标的价值。方法 计算机检索PubMed、EMBASE、Cochrane图书馆、中国知网、万方、维普数据库,搜集有关血小板与胰腺癌患者预后的文章,由两位评价者独立进行文献检索、纳入排除、资料信息提取和质量评价,选择总生存作为主要指标,风险比作为预后效应量,采用 RevMan 5.3软件进行Meta分析。结果 最终纳入15篇文献,共计2 420例胰腺癌患者。Meta分析结果显示:血小板计数升高与胰腺癌患者总生存时间减少显著相关,合并所有报道的风险比为1.38(95%置信区间1.11~1.71,P=0.004)。合并11篇使用多因素回归方法计算风险比的文章,风险比为1.67(95%置信区间1.26~2.23, P=0.000 4),提示血小板计数升高是胰腺癌预后不良的独立风险因素。亚组分析显示,接受根治性手术的患者,血小板计数的预后价值高于姑息性治疗的患者,两者风险比分别为2.19(95%置信区间1.59~3.02,P<0.000 1)和1.63(95%置信区间1.12~2.36,P=0.01)。在无转移患者中血小板水平与预后显著相关(风险比1.61,95%置信区间1.18~2.20,P=0.003);而合并所有纳入了转移患者的研究显示血小板水平与预后无关(风险比1.15,95%置信区间0.75~1.76,P=0.51)。结论 治疗前外周血血小板计数升高是胰腺癌预后不良的风险因素,其在接受根治性手术切除的患者中作为预后指标的价值较高,在伴有转移的患者中预后价值较低。
Objective To clarify the role of platelet count in predicting the prognosis of pancreatic cancer patients through summarizing the current evidences by meta-analysis.MethodsThe PubMed, EMBASE, Cochrane library, CNKI, WANFANG, and VIP database were searched for studies investigating the relationship between platelet count and pancreatic cancer prognosis. The Newcastle-Ottawa scale was used to evaluate the quality of the literatures. Meta-analysis was performed using RevMan 5.3 software to analyze the prognostic value of platelet counts using the hazard ratio (HR) and 95% confidence intervals (95%CI).ResultsA total of 15 studies including 2 420 patients were included. The pooled HR of 1.38(95%CI 1.11~1.71,P=0.004)showed that patients with elevated platelet counts were expected to have poor overall survival (OS). Pooled of 11 studies using multivariate analysis revealed a HR of 1.67(95%CI 1.26~2.23, P=0.000 4), suggesting elevated pretreatment platelet count was an adverse prognosis factor for pancreatic cancer patients. Subgroup analysis showed that prognostic value of platelet level was stronger in patient those received surgical resection(HR=2.19, 95%CI 1.59~3.02,P<0.000 1) followed by in patient received palliative therapy (HR=1.63,95%CI 1.12~2.36,P=0.01); additionally, in patients without metastasis the increased platelet count was significantly associated with decreased OS (HR=1.61, 95%CI 1.18~2.20,P=0.003), but not in patients with metastasis (HR=1.15,95%CI 0.75~1.76, P=0.51).ConclusionPretreatment platelet count is a prognosis factor in patients with pancreatic cancer. Patients with elevated platelet count may have decreased OS, especially for those received surgical resection.
血小板来自骨髓造血干细胞生成的巨核细胞, 是血液循环中最小的无核细胞成分, 早在19世纪学者们就发现恶性肿瘤患者往往伴有血小板计数异常升高[1]。不同类型肿瘤患者中血小板计数升高的比例、水平不同, 但随着肿瘤TNM分期的升高, 其血小板增高的比例和程度都会有所提高, 提示血小板升高与肿瘤的进展存在关联。进一步研究发现肿瘤细胞本身即具有激活血小板并诱导血小板聚集的能力, 这种现象称之为“ 癌细胞诱导的血小板聚集” (tumor cell induced platelet aggregation, TCIPA), 而血小板的增多与活化又能通过多种途径促进肿瘤的生长、侵袭、转移等恶性行为[2, 3]。例如, 血小板通过释放碱性纤维母细胞生长因子(basic fibroblastic growth factor, b-FGF)、血小板衍生生长因子(platelet derived growth factor, PDGF)、血管内皮生长因子(vascular endothelial growth factor, VEGF)等多种生长因子促进肿瘤的增殖和新生血管的形成; 血小板分泌的一些蛋白水解酶类如基质金属蛋白酶、明胶酶、类肝素酶等能够分解细胞基质、促进肿瘤侵袭迁移; 血液循环中的血小板还能与肿瘤细胞聚集形成栓子, 起到保护循环肿瘤细胞免受血流剪切力的物理损伤和逃避宿主免疫杀伤的作用[4]。
胰腺癌是消化系统常见恶性肿瘤之一, 具有起病隐匿、进展迅速、易复发转移等特点, 近年来发病率不断升高[5]。血小板计数是临床常规检测项目, 具有成本低、检测便捷等特点, 大量研究表明其与胰腺癌预后关系密切, 可能是一种可靠的预后指标, 但相关研究尚存在争议。故本研究全面系统地检索相关文献, 并采用Meta分析的方法客观评价血小板计数作为胰腺癌预后指标的价值, 从而为指导临床诊治提供科学依据。
计算机检索 PubMed、 EMBASE、Cochrane 图书馆、中国知网、维普、万方数据库, 查找有关外周血血小板水平与胰腺癌预后相关的文章, 检索时限均为从建库至 2017 年8 月 1日。采用自由词与主题词相结合的方式进行检索。中文检索词包括胰腺癌、胰腺恶性肿瘤、胰腺肿瘤、血小板、血常规、血像、血液指标、血液参数。英文检索词包括pancreas、 pancreatic、tumor、tumour、neoplasm、cancer、carcinoma、adenocarcinoma、 platelet、blood、hematological、hemogram、platelet。以PubMed为例, 具体检索策略如下:(pancreas OR pancreatic) AND (tumor OR tumors OR neoplasm OR neoplasms OR cancer OR carcinoma OR adenocarcinoma) AND (hematological OR hemogram OR platelet)。
1.2.1 纳入标准
研究类型为前瞻性或回顾性队列研究。研究对象为病理确诊为胰腺癌的患者。暴露因素为外周血血小板水平, 结果判读根据原始文献临界值区分。研究的结局指标为血小板水平与胰腺癌患者生存情况, 至少报道一项生存指标。
1.2.2 排除标准
排除下列文献:①综述、会议摘要、评论等非论著文章; ②数据缺失导致无法提取可以进行Meta分析的效应量, 联系作者无果的研究; ③同一人群发表的多篇报道, 只纳入最新、报道结果最完整的文章。
由两位研究者(周雨和林叶)使用标准化的数据提取表独立提取数据。提取内容包括:(1)研究的一般特征, 包括作者、发表时间等; (2)研究纳入人群的一般特征, 包括性别、年龄、疾病分期分级、接受的治疗方式等; (3)研究的方法学特征。纳入队列研究的偏倚风险采用NOS(Newcastle-Ottawa scale)量表进行评价, 总分6分以上认为研究质量较高。如意见分歧通过与第三者(简志祥)共同讨论解决。
所有合并分析采用 RevMan 5.3 软件进行。选择风险比(hazard ratio, HR)及其95%置信区间(confidence interval, CI)作为评价生存情况的效应量, 总生存(overall survival, OS)作为主要结局指标。如文献中给出具体数据, 直接提取; 如文献中只提供生存曲线, 则通过Tierney等提供的方法由生存曲线提取计算[6]。各研究间的异质性用 Q 检验和 I2检验来探究, 如P< 0.01或I2> 50%则认为异质性较大, Meta分析采用随机效应模型, 反之则采用固定效应模型。所有合并结果以P< 0.05为差异有统计学意义。
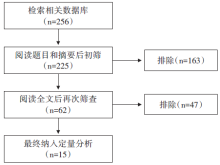
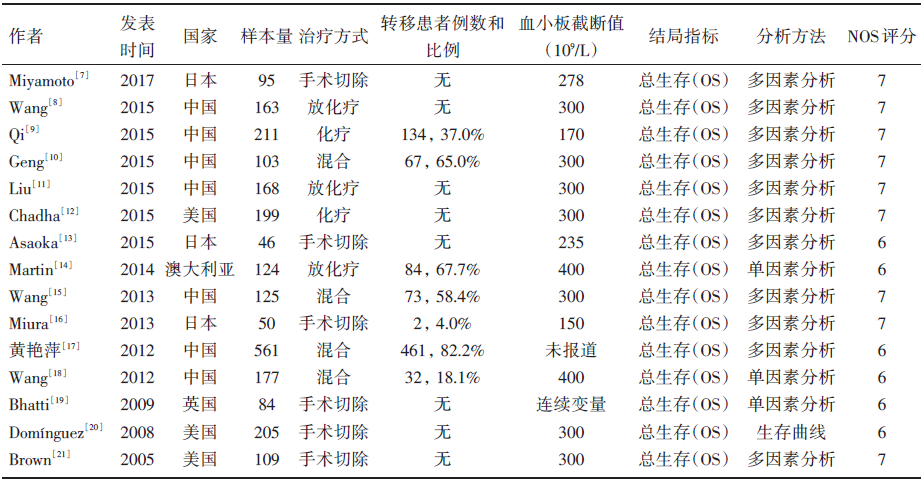
通过上述的检索策略, 初步检索各数据库共获得文献256篇。去掉31篇重复文章后, 通过阅读标题和摘要排除了163篇文献, 将剩余的62篇文献进行全文阅读, 根据纳入与排除标准, 共纳入15篇文献进行Meta分析[7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21]。具体筛选流程见图1。纳入研究的一般特征与质量评价结果见表1。所有研究都是回顾性的, 且都以OS为主要结局指标, 共纳入2 420例胰腺癌患者。11项研究采取了多因素回归的方法计算HR[7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 21]。质量评价分数分布于6~7分, 缺乏组间可比性是扣分的最常见原因。
| 表1 纳入研究的基本特征 |
2.2.1 主要结果
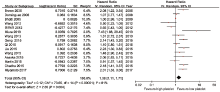
所有(15篇)研究均报道了治疗前外周血血小板水平与胰腺癌患者预后的关系。采用随机效应模型合并各研究结果, 发现血小板水平升高是预后不良的风险因素(HR=1.38, 95%CI 1.11~1.71, P = 0.004, I2= 81%), 见图2, 其中I2> 50%提示各研究间存在异质性。
2.2.2 亚组分析
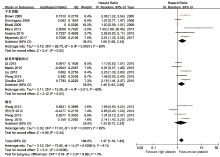
根据研究人群的不同, 将纳入研究分为三组:第一组为只纳入接受手术切除胰腺癌患者的研究, 第二组为只纳入接受姑息性治疗的不可切除胰腺癌患者的研究, 第三组为既纳入手术患者又纳入姑息性不可手术患者的研究。亚组分析发现, 治疗前外周血血小板水平在第一组和第二组中均为预后指标, 合并的HR分别为1.60(95%CI 1.09~2.34, P=0.02)和1.46(95%CI 1.03~2.06, P=0.03), 见图3。
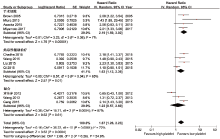
共有11篇文章采取多因素回归的方法计算HR[7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 21], 其合并后HR为1.67(95%CI 1.26~2.23, P=0.000 4, I2=72%); 参照上述分组, 对这11篇研究进行亚组分析, 发现治疗前血小板水平升高是胰腺癌患者根治性术后预后不良的独立风险因素(HR=2.19, 95%CI 1.59~3.02, P< 0.000 1, I2=7%); 同时也是姑息性治疗胰腺癌患者预后不良的独立风险因素(HR=1.63, 95%CI 1.12~2.36, P=0.01, I2=65%)。见图4。针对根治性手术患者的各研究合并结果I2仅为7%, 提示研究间异质性很小, 可能与可接受根治性手术的胰腺癌患者同质性较好有关。
根据纳入人群是否包含转移患者, 进行亚组分析。合并8篇没有纳入转移患者的研究, 结果显示血小板水平与预后显著相关(HR=1.61, 95%CI 1.18~2.20, P=0.003); 而合并7篇纳入了转移患者的研究显示血小板水平与预后无关(HR=1.15, 95%CI 0.75~1.76, P=0.51)。见图5。上述结果提示血小板水平对不伴有转移的胰腺癌患者预后指示作用更好。
2.2.3 敏感性分析和发表偏倚
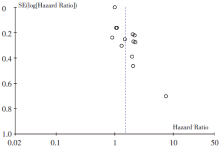
通过切换固定效应模型和随机效应模型, 或从总体合并结果中抽出单个研究进行敏感性分析, 结果显示Meta分析结果稳定。血小板水平与胰腺癌患者具有关系的漏斗图结果显示各研究在图形上分布基本对称, 提示发表偏倚较小, 见图6。
恶性肿瘤患者常伴有外周血血小板计数增高, 这种现象可能由几种机制共同引起[2, 22, 23]:①肿瘤细胞能够分泌促血小板生长因子, 它能促进骨髓巨核细胞集落形成, 使血小板生成增多; ②肿瘤细胞产生的白介素-6等炎性因子诱导促血小板生成素、巨核细胞生长因子的产生; ③肿瘤患者血液高凝状态、肿瘤引起的出血失血、肿瘤组织坏死等造成血小板破坏加速, 造成代偿性血小板增多。同时, 肿瘤细胞能够诱发TCIPA现象, 促进血小板的活化、聚集[2]。肿瘤与血小板增多之间的紧密联系促使人们探讨其临床价值, 目前已有诸多研究显示血小板升高与多类肿瘤患者的预后相关。尽管胰腺癌患者常伴有高凝状态和血小板升高, 也有许多研究提示血小板水平可作为胰腺癌患者预后的一个潜在指标, 但尚未获得高质量循证医学证据支持。
我们的Meta分析结果显示, 在胰腺癌患者中, 治疗前外周血中血小板水平与临床预后关系密切, 血小板计数升高提示预后不良。亚组分析发现, 在接受根治性手术切除的胰腺癌患者中, 治疗前血小板水平与预后关系最为密切, 其次为接受姑息性治疗的患者。表明治疗前血小板水平能够作为胰腺癌预后指标, 能够广泛应用于胰腺癌患者, 尤其是可手术切除的患者中。
血小板是具有生物活性的小块物质, 自身能够分泌多种细胞因子。活化、增殖的血小板对肿瘤的生长、转移具有重要作用[24]。血小板在肿瘤生长的早期就能表达、释放血小板反应蛋白(thrombospondin, TSP)、b-FGF、PDGF等多种促癌成分, 不但能够直接促进肿瘤细胞生长, 还能上调肿瘤细胞上的 Twist、Snail、Vimentin等基因的表达从而促肿瘤细胞上皮间质转化的发生, 增强肿瘤细胞抗凋亡、自噬和增殖的能力[25]。血小板还能储存和表达包括VEGF在内的30多种重要的血管生成调节蛋白, 不但能够促进肿瘤血管新生, 还能保护和维持肿瘤血管的完整性。研究还发现, 血小板对血液循环中的肿瘤细胞具有保护作用。循环肿瘤细胞同时面临血流剪切力产生的机械损伤和宿主免疫系统的攻击, 而肿瘤细胞与血小板能够在粘附因子、纤维蛋白原的作用下形成血小板-肿瘤细胞栓子, 抵抗血流动力的机械损伤; 因血小板属于正常细胞, 还能够有效降低自然杀伤细胞等免疫细胞的免疫原性, 诱导免疫耐受, 此外包围肿瘤细胞的血小板还能形成物理屏障阻碍免疫细胞与肿瘤细胞的直接接触[26]。除上述分子生物学机制外, 高凝状态和血小板活化引起的静脉血栓本身就是晚期肿瘤患者死亡的第二大诱因[27]。血小板这种多途径的促癌作用使得抗血小板治疗成为一种潜在的治疗肿瘤的新途径。已经有临床研究结果显示抗血小板药物能够改善肿瘤患者的预后、延长生存期[28], 通过靶向纳米药物抑制血小板功能也为抗肿瘤治疗提供了一种新策略[29]。
本研究存在一些不足:①所有纳入研究都是回顾性研究; ②大多数研究没有采取匹配设计的方法提高组间患者基线数据的可比性; ③几乎所有研究将血小板计数作为二分类变量进行分析, 但各研究间血小板升高和降低的标准并未统一。因此, 如能开展前瞻性、匹配设计的队列研究, 进一步明确血小板计数作为胰腺癌预后指标的价值, 明确其最佳截断值, 对于其临床应用具有重要作用。此外, 通过本研究我们初步明确了治疗前外周血血小板计数是胰腺癌的预后指标, 但也发现尚缺乏研究探讨治疗过程中血小板计数水平和变化情况与复发、转移、预后的关系, 这也是未来研究应着重探讨的问题。
综上, 现有证据表明:治疗前外周血血小板计数是胰腺癌的重要预后指标, 血小板水平升高提示预后不良。血小板检测简单便捷, 是易于临床应用的预后指标。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|