作者简介:

李志铭,教授,主任医师,博士研究生导师,中山大学肿瘤防治中心内科。中国抗癌协会青年理事会常务理事,中国临床肿瘤学会(CSCO)抗淋巴瘤联盟副秘书长、常务委员,中国抗癌协会淋巴瘤专业委员会青年委员会副主任委员,中国医师协会肿瘤医师分会青年委员会副主任委员,广东省抗癌协会靶向与个体化治疗专业委员会副主任委员,广东省中西医结合学会肿瘤免疫专业委员会副主任委员,广东省健康管理学会生育力保护专业委员会副主任委员,广州抗癌协会淋巴瘤专业委员会副主任委员,广东省抗癌协会化疗专业委员会常务委员,中国抗癌协会淋巴瘤专业委员会委员。
Madle M, Kramer I, Lehners N, et al. The influence of Rituximab, high-dose therapy followed by autologous stem cell transplantation, and age in patients with primary CNS lymphoma[J]. Ann Hematol, 2015, 94(11):1853-1857.
2a。
95%以上的原发中枢神经系统淋巴瘤(primary central nervous system lymphom, PCNSL)的病理类型为弥漫大B细胞淋巴瘤。利妥昔单抗为系统性弥漫大B细胞淋巴瘤标准治疗方案的重要组成部分, 但其血脑屏障通过率低, 在PCNSL中的运用尚无定论。
回顾性临床资料分析, 明确利妥昔单抗是否可改善大剂量甲氨蝶呤(high-dose Methotrexate, HDMTX)为主的化疗方案在PCNSL的生存率。
• 研究条件:德国海德堡大学附属医院2000-2011年的临床病例资料。
• 研究方法:回顾性临床研究。
• 研究对象:接受过至少1个疗程的HDMTX为主化疗方案治疗的PCNSL患者。
• 干预措施:52名患者接受HDMTX为主的化疗方案, 27名患者接受HDMTX为主的化疗方案联合利妥昔单抗治疗。
• 评价指标:生存率。
利妥昔单抗与HDMTX联用可提高PCNSL患者的生存率。
本研究是基于PCNSL进行的一项单中心回顾性研究。PCNSL是非霍奇金淋巴瘤的一种亚型, 只局限于中枢神经系统, 可累及脑、脊髓、眼、软脑膜而无全身受累的表现。病理类型以弥漫大B细胞淋巴瘤多见(> 90%)[1, 2]。根据CBTURS的统计数据, PCNSL的5年生存率为33%, 10年生存率为25.6%。
现国际上以HDMTX为基础的联合化疗作为主要治疗方案, 以大剂量化疗加造血干细胞移植为巩固治疗方案。已有数据证实手术治疗对于延长生存期无益, 全脑放疗单用于临床治疗可得到临床缓解但几乎所有患者都会复发, 全脑放疗与化疗联用相比于单用化疗患者的无进展生存率有所提高, 但对总生存率并无影响[3]。目前对于PCNSL的治疗仍存在许多问题, 包括诱导化疗有效率不够、复发率高、联合化疗耐受性差、副反应大且诱导有效后进行全脑放疗巩固治疗的神经毒性大等等。也就是说, 治疗的困境在于一方面要强化治疗以提高治愈率, 另一方面要尽可能减低或避免神经毒性。
以HDMTX为基础的联合化疗已成为国际热点, 而利妥昔单抗是其中的一个重点。Shah 等2007年报道, 将利妥昔单抗联合MPV方案(HDMTX+甲基卞肼+长春新碱)用于初治PCNSL患者的诱导治疗, 客观缓解率为93%, 完全缓解率为78%。Wieduwilt 等2012年报道, 在31例中位年龄61岁的初治PCNSL患者中, 应用MT-R方案(HDMTX+TMZ+利妥昔单抗)进行诱导化疗, 有效患者随后以EA方案(依托泊苷联合HD-阿糖胞苷)进行巩固治疗, 诱导化疗的客观缓解率为 52%, 对于接受了巩固治疗的患者, 2年无进展生存率和总生存率则分别为78%和93%, 整体治疗有效且耐受性良好, 无明显神经毒性。这两项研究提示出以利妥昔单抗联合不同的化疗方案对PCNSL进行治疗的可行性与安全性, 然而并未展开系统性对照性临床试验以提供参考。
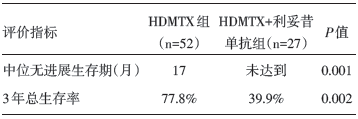
本次我们所评价的由Madle等发布于2015年的研究, 主要意义在于进行了回顾性分析, 证实了利妥昔单抗在PCNSL中作为一线治疗的应用价值, 除此之外还分析了年龄(≤ 60岁vs. > 60岁)、自体干细胞移植等因素对于患者预后的判断以及总生存率的影响。结果可见应用利妥昔单抗患者的3年总生存率为77.8%, 未使用者仅为39.9%; ≤ 60岁患者的总生存率为78.2%, > 60岁者为38.7%; 化疗与自体干细胞移植联用患者的3年总生存率为85.2%, 未使用自体干细胞移植者只有35.2%。结论认为利妥昔单抗、年龄以及是否使用自体干细胞移植均为PCNSL的独立预后因素。而此结论与之前的其他临床观察性研究以及后续的IELSG32前瞻性试验相吻合。
该研究的缺陷在于, 由于是回顾性试验, 具体联合化疗方案的使用剂量及是否进行鞘内注射等并未列出也未做出讨论, 化疗方案达到9种以上, 可能带来较多干扰因素。另外, 该研究为单中心回顾性研究, 受到地域、人种等不同因素的限制。然而, 该研究例数较多且对于多因素分析考虑全面。在后续2016年Ferreri 等开展的前瞻性多中心临床试验中得到了较好的证实。Ferreri 等开展的IELSG32前瞻性临床研究证实, 中位随访30个月, 接受利妥昔单抗和塞替哌治疗患者的完全缓解率为49%(95%可信区间38%~60%), 仅接受甲氨蝶呤/阿糖胞苷治疗患者的完全缓解率为23%(95%可信区间14%~31%), 风险比0.46(95%可信区间 0.28~0.74); 其他接受甲氨蝶呤/阿糖胞苷+利妥昔单抗治疗患者的完全缓解率为30% (95%可信区间21%~42%), 风险比0.61(95%可信区间0.40~0.94)[4]。而该研究同时证明了全脑放疗和自体干细胞移植分别与化疗联用对于患者的无进展生存期均有意义[5]。基于这些临床研究的结果, 现利妥昔单抗已被美国NCCN指南列入PCNSL二线治疗方案的选择。
然而, 2017年12月美国血液病学年会报道, 由Doorduijn领导的200例患者的国际多中心Ⅲ 期临床试验却发现, 新诊断的PCNSL中, 利用利妥昔单抗治疗基于HDMTX的化疗虽然尚未达到中位总生存期, 但缓解率、无事件生存率或无进展生存率并未有所提高, 需要更长时间的随访来评估对总生存的影响。而基于年龄与利妥昔单抗的探索性多变量分析表明利妥昔单抗可能对年轻患者产生影响。因此利妥昔单抗对于PCNSL的作用仍待考证, 我们对该试验的最终结果拭目以待。
其他的化疗药物比如阿糖胞苷, 靶向药物如依鲁替尼、来那度胺、PI3K抑制剂Buparlisib、mTOR抑制剂西罗莫司脂化物、PD-1抗体、CAR-T等治疗PCNSL的临床试验也在进行中。相信随着临床试验的开展, 未来对于PCNSL的治疗将不断取得突破性进展。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|