作者简介:
 | 胡夕春教授,复旦大学附属肿瘤医院临床试验机构常务副主任、肿瘤内科主任,上海抗癌协会乳腺癌专业委员会副主任委员、上海市疾病预防控制中心乳腺癌防治专业委员会副主任委员、中国抗癌协会乳腺癌专业委员会常务委员兼秘书长、国家食品药品监督管理局审评中心审评专家、中国抗癌协会癌症康复和姑息治疗委员会常务委员、中国抗癌协会临床肿瘤学协作专业委员会学术委员会委员、美国临床肿瘤学会(ASCO)会员、上海市肿瘤化疗质控中心专家委员会委员、中国研究型医院学会乳腺专业委员会副主任委员、上海抗癌协会癌症康复和姑息治疗委员会主任委员。曾经在美国Rochester的Mayo Clinic参加临床试验培训,主要致力于肿瘤化疗,尤其是乳腺癌内科治疗的研究。目前担任《International Journal of Biological Markers》、《Journal of Bone Oncology》、《中华乳腺病杂志》、《中国癌症杂志》、《临床肿瘤学杂志》和《中德临床肿瘤学杂志》编委。获得过中国抗癌协会科技奖一等奖、上海市医学科技进步奖一等奖、全国妇幼健康科学技术奖一等奖等多项奖项。目前已经发表论文160多篇。 |
Lowenfeld L, Mick R, Datta J, et al. Dendritic cell vaccination enhances immune responses and induces regression of HER2pos DCIS independent of route: Results of randomized selection design trial[J]. Clin Cancer Res, 2017, 23(12): 2961-2971.
1b。
• 人表皮生长因子受体2(human epidermal growth factor receptor 2, HER2)阳性乳腺癌患者存在抗HER2 Th1免疫应答的进行性丧失, HER2肽脉冲式树突状细胞(dendritic cell, DC)可诱导强烈的抗HER2免疫反应。
• 静脉、皮下或淋巴结内注射DC疫苗可诱导特异性T细胞应答。
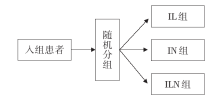
• 通过病灶内(intralesional, IL)、淋巴结内(intranodal, IN)或病灶内和淋巴结内(intra-lesional and intranodal, ILN)注射DC疫苗, 建立不同接种途径的安全性, 并评估其免疫和临床效应。
• 研究条件: 宾州大学Abramson癌症中心的临床试验协作项目(DCIS 6)。
• 研究时间: 2009年7月至2015年7月。
• 研究方法: 多中心, Ⅲ 期, 随机对照临床试验。
• 研究对象: 患者活检证实为HER2阳性导管原位癌(ductal carcinoma in situ, DCIS), DCIS合并微小浸润癌, DCIS合并浸润性癌且最大径< 5 mm, 或乳头Paget's病。未曾接受治疗。
• 干预措施: 干预措施和流程见图1。
• 评价指标: 外周血和前哨淋巴结中的免疫应答率, 手术切除标本的病理学反应。
共入组54例HER2阳性乳腺癌患者(包括42例DCIS及12例早期浸润性乳腺癌)。患者对所有注射途径的疫苗接种都具有良好的耐受性, 见表1。DCIS患者外周血和前哨淋巴结的病理学反应情况见表2。DCIS患者的病理完全缓解(pathologic complete response, pCR)率高于早期浸润性乳腺癌患者(28.6% vs. 8.3%)。
| 表1 不同注射途径患者免疫应答率的比较 |
| 表2 DCIS患者不同病理学应答评价指标的比较 |
• 抗HER2 DC1疫苗是一种安全且具有免疫原性的治疗方法, 用以诱导HER2阳性患者肿瘤特异性T细胞应答, 其免疫和临床效应与接种途径无关。
• 与外周血相比, 前哨淋巴结的免疫反应可作为更能反映抗肿瘤活性的终点。
目前免疫治疗作为攻克肿瘤的新方法获得了广泛的关注, 其在多个瘤种中已被证实具有显著的疗效。免疫治疗主要针对肿瘤免疫的缺陷环节, 通过激活主动免疫、被动免疫和逆转免疫抑制等方式恢复肿瘤特异性的免疫反应, 攻击肿瘤细胞。但免疫治疗在乳腺癌当中的疗效却并不显著。
由于免疫治疗本身的特性, 它可能在尚未建立免疫抑制微环境的较为早期的肿瘤中或肿瘤病灶已清除而仅剩尚未激活的残余肿瘤细胞的情况下更为有效。而HER2阳性的乳腺癌组织中抗HER2的免疫反应有不同程度的缺陷[1]。因此该研究利用受HER2肽链激活的DC刺激机体主动产生HER2特异性的T细胞应答, 探索其在术前应用于HER2阳性的42名乳腺DCIS患者和12名pT1mic/pT1aN0M0(早期浸润性)乳腺癌患者的安全性和有效性。
结果显示, 该研究纳入的54名患者均完成了所有的治疗, 并且无3级及以上的不良事件发生。疫苗的安全性与注射途径无显著关联。在53名可评估免疫反应的患者中, 43名(81.1%)检测到了新发生或增强的免疫反应。这同样与注射途径无显著关联, 但经淋巴结注射者发生HER2特异性CD4阳性T细胞免疫反应者相对较多(外周血89.5%, 前哨淋巴结91.7%)。乳腺DCIS患者和浸润性癌患者在免疫反应的激活上无明显差异。在临床疗效上, 13名患者获得pCR, 其中DCIS者占多数, 并且DCIS患者pCR率达28.6%。获得pCR与未获得pCR的患者相比, 前哨淋巴结中的HER2特异性免疫反应更为活跃, 而外周血中的反应在二者之间无显著差异。
该研究中HER2特异性的DC疫苗显示了其有效激发HER2特异性免疫反应的能力并在DCIS患者中获得了大于20%的pCR率, 明显优于现有的免疫治疗在乳腺癌患者中的疗效。根据回顾性研究结果, HER2阳性的DCIS相较于其他DCIS更容易复发[2, 3]。这一新的治疗方式可能降低这类患者的局部复发率甚至死亡率, 需要进一步样本量更大、随访时间更长的临床研究来证实。
但应用现有的治疗手段 , DCIS的患者10年乳腺癌特异生存率已达97%~98%[4]。全球范围多项前瞻性对照研究提示, 行保乳手术者的8~10年局部复发率为4%~20%, 行全乳切除术者为2%~9%, 保乳手术联合辅助放疗者的局部复发率可降低至与全乳切除术相当或略高水平[5, 6, 7, 8]。尽管有Ⅱ 期临床试验表明术前HER2靶向治疗能安全地缩小DCIS[9], 但目前国内外指南与共识暂无对粗针穿刺结果显示DCIS且淋巴结阴性的患者进行新辅助治疗的推荐。对于术后病理明确为DCIS患者的辅助治疗, 也仅推荐ER阳性患者进行内分泌治疗, 而不推荐针对HER2的辅助治疗。NSABP B-43 Ⅲ 期临床试验试图评估曲妥珠单抗辅助治疗对HER2阳性DCIS患者预后的影响, 目前随访结果尚未公布[10]。但Alvarado等的研究显示, 加用曲妥珠单抗的成本效益极低, 对这类患者可以说是一种过度治疗[11]。DC疫苗的制造成本较曲妥珠单抗更高, Dendreon公司甚至因不堪细胞疫苗研发的重负而破产。在10年局部复发率低于10%且疾病特异生存率高于95%的人群中应用这一昂贵的治疗方式无疑成本效益更低。本研究还入组了pT1mic/pT1aN0M0的患者, 尽管DC疫苗疗效不佳, 但在现有治疗手段下, 这些患者无论是否接受辅助全身治疗, 5年无复发生存率为89.4%~97.2%, 5年总生存率为95.7%, 接受辅助全身治疗患者的5年无复发生存率甚至达92.2%~100%, 5年总生存率达99.0%[12, 13, 14]。
综上所述, 该研究的学术价值远远超过它的社会经济学价值, HER2特异性的DC疫苗虽然在DCIS患者中显示可观的疗效, 但成本效益可能极低, 在DCIS患者未来治疗中的地位存疑。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|