作者简介:
 | 杨学宁,肿瘤学博士,主任医师,现任广东省人民医院/广东省肺癌研究所肺外科(肺二科)科主任、中国抗癌协会肺癌专业委员会副主任委员、中国临床肿瘤学会(CSCO)理事、广东省医学会循证医学分会主任委员、《循证医学》杂志副主编、《中国肺癌杂志》常务编委。从事肿瘤外科临床工作十五年,擅长肺癌等胸部肿瘤多学科综合治疗。主要研究方向为以外科为主的肺癌多学科综合治疗、肺癌免疫治疗和孤立肺结节诊断。 在肺癌的早期诊断和治疗,肺结节的诊疗策略,肺癌各期淋巴结转移规律和淋巴结清扫范围以及术前术后辅助治疗方面有深入的研究。参与组织多个有关非小细胞肺癌围术期化疗的国内多中心随机对照研究,参与多个国际多中心随机对照临床研究。参加和主持国家“十五”重大科技专项、国家卫生健康委员会、广东省科委、广东省卫生计生委等多项科研项目。国家科学技术进步奖二等奖《肺癌分子靶向精准治疗模式建立和推广》和广东省科学技术奖一等奖《可手术非小细胞肺癌系统性淋巴结清扫的基础和临床研究》获得者。在国内外发表相关学术论文五十余篇。专著《肺癌多学科综合治疗的理论与实践》副主编,《2010中国肺癌临床指南》等多部专业著作委员。 |
Wakelee HA, Dahlberg SE, Keller SM, et al. Adjuvant chemotherapy with or without Bevacizumab in patients with resected non-small-cell lung cancer (E1505):An open-label, multicentre, randomised, phase 3 trial[J]. Lancet Oncol, 2017, 18(12):1610-1623.
1b。
• 可手术非小细胞肺癌术后行辅助化疗可提高患者的生存期。
• 贝伐珠单抗为针对血管内皮生长因子的单克隆抗体, 在晚期非鳞非小细胞肺癌中, 在含铂化疗方案的基础上加用贝伐珠单抗可延长患者的生存期。
本研究旨在探讨可手术非小细胞肺癌辅助化疗中加入贝伐珠单抗对患者生存期的影响。
• 研究条件: 美国、加拿大等多国参加的全球多中心E1505研究(NCT00324805)。
• 研究时间: 2007年6月1日至2013年9月20日完成受试者登记和随机分组。
• 研究方法:全球多中心、开放标签的Ⅲ 期随机临床试验。
• 研究对象:完全切除的Ⅰ B (≥ 4 cm) ~Ⅲ A期非小细胞肺癌(AJCC 6th), 且行标准术后含铂双药辅助化疗的患者。
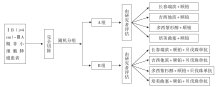
• 干预措施:患者随机分为两组, A组仅接受术后辅助化疗, 共4周期; B组在接受术后辅助化疗的基础上, 从第一周期术后辅助化疗开始即加用贝伐珠单抗, 每21天一次, 共1年。其中化疗方案为含顺铂(75 mg/m2, 第1天, 每21天1周期)的双药, 另一药物根据研究者判断可选择长春瑞滨(30 mg/m2, 第1天和第8天)、吉西他滨(1 200 mg/m2, 第1天和第8天)、多西紫杉醇(75 mg/m2, 第1天)或培美曲塞(500 mg/m2, 第1天), 见图1。
• 评价指标:采用意向性治疗分析, 主要研究终点指标为总生存期, 并根据化疗方案、分期、病理类型、性别进行分层。
A组最终入组749例, B组最终入组752例。入组患者的主要病理类型为腺癌(58%)和鳞癌(28%), 大部分患者为Ⅱ 期(44%), Ⅲ A/N2期患者仅占26%; 共有12.8%的患者接受全肺切除, 75.6%的患者接受肺叶切除。具体信息详见表1。
| 表1 入组患者的基本临床特征 |
辅助化疗中增加贝伐珠单抗并不能提高早期可手术非小细胞肺癌患者的生存期, 此类患者的辅助治疗中不应使用贝伐珠单抗。
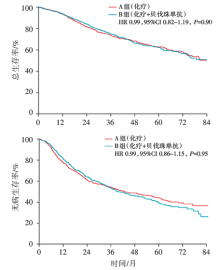
E1505研究这项耗时10年的Ⅲ 期临床试验显示[1], 术后化疗联合贝伐珠单抗与术后化疗相比, 不能延长总生存期和无病生存期。即使亚组分析也未能发现非鳞癌组有生存获益。而且, 联合贝伐珠单抗方案的毒性更大。E1505研究的结论是:贝伐珠单抗在非小细胞肺癌术后辅助治疗中没有地位。
在晚期非鳞非小细胞肺癌的多项研究中, 贝伐珠单抗联合紫杉醇/卡铂或者吉西他滨/顺铂方案首次超过了1年生存期[2]。因此含贝伐珠单抗的方案获得热烈追捧, 并自然地推向辅助治疗。然而, E1505研究的结果却提示我们, 不能简单地将晚期抗肿瘤治疗方案应用为辅助治疗方案。在此前已报道的结肠癌和乳腺癌术后辅助治疗研究中, 化疗联合贝伐珠单抗方案亦不能增效。
在E1505研究启动的2007年, 晚期非小细胞肺癌正大步进入精准医学时代。然而, 贝伐珠单抗遗憾地无类似EGFR-TKI那样有可预测其有效性的肿瘤标志物/驱动基因。至今未找到贝伐珠单抗和其他抗血管生成药物的预测性生物标志物。因此, 研究者无法筛选出贝伐珠单抗的有效人群, 甚至也未能如IPASS研究般富集潜在有效人群(腺癌), 虽然有E4599的非鳞癌优势人群可供参考。再加上入组Ⅰ B~Ⅲ A期差异这么大的分期, 导致需要极大的样本量和很长的入组/随访时间才能得到研究结果。同样无差别入组的国际肺癌辅助治疗研究(International Adjuvant Lung Cancer Trial, IALT)入组了1 867例非小细胞肺癌并耗时10年时间[3]。
此外, 漫长的研究时间也是一个不确定因素!我们难以预测一个10年后才能获得结论的研究。因为新的高效药物出现, 更精准的人群选择, 从而使研究原设计要回答的问题大打折扣!例如, 继E1505研究2007年开始之后, EGFR-TKI靶向辅助治疗CTONG1104研究也在2011年开始入组[4], 而贝伐珠单抗与吉非替尼的潜在优势人群有重叠。即使今天E1505是阳性结论, 我们在面临腺癌人群时仍然会优选EGFR基因检测明确是否适合接受EGFR-TKI辅助治疗。
E1505研究的结果提示贝伐珠单抗在辅助治疗研究中需要一个预测性肿瘤标志物。CTONG1104研究开创了精准辅助治疗时代, 未来设计辅助治疗或者新辅助治疗临床试验应尽可能在精准医学原则的指导下进行。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|