| 石敏, 肿瘤学博士、主任医师、副教授、学术型博士研究生导师、博士后合作导师、南方医科大学南方医院肿瘤内科副主任。 从事恶性肿瘤的临床、科研和教学工作20余年,擅长恶性肿瘤的个体化综合诊疗,尤其在胃肠肿瘤的内科治疗方面有较丰富经验。注重胃肠道肿瘤代谢、转移、肿瘤微环境等领域的转化及机制研究,主要研究方向:基于分子检测的胃肠肿瘤个体化治疗,胃肠肿瘤代谢重塑和微环境,肝转移瘤的力学生物学。 |
研究一: Allegra CJ, Yothers G, O'Connell MJ, et al. Neoadjuvant 5-FU or Capecitabine plus radiation with or without Oxaliplatin in rectal cancer patients: A phase Ⅲ randomized clinical trial[J]. J Natl Cancer Inst, 2015, 107(11). pii: djv:248.
研究二:Azria D, Doyen J, Jarlier M, et al. Late toxicities and clinical outcome at 5 years of the ACCORD 12/0405-PRODIGE 02 trial comparing two neoadjuvant chemoradiotherapy regimens for intermediate-risk rectal cancer[J]. Ann Oncol, 2017, 28(10): 2436-2442.
研究一:1b; 研究二:2a。
T3-4N0M0或TanyN+M0直肠癌的标准治疗是全直肠系膜切除手术(total mesorectum excision, TME), 有许多临床试验评价了新辅助治疗中放疗加氟尿嘧啶类化疗治疗直肠癌的疗效, 结果提示可降低局部复发率, 提高局部控制, 但不论术前还是术后联合应用氟尿嘧啶类为基础的化疗, 均未能明显改善总生存率(overall survival, OS)。因此需要新策略来改善局部进展期直肠癌的无病生存率(disease-free survival, DFS)和OS。基于氟尿嘧啶类的结肠癌辅助化疗中加入奥沙利铂对DFS和OS有获益。因此, 这种组合在几项试验中进行了研究, 同时进行了新辅助放疗, 期望得到更好疗效及生存控制。
进一步明确奥沙利铂在局部晚期直肠癌新辅助化疗中的作用。
研究一:
• 研究条件:NSABP R-04研究是以美国为主的多中心临床注册项目 (NCT00058474)。
• 研究时间:2004年7月至2010年8月。
• 研究方法:随机、开放、Ⅲ 期多中心临床研究, 共入组Ⅱ /Ⅲ 期直肠癌患者1 608例。
• 研究对象:Ⅱ /Ⅲ 期直肠腺癌患者。入组标准:年龄≥ 18岁, ECOG评分0~1, 预期寿命5年以上, 诊断Ⅱ /Ⅲ 期直肠腺癌, 肿瘤必须被认为适合于根治性切除术。排除标准:6个月以内发生心肌梗塞、活动性感染、盆腔放疗。
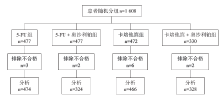
• 干预措施:流程图见图1。
• 评价指标:主要研究终点指标是肿瘤局部控制率, 次要终点是OS、DFS、局部复发时间。
研究二:
• 研究条件:56 个机构参加的ACCORD 12研究为以法国为主的多中心临床注册项目(NCT00227747)。
• 研究时间:2005年11月至2008年7月。
• 研究方法:随机、多中心临床研究。
• 研究对象:中度风险直肠腺癌患者598 名参与试验。患者入选标准:组织学证实的腺癌, 可通过数字直肠检查, 分期T2Nx 远端前直肠或T3-T4NxM0(通过直肠内超声和/或磁共振成像)。
• 评价指标:主要终点指标为病理完全反应率(pathological complete response, pCR)。次要终点指标为是总生存期、无病生存期、圆周直肠边缘、括约肌保留和局部控制。
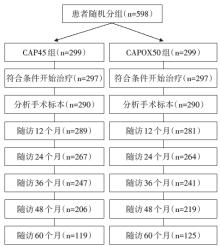
• 干预措施:两种新辅助放化疗方案随机分配:CAP45 组(RT 45 Gy, 5 周, 同期卡培他滨)和CAPOX50组(RT 50 Gy, 5周, 同期卡培他滨和奥沙利铂)。干预措施流程见图2。
研究一:
5-FU与卡培他滨方案随机治疗的1 608例患者, 其3年局部肿瘤控制率 (11.2% vs. 11.87%)、5年DFS (66.4% vs. 67.77%)、5年OS (79.9% vs. 80.7%)的差异没有统计学意义。含奥沙利铂与不含奥沙利铂治疗方案的三个终点指标:局部肿瘤控制率、DFS和OS(11.27% vs. 12.1%、69.2% vs. 64.2%和81.3% vs. 79.07%)差异均无统计学意义, 与全人群相比, 奥沙利铂组的3~4级腹泻发生率差异有统计学意义(P< 0.000 1), 行R0切除术后患者的3年局部复发率为3.1%~5.1%。
研究二:
598例患者中位随访60.2个月, 治疗组在无病生存期和总生存期的多变量分析中没有差异[风险比(hazard ratio, HR)1.02, 95%可信区间(confidence interval, CI)0.76~1.36, P=0.9; HR 0.87, 95%CI 0.66~1.15, P=0.3]。单因素分析的局部控制率无显著性差异(HR 0.92, 95%CI 0.51~1.66, P< 0.7)。晚期毒性可接受, 1.6%出现Ⅲ 度肛门失禁, < 1%出现Ⅲ 度腹泻、直肠出血、狭窄、尿失禁、尿潴留、骨髓毒性和Ⅲ ~Ⅳ 度疼痛。随着时间的推移勃起功能障碍略有增加, 5年时勃起功能障碍率为63%。两组的毒性反应差异没有统计学意义。
对于局部进展期直肠癌, 新辅助治疗在氟尿嘧啶类加放疗的基础上增加奥沙利铂治疗, 在肿瘤局部控制、无病生存和总生存上并未带来额外好处, 且增加了治疗毒性。
直肠癌是全球最常见的恶性肿瘤之一, 也是我国肿瘤治疗领域重点关注的疾病。手术是直肠癌治疗的重要手段, TME的出现降低了局部进展期直肠癌的局部复发率[1, 2]。近些年来, 随着术前新辅助同步放化疗的推广和应用, 降低了肿瘤分期、增加了手术切除率并减少了局部复发率。然而, 直肠癌的治疗仍然存在很多问题亟待解决, 例如直肠解剖特点增加了手术的难度, 患者对保留肛门括约肌功能、性功能和排尿功能等的需求, 放疗对手术的不利影响等。
随着多项临床研究的开展, 逐渐奠定了氟尿嘧啶类药物(5-FU和卡培他滨)在新辅助放化疗中的治疗地位, 而增加奥沙利铂治疗是否能进一步增强疗效、提高pCR并且改善预后, 是临床工作者非常关心的问题。针对这个问题, 从2003年开始先后有5个大型临床研究(美国NSABP R-04、法国ACCORD 12、 意大利STAR-01、欧洲PETTAC-6以及德国CAO/ARO/AIO-04)探讨了奥沙利铂在直肠癌新辅助治疗中的作用。这些临床研究都是在氟尿嘧啶类药物的基础上增加了奥沙利铂, 作为增敏的化疗药物。
NSABP R-04旨在通过比较卡培他滨和5-FU在直肠癌患者新辅助治疗中的疗效差异, 以及在新辅助治疗中增加奥沙利铂是否对疗效产生影响, 从而观察卡培他滨和奥沙利铂在直肠癌术前新辅助治疗中的作用。研究结果提示联合卡培他滨的新辅助放化疗的pCR、保肛率及肿瘤降期与持续静滴5-FU相似。同时研究结果显示氟尿嘧啶类药物联合奥沙利铂组的pCR并无获益, 奥沙利铂并没有改善患者的局部控制率、DFS或OS, 反而增加了毒性。ACCORD 12临床研究也得到了类似的结果:在卡培他滨联合放疗的基础上增加奥沙利铂化疗, 不能改善作为首要研究终点的pCR以及3年局部控制率、无病生存期和总生存期。
在探讨奥沙利铂在局部进展期直肠癌新辅助治疗中应用的其他临床研究中, 由中山大学附属第六医院汪建平教授主持的一项多中心研究FOWARC[3], 将Ⅱ 、Ⅲ 期直肠癌患者随机分成三组, 分别予以5-FU单药化疗联合放疗、mFOLFOX6化疗联合放疗及单纯mFOLFOX6化疗。初步结果显示, 三组的pCR分别为14.3%、28.0%和6.1%, 各组的肿瘤降期率分别有37.6%、57.4%和35.8%, 证明了mFOLFOX6联合放疗有更高的pCR, 同时降低了肝转移风险。然而最终结果显示, mFOLFOX6相比传统方案, 无论是否联用放疗, 均不能改善DFS和OS。
FOWARC研究与NSABP R-04及ACCORD 12研究有不同的地方。NSABP R-04及ACCORD 12两个研究均采用奥沙利铂(50~60 mg/m2)单周方案, 持续给药亦可能使毒副反应发生率增加, 部分患者难以耐受治疗。而FOWARC研究采用mFOLFOX6方案, 将奥沙利铂剂量提高到85 mg/m2, 3~4级不良事件发生率在mFOLFOX6联合放疗组最高, 但mFOLFOX6联合放疗组的全量给药率(94.9%)和放疗接受率(90.5%)均较高, 提示在临床决策中, 要考量具体的给药方式方法。另外, 如何将pCR等指标转化成最终的OS获益, 在期待更多治疗药物、手段和方法的同时, 需要进行更多的大型临床研究。
总之, 随着多个大型临床研究的深入探讨, 为直肠癌的治疗提供了重要的指导价值。目前, 对于局部进展期直肠癌, 新辅助治疗在氟尿嘧啶类加放疗的基础上增加奥沙利铂治疗, 未给患者带来更多获益。将来, 期望通过对患者人群进行分组分层分析, 筛选出适合的适应证人群, 从而优化治疗策略。在循证医学和个体化治疗原则的引导下, 使直肠癌患者在保持生活质量的前提下, 更好地延长生存时间。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|