| 张涛,主任医师,教授,博士研究生导师,华中科技大学同济医学院附属协和医院肿瘤中心副主任,肿瘤学教研室副主任。中国临床肿瘤学会(CSCO)理事,CSCO胰腺癌专家委员会副主任委员,CSCO结直肠癌、胃癌专家委员会委员,湖北省抗癌协会肿瘤分子靶向治疗专家委员会主任委员。长期从事消化系统恶性肿瘤的基础研究和临床工作,特别在放化疗专业有较丰富的经验。在《Blood》、《Cancer Res》、《J Immunother》、《Int J Cancer》、《Oncogene》等杂志上发表论文五十余篇。获得科技部重大专项子课题一项,国家自然科学基金三项。 |
Deng Y, Chi P, Lan P, et al. Modified FOLFOX6 with or without radiation versus Fluorouracil and Leucovorin with radiation in neoadjuvant treatment of locally advanced rectal cancer: Initial results of the Chinese FOWARC multicenter, open-label, randomized three-arm phase Ⅲ trial[J]. J Clin Oncol, 2016, 34(27):3300-3307.
1b。
术前给予5-氟尿嘧啶(Fluorouracil, FU)为基础的新辅助化疗+全直肠系膜切除术(total mesorectal excision, TME)+以5-FU为基础的术后辅助化疗+术后放疗是目前局部进展期直肠癌的标准治疗方法。
在多个国际大型临床研究中, 仅有CAO/ARO/AIO-04研究证实5-FU联合奥沙利铂作为围手术期化疗可将3年无病生存率(disease-free survival, DFS)从71.2%提高至75.9%。其他研究均提示奥沙利铂作为新辅助化疗不仅毒性增加且对病理完全缓解率(pathologic complete response, pCR)及生存时间没有提高。
同样, 术前新辅助放疗也未能延长生存时间, 且增高了大小便失禁、直肠黏膜坏死、性功能障碍等并发症的发生率。
因此, 本研究对几种不同治疗方案的不同搭配之间进行相互比较, 希望能够找出更高效、低毒的围手术期治疗方案。
比较mFOLFOX6(改良的持续泵注5-FU + 亚叶酸钙 + 奥沙利铂)方案联合或不联合放疗与传统5-FU方案联合放疗在新辅助治疗局部进展期直肠癌的疗效。
• 研究条件:中山大学附属第六医院、广州市第一人民医院等15家国内医院参加的临床研究协作项目(NCT01211210)。
• 研究起止时间:2010年6月至2015年2月。
• 研究方法:三臂、多中心、开放、随机的三期临床研究。
• 研究对象:诊断明确的Ⅱ (T3-4/N0)/Ⅲ (T1-4 /N1-2)期直肠腺癌患者, 患者PS评分≤ 1分且有足够的肝肾功能。以下患者需排除:有远处转移, 曾经接受过放疗或化疗, 合并其他肿瘤, 临床明确的心血管及精神疾病。
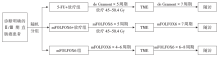
• 干预措施:干预措施流程见图1。
• 评价指标:无病生存期、肿瘤缓解率, pCR、R0切除率、总生存时间、无复发生存率、生活质量和安全性。
患者的手术情况见表1, 三组中, mFOLFOX6+放疗组的患者能进行R0切除的数量最多。
| 表1 手术结果分析 |
术后病理情况见表2, 三组中, mFOLFOX6+放疗组的患者肿瘤退缩最明显, 降期率最高。
| 表2 术后病理反应 |
安全性方面, 几组患者主要的不良反应为白细胞及中性粒细胞减少, 放射性皮炎及放射性肠炎。其中, mFOLFOX6+放疗组的血液学毒性最多, 放射性皮炎及放射性肠炎的发生率也最高。见表3。
| 表3 安全性与依从性 |
mFOLFOX6+放疗作为新辅助治疗比单纯5-FU+放疗有更高的pCR率, 但相对的, 毒性反应也比其他两组增加; 单纯mFOLFOX6作为围手术期化疗的pCR较低。但单纯化疗与5-FU+放疗相比, 肿瘤降期率相似, 且单纯化疗的术后并发症更少。
以FU为基础的新辅助放化疗联合TME及术后辅助化疗是目前局部晚期直肠癌的标准治疗模式, 一直以来在5-FU基础上增加其他细胞毒药物如奥沙利铂, 以提高pCR并改善预后, 是研究的重点。目前国际上已有5项随机对照研究(CAO/ARO/AIO-04、STAR-01、NSAPBR-04、ACCORD 12/0405-Prodige 2、PETACC-6)将5-FU或卡培他滨联合奥沙利铂同步放化疗与单药5-FU或卡培他滨同步放化疗进行对比。然而除了德国CAO/ARO/AIO-04研究外, 其余4项研究均认为奥沙利铂显著增加了不良反应尤其是腹泻的发生率, 且近期疗效pCR没有明显提高, 而远期疗效上长期的随访结果也难以令人满意[1]。因此, 在目前的证据基础上, 奥沙利铂并不被推荐用于局部晚期直肠癌新辅助放化疗中。考虑到中国人群直肠癌的中位发病年龄比欧美国家平均年轻约10岁, 对放化疗的耐受性相对更好, 因此有必要设计针对中国人群的临床研究来探讨奥沙利铂在局部晚期结直肠癌新辅助治疗中的价值。
尽管从最新更新结果来看, FORWARC研究结果提示mFOLFOX6联合放疗与5-FU单药联合放疗相比未改善DFS, 但奥沙利铂的加入明显提高了pCR, 提示这一部分患者对增加强度的新辅助治疗更加有效。随着“ watch and wait” 策略在临床的深入探索, 中国人群中高达27.5%的pCR这一结果令人振奋, 也使得潜在的更多患者将从中获益。当然临床实践中如何挑选这一部分需要增加强度治疗的患者仍有待研究, 是选强烈要求达到病理完全缓解以避免手术的还是肿瘤分期偏晚复发风险高的人群呢?另外, 单纯的mFOLFOX6新辅助化疗与5-FU单药联合放疗相比, 尽管pCR低, 但两组有相似的R0切除率、局部控制率、3年DFS和3年OS(更新数据)[2], 且新辅助化疗组毒副反应及手术并发症相对较低, 由此提示对于部分选择性患者可考虑单纯新辅助化疗方案, 从而避免放疗带来的不良反应。
作为首个在中国人群中开展的局部晚期直肠癌新辅助治疗的大型三期多中心随机对照研究, FORWARC研究样本量大, 设计严谨, 90%以上患者接受了全量放疗, 80%以上患者接受预定设计的术后化疗, 80%患者TME手术质量佳, 因此该研究无论方案设计、项目执行等各个方面都是非常严格, 其结果是可信的。与前期研究不同之处在于FORWARC研究中奥沙利铂采用了标准的化疗剂量(85 mg/m2), 而非以往研究的同步放化疗剂量(50~60 mg/m2), 另外5-FU也是标准的化疗剂量。很显然既往研究中同步放化疗方案中奥沙利铂及5-FU的目的是化疗增敏, 而FORWARC研究中采用足量的化疗最终取得更高的pCR也不难理解。
当然, 任何研究都不可能十全十美。从入组人群上看, 在FORWARC研究中标准淋巴结阳性定义为影像学直径大于1 cm, 但已有研究表明MRI评价仅凭淋巴结大小来判断阳性准确率很低[3], 因此存在判断不准确导致治疗组间不平衡的可能。其次, 从结果看, 与mFOLFOX6联合放疗相比, 5-FU单药联合放疗组中患者新辅助化疗、辅助化疗完成率均相对偏低, 且新辅助治疗中还有1例穿孔及感染, 是否提示该组患者本身基线状态较差的可能。另外, 研究中也没有提供环周切缘、壁外脉管癌栓、病理类型、分化程度、术后详细分期等重要信息, 一定程度上影响了结果的解读。还需要注意的是, 新辅助治疗后mFOLFOX6联合放疗或单药5-FU联合化疗组的阳性淋巴结分别为19.1%和12.6%, 且肿瘤评价长度(4.3 cm), 提示相对于既往研究大部分患者可能相对分期较早。因此需要注意的是, 在临床实践中, 如果要根据该研究结果采取单纯新辅助化疗, 必须明确患者的术前分期, 尤其是局部分期相对偏晚的患者, 去放疗的策略仍值得商榷。
综上所述, FORWARC研究的问世, 为局部晚期直肠癌的新辅助治疗提供了新的策略与方向。mFOLFOX6联合放疗与标准5-FU放化疗相比虽然未改善DFS, 但可获得高pCR, 而单纯的mFOLFOX6新辅助化疗与标准5-FU放化疗相比, 有相似的局部控制率、3年DFS和3年OS, 但毒副反应明显下降。目前也有研究开始探讨增加治疗强度的新辅助治疗后, 再根据肿瘤反应来决定下一步是否行放疗或者手术[4]。当然不管是去放疗还是去手术, 这些研究仅是初步的探索, 在临床实践中一定要结合实际情况, 不可全盘照搬。直肠癌的新辅助治疗仍需要肿瘤专科医生通过多学科团队协作, 结合患者状态及意愿、肿瘤分期、肿瘤反应、病理特征等多方面来综合考量。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|