| 潘崚,1983年毕业于河北医学院医学系,2001年毕业于日本浜松医科大学获得医学博士学位,曾任河北医科大学第二医院血液科科主任、主任医师、教授、硕士及博士研究生导师,河北省医学会血液学专业委员会主任委员。2010年调到四川大学华西医院血液科,现为华西医院血液科教授、主任医师,硕士研究生导师,四川省医学会血液学专业委员会委员;《中华血液学杂志》、《国际输血及血液学杂志》、《白血病·淋巴瘤》、《临床血液学杂志》和《中国输血杂志》等杂志编委。主要研究方向为慢性骨髓增殖性肿瘤和多发性骨髓瘤的诊断与治疗。已培养毕业博士研究生10人、硕士研究生40人,在中英文杂志上发表文章90余篇,主编或参编著作6部。 |
Reviewer's address:Department of Hematology,West China Hospital of Sichuan University,Chengdu 610041,China
Mesa RA, Kiladjian JJ, Catalano JV, et al. SIMPLIFY-1: A phase Ⅲ randomized trial of Momelotinib versus Ruxolitinib in Janus kinase inhibitor-nä ive patients with myelofibrosis[J]. J Clin Oncol, 2017, 35(34): 3844-3850.
1b。
• 芦可替尼(Ruxolitinib)是目前唯一获得美国食品药品监督管理局批准的治疗骨髓纤维化的药物, 对于骨髓增殖性肿瘤(myeloproliferative neoplasm, MPN)患者, 无论是否携带JAK2突变, 芦可替尼在控制症状性脾肿大和全身症状方面均具有较好效果。
• 莫洛替尼(Momelotinib)是一种选择性的小分子JAK1/2抑制剂, 至今尚无莫洛替尼与芦可替尼之间比较的数据, 未明确莫洛替尼在安全性和有效性方面是否优于芦可替尼。
在JAK抑制剂未经治的骨髓纤维化患者中, 比较莫洛替尼与芦可替尼的有效性和安全性。
• 研究条件:127个研究中心参与的国际多中心试验。
• 研究起止时间:2013-12-06至2016-09-12。
• 研究方法:多中心、随机、双盲Ⅲ 期临床试验。
• 研究对象:确诊原发性骨髓纤维化 (WHO标准)或由真性红细胞增多症或原发性血小板增多症继发的骨髓纤维化的患者且未使用过JAK抑制剂, 未行脾切除术或3个月内未行脾脏照射, 年龄大于18岁, 可触及肋缘下大于5 cm的脾肿大。
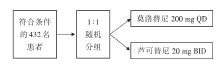
• 干预措施:本研究的流程见图1。
• 评价指标:主要终点指标:脾脏体积在第24周时缩小≥ 基线35%的患者比例(脾脏反应率, spleen response rate, SRR24)。次要终点指标:总症状评分(total symptom score, TSS)反应率(TSS减少大于50%的患者比例); 非红细胞输注依赖率; 红细胞输注依赖率; 红细胞输注率(治疗期间每月输注红细胞单位数)。
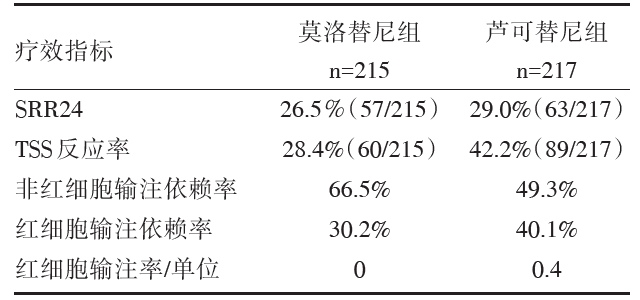
本研究的主要疗效指标见表1。
| 表1 SIMPLIFY-1研究的疗效指标 |
• 对于缩小脾脏体积, 两者非劣效性比例差异为0.09[95%可信区间(confidence interval, CI)0.02~0.16], 双侧95%CI的下限大于0, 莫洛替尼达到非劣效于芦可替尼的主要终点(P=0.011)。
• 对于减小TSS反应率, 非劣效性比例差异为0.00(95%CI -0.08~0.08); 双侧95%CI的下限不大于0, 莫洛替尼未达到非劣效于芦可替尼(P=0.98), 表明与芦可替尼组相比, 莫洛替尼组患者的症状改善无增加。
• 与芦可替尼组相比, 莫洛替尼治疗组在第24周时非红细胞输注依赖率升高(P< 0.001)、输血依赖率较低(P=0.019)、红细胞输注率下降(P< 0.001)。
• 相比芦可替尼组(34.6%), 莫洛替尼组(38.6%)的患者在第24周达到两个或更多预定终点指标(SRR24, TSS反应或非输注依赖)。使用莫洛替尼(10.2%)患者达到三个终点指标的患者比例也高于芦可替尼组(7.8%)。
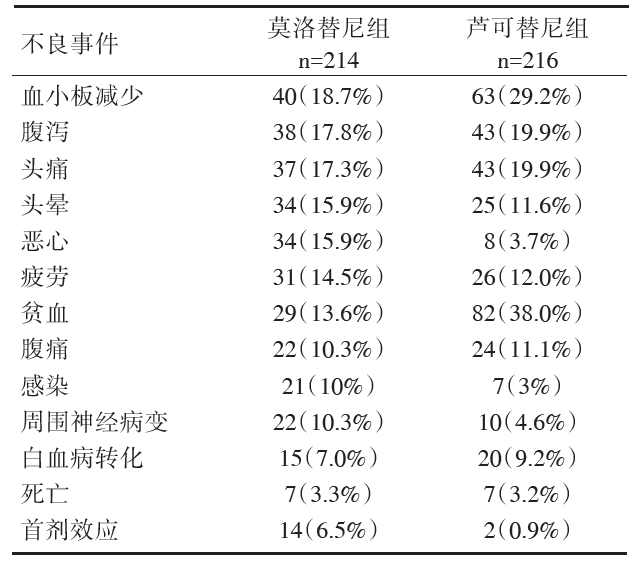
本研究的治疗相关不良事件见表2。
| 表2 SIMPLIFY-1研究的治疗相关不良事件 |
莫洛替尼组、芦可替尼组分别有22.9%、18.1%患者合并严重的血液学不良事件(≥ 3级)。因血液学不良事件而导致停药的患者中, 13.1%患者接受莫洛替尼治疗, 5.6%患者接受芦可替尼治疗。因血液学不良事件而导致研究药物剂量减少或暂时中断治疗的患者中, 17.8%接受莫洛替尼治疗, 36.6%接受芦可替尼治疗。
• 在JAK抑制剂未经治的骨髓纤维化患者24周疗效评估中, 在脾脏反应方面, 莫洛替尼组非劣效于芦可替尼组, 但症状改善方面, 莫洛替尼未到达非劣效性。
• 与芦可替尼组相比, 莫洛替尼组输注需求降低。
骨髓纤维化(myelofibrosis, MF)是一种慢性骨髓增殖性肿瘤, 主要表现为贫血、髓外造血、脾脏肿大, 常有乏力、盗汗、体质量减轻、左上腹胀满等全身症状。约90%的MF患者有JAK2V617F突变或CALR或MPL基因突变, 导致JAK信号通路异常活化, 骨髓纤维组织增生, 正常造血功能受抑[1]。目前已获批用于治疗MF的唯一靶向药物芦可替尼对大部分患者有缩小脾脏、改善全身症状、逆转或稳定MF的疗效, 而不论患者是否有JAK2V617F突变。但芦可替尼治疗过程中会引发或加重贫血、血小板减少, 甚至导致减量或停药。因此寻找治疗效果更好、副作用更小的新型靶向药物势在必行。莫洛替尼是一种口服、小分子、高选择性JAK1/2激酶抑制剂, 一项Ⅰ /Ⅱ 期临床试验数据显示, 莫洛替尼可以使MF患者的脾脏体积缩小, 临床症状改善, 红细胞输注需求减少[2]。
SIMPLIFY-1是一项随机、双盲、对比研究莫洛替尼与芦可替尼治疗JAK激酶抑制剂未经治的MF患者有效性和安全性的Ⅲ 期全球多中心临床试验, 为非劣效性研究。主要研究终点指标是治疗24周时与基线值相比脾脏体积缩小≥ 35%的患者比例, 次要终点指标包括治疗24周时总症状评分(TSS)下降≥ 50%的患者比例、非红细胞输注依赖(治疗的前24周不需要输血并且在前12周没有血红蛋白< 8 g/dL)的患者比例, 红细胞输注依赖(在开始治疗的前8周内输红细胞≥ 4单位或血红蛋白< 8 g/dL)的患者比例, 以及输血率(治疗期间每人每月输注的红细胞单位数)。从2013-12-06至2016-09-12, 全球127个中心共随机纳入432位受试者, 莫洛替尼组215例, 芦可替尼组217例。
本研究有几个非常有意思的发现:(1)治疗24周时, 两组脾脏体积缩小≥ 35%的患者比例相似, 莫洛替尼组26.5%, 芦可替尼组29%, 莫洛替尼的缩脾疗效与芦可替尼达到非劣效性。(2)TSS减少≥ 50%的患者比例莫洛替尼组28.4%, 芦可替尼组42.2%, 莫洛替尼的疗效没有达到与芦可替尼的非劣效性标准, 可能是莫洛替尼和芦可替尼对诱发MF相关症状的细胞因子的抑制作用不同。(3)与芦可替尼相比, 莫洛替尼组患者的输血率、非输血依赖及输血依赖等临床指标有明显改善, 血红蛋白、血清铁和转铁蛋白饱和度等客观指标的改善也优于芦可替尼。这可能与莫洛替尼通过抑制骨形态发生蛋白受体激酶激活素Ⅰ 型受体A(ACVR1)通路、对铁调素产生负调控, 进一步促进网状内皮细胞释放储存铁而增加红系造血有关, 而芦可替尼没有类似作用[3]。(4)莫洛替尼组在改善贫血方面有明显获益, 但芦可替尼组患者的疲乏症状却有明显改善, 提示引起疲乏的原因是多方面的, 而不仅仅是贫血。(5)两组的主要血液学不良事件为贫血和血小板减少, 但与芦可替尼相比, 莫洛替尼组患者较少出现贫血和血小板减少。外周神经病变(peripheral neuropathy, PN)是发生在用药初期的主要非血液学不良事件, 但两组均无患者因PN而停药。莫洛替尼组PN的发生率没有明显高于芦可替尼组。JAK激酶抑制剂导致PN的机制尚不清楚, 亦没有发现可能诱发PN的危险因素。
本研究也有不足之处:(1)没有监测JAK激酶抑制剂的临床疗效与MF驱动基因如JAK2V617F、CALR和MPL的突变状态及突变基因表达水平的相关性, 以及临床疗效与MF预后相关的非表型驱动基因如ASXL1、EZH2、TET2、IDH1/IDH2、SRSF2、SF3B1等的突变状态的相关性; (2)没有监测JAK激酶抑制剂治疗后MF的改善情况; (3)没有监测临床症状评分的变化与MF相关的炎性因子水平变化的相关性。
尽管莫洛替尼改善全身症状的疗效不如芦可替尼好, 但其缩脾的疗效与芦可替尼相当, 并且有改善贫血的潜在优势。考虑到MF临床表现的多样性, 治疗方案应该个体化, 莫洛替尼有望为伴有严重贫血的MF患者提供一种新的治疗选择。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|