| 余科达,复旦大学附属肿瘤医院乳腺外科行政副主任,主任医师,教授,硕士研究生导师,国家自然基金委(NSFC)优秀青年基金获得者。近5年以通讯作者/第一作者在《Nat Commun》、《Sci Adv》、《Cancer Res》、《Clin Cancer Res》、《BMC Med》等国际权威SCI期刊上发表论著30余篇,多篇述评发表于《Nat Rev Cancer》、《J Clin Oncol》等期刊上。据Web of Science 2018统计,论文被引用1 900余次,H指数为23(有23篇论文分别被引用至少23次以上)。担任《Transl Cancer Res》(SCI期刊)副主编、《Cancer Med》(SCI期刊)编委。 中华医学会肿瘤分会乳腺青年学组主任委员,中国抗癌协会乳腺癌专业委员会委员,中国抗癌协会肿瘤靶向治疗专业委员会委员,中国抗癌协会青年理事会理事,中华医学会肿瘤学分会乳腺学组秘书,中国医师协会乳腺外科医师委员会委员,上海市抗癌协会乳腺癌专业委员会常务委员/秘书,上海市抗癌协会乳腺癌青年委员会副主任委员,上海市抗癌协会青年理事会副理事长,上海医学会肿瘤靶分子分会秘书/委员。 |
Reviewer's address:Department of Breast Surgery,Fudan University Shanghai Cancer Hospital,Shanghai 200032,China
Cardoso F, van't Veer LJ, Bogaerts J, et al. 70-gene signature as an aid to treatment decisions in early-stage breast cancer[J]. N Engl J Med, 2016, 375(8):717-729.
1b。
70基因检测(MammaPrint)是来自荷兰癌症研究院的研究者开发的一套乳腺癌多基因检测系统, 在5年和10年远处复发风险基础上, 根据基因表达与临床结果的相关性, 将患者分为预后良好组及预后不良组, 并且已有多项回顾性研究证实了MammaPrint 70基因检测对早期乳腺癌患者预后的预测作用。但目前尚缺乏前瞻性评价MammaPrint 70基因检测对化疗决策影响的临床试验。
本研究旨在探索MammaPrint 70基因检测能否作为临床决定早期乳腺癌患者是否需要接受化疗的指标。
• 研究条件: 欧洲癌症研究与治疗联盟等多个机构临床试验注册项目(ClinicalTrials.gov number, NCT00433589; EudraCT number, 2005-002625-31)。
• 研究起止时间:2007-2011年。
• 研究方法:多中心, Ⅲ 期, 随机对照临床试验。
• 研究对象:淋巴结0~3枚转移的早期浸润性乳腺癌患者6 693名。年龄18~70岁, 确诊为早期浸润性乳腺癌的患者(T1或T2或可行手术治疗的T3), 伴有0~3个淋巴结转移, 但无远处转移。
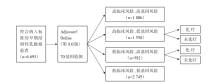
• 干预措施:对临床风险(基于改良的Adjuvant!Online工具)和基因风险(基于MammaPrint)不一致的患者(高临床风险、低基因风险的患者或低临床风险、高基因风险的患者)随机进行辅助化疗或不化疗。由于两种检测结果提示高风险的患者应接受辅助化疗。被指定接受辅助化疗的患者可以被随机分配接受含蒽环类药物方案或多西紫杉醇/卡培他滨治疗方案。具有激素受体阳性的乳腺癌患者可以进一步随机分配接受他莫昔芬联合来曲唑方案或单药来曲唑治疗方案。见图1。
• 评价指标:5年无远处转移生存率。
本研究共入组6 693名患者, 高临床风险、高基因风险的患者1 806名, 低临床风险、低基因风险的患者2 745名, 高临床风险、低基因风险的患者1 550名, 低临床风险、高基因风险的患者592名, 随访时间5年。
其中1 550名(23.2%)被认为是具有高临床风险、低基因风险的患者中, 未接受化疗患者的5年无远处转移生存率为94.7%(95%可信区间92.5%~96.2%), 这些患者的5年无远处转移生存率比接受化疗的患者低1.5%(校正后风险比=0.78, P=0.27)。
根据MammaPrint检测结果选择是否接受辅助化疗不能为临床风险低的患者提供临床获益; 临床风险高的患者MammaPrint的检测判定低复发风险而不接受化疗降低了1.5%的5年疾病控制获益, 提示低基因风险的患者可以免除化疗。
当前, 随着乳腺癌基因表达谱工具日趋成熟, 一些工具进入前瞻性验证试验, 其中OncotypeDX和MammaPrint是最引人注目的两款工具。本研究即是以MammaPrint为研究主体的MINDACT试验的部分重要结果报道, 显示:(1)基本上所有低临床风险(无所谓基因低风险还是高风险)的乳腺癌都不再需要化疗; (2)高临床风险、低基因风险乳腺癌中也有将近46%的患者可能不需要化疗。
本研究具有重要临床指导价值, 凸显了基因检测所带来的重大影响, 开辟了一条对约50%所谓临床高危患者免除化疗的可行道路。临床医生在判断乳腺癌预后时, 多将肿瘤大小、淋巴结转移状态、组织学分级、激素状态、HER2状态等因素纳入考量, 而MammaPrint希望独立于上述肿瘤临床病理因素, 从基因组水平判断肿瘤复发转移的可能性, 希望最终遴选出化疗不获益的患者, 做化疗减法。
MINDACT研究结果体现了精准治疗理念。精准治疗时代, 追求疗效更高、毒性更低。MINDACT试验整体上设计合理, 结论可靠, 适合临床借鉴。其意向性治疗人群分析中, 高临床风险、低基因风险亚组中, 化疗者5年无远处转移生存率为95.9%, 仅比观察组患者的94.4%高出1.5%, 校正后风险比=0.78, P=0.27, 提示“ 基因工具可逆转高危临床风险” 的补充价值。而低临床风险、高基因风险亚组中, 化疗者5年无远处转移生存率为95.8%, 略微高于观察组的95.0%, 校正后HR=1.17, P=0.66, 也体现出“ 临床低危状态具有先决作用” 的经典价值。当临床风险和基因风险不一致时, 化不化疗对患者的无病生存期和总生存期似乎影响不大。
但本研究的一些细节和不足也值得我们斟酌和推敲:
第一, 本研究入组时无所谓激素受体状态和HER2状态。随着肿瘤分子分型时代的开启, 我们越来越关注激素受体阳性和HER2阴性的Luminal型患者免除化疗的可能性。本研究入组人群中, 激素受体阳性患者高达88%, HER2阴性高达90%, 提示本研究结论主要适用于激素受体阳性、HER2阴性患者; 而对HER2阳性和三阴性患者亚组, 结论推行要慎重。
第二, 本研究所谓的“ 临床危险” 分层, 是基于改良的Adjuvant! Online工具, 里面包含激素受体状态、HER2状态、淋巴结状态、肿瘤大小及组织学分级, 但并没有纳入癌栓、年龄等因素, 因此所谓“ 低危” 或“ 高危” 是一种群体性情况, 当遇到个体时, 一定要个体化分析。例如, 按MINDACT设计, “ ER阳性、HER2阴性、2 cm、Ⅰ 级、淋巴结3枚转移” 归类为“ 低危” (参见试验的附加Supplementary Appendix文件), 但是若再加上年龄30岁、癌栓阳性, 相信大多数医生会判定这是一个风险并不低的患者。因此, 具体问题、具体分析, 不能机械地理解和分类高低危。
第三, 在试验阶段, MammaPrint采用新鲜液氮冻存组织用于基因mRNA检测, 而在实际临床实践中, 基本以蜡块为主, 想把MammaPrint的结论推广应用, 首先要解决检测方法优化, 处理好蜡块标本与新鲜标本间检测数据的一致性等质控问题。
第四, 未化疗组生存那么好, 似乎也有治疗原因。通过细读研究方案, 我们发现, 所有入组的激素受体阳性患者, 均接受了长达7年的内分泌治疗(2年他莫昔芬加5年来曲唑, 或者7年来曲唑, 绝经前患者同期卵巢功能抑制), 这是非常极端而长期的内分泌治疗方法, 即便放在今天, 对低危患者不加区分地采用7年卵巢功能抑制联合芳香化酶抑制剂, 也会遭人诟病。因此, 研究中化疗组与未化疗组相差不大, 一个潜在解释是未化疗组的内分泌治疗太强大且长期了。而在现实世界中, 我们真的能一律采用7年强化内分泌治疗吗?恐怕未必, 那么未化疗组效果可能会因此而打折扣吗?有可能。
综上, 通过应用MammaPrint, 可能使高临床风险、低基因风险乳腺癌患者中有将近46%可能不再需要化疗, 但同时我们也要慎重对待免于化疗人群, 精准评估其肿瘤特性是否很“ Luminal” , 内分泌治疗是否敏感而充分。我们既要改变治疗过度的现实, 也要防止治疗不足的危机。