| 康晓征,北京大学肿瘤医院胸外一科副主任医师,副教授。中国临床肿瘤学会CSCO青年专家委员会秘书、肺癌学组青年委员,中国抗癌协会CACA食管癌专业委员会青年委员,北京医学会胸外科分会青年委员,中国研究型医院学会胸外科分会常务委员。美国胸外科学会STS会员,美国临床肿瘤学会ASCO会员,美国癌症研究协会AACR会员,欧洲胸外科学会ESTS会员。美国杜克大学医学中心、癌症中心访问学者。2016年北京市优秀人才培养资助青年骨干。主要致力于肺癌、食管癌、肺转移瘤的围术期综合治疗及相关临床转化医学研究。 |
Soria JC, Ohe Y, Vansteenkiste J, et al. Osimertinib in untreated EGFR-mutated advanced non-small-cell lung cancer[J]. N Engl J Med, 2018, 378(2):113-125.
1b。
• 晚期非小细胞肺癌(non-small cell lung cancer, NSCLC)患者携带表皮生长因子受体(epidermal growth factor receptor, EGFR)基因突变可从一代或二代EGFR酪氨酸激酶抑制剂(tyrosine kinase inhibitor, TKI), 例如厄洛替尼、吉非替尼或阿法替尼的药物治疗中获得生存获益并且疗效优于全身化疗, 因此EGFR-TKI已成为此类患者的一线治疗方案。
• 既往研究发现在超过50%的一线EGFR-TKI治疗失败的患者中检测到T790M基因突变。AURA研究(Ⅰ 期研究)提示, 奥希替尼作为第三代EGFR-TKI药物可有效改善EGFR T790M突变患者的预后, 并且血脑屏障通透效力及中枢神经系统(central nervous system, CNS)疾病控制疗效均优于以铂类为基础的双药联合化疗方案。
• 奥希替尼同标准EGFR-TKI治疗方案(厄洛替尼/吉非替尼)在初治型EGFR敏感突变的NSCLC患者疗效比较结果尚不明确。
评估奥希替尼治疗初治型EGFR敏感突变的晚期NSCLC的疗效是否优于标准一线EGFR-TKI(厄洛替尼/吉非替尼)方案。
• 研究条件:全球29个国家共计132个中心参与的FLAURA研究(NCT02296125)。
• 研究起止时间:2014年12月至2016年3月。
• 研究方案:多中心、双盲、随机对照、Ⅲ 期临床研究。
• 研究对象:初治型携带EGFR敏感突变(exon19del/exon21L858R)的局部晚期或晚期NSCLC患者; 若存在CNS转移灶, 则要求神经系统症状稳定。
• 干预措施:随机接受奥希替尼或一代TKI治疗方案(厄洛替尼/吉非替尼), 具体流程见图1。根据 RECIST 1.1标准每6周评估疗效直到疾病进展。
• 评价指标:主要终点指标为无进展生存期(progression-free survival, PFS)。次要终点指标:毒副反应, 总生存期(overall survival, OS), 客观缓解率(objective response rate, ORR), 药物反应期, 疾病控制率, 药物反应深度及安全性。
共入组556名患者, 结果表明奥希替尼一线治疗方案的疗效优于标准一代TKI(厄洛替尼/吉非替尼)治疗方案, 且毒副事件发生率较低。
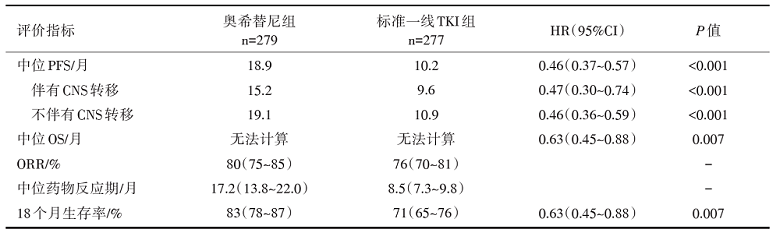
奥希替尼组中位PFS明显优于标准TKI治疗组[18.9 个月vs. 10.2个月, 风险比(hazard ratio, HR)=0.46, P< 0.001, 95%可信区间(confidence interval, CI)0.37~0.57], OS数据尚未成熟。ORR在两组间无明显差异(80% vs. 76%)。见表1。
| 表1 FLAURA研究的主要疗效结果 |
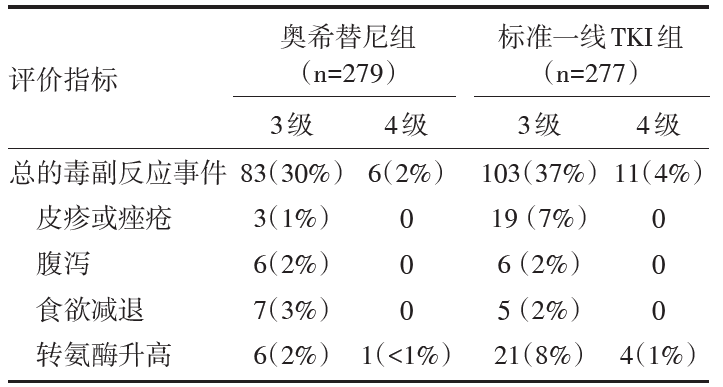
在主要毒副反应方面, 奥希替尼组的3/4级不良事件发生率明显低于标准一线TKI治疗方案。见表2。
| 表2 FLAURA研究的主要3/4级毒副反应 |
对于携带EGFR敏感突变的局部晚期或转移性NSCLC患者, 一线使用奥希替尼疗效优于标准EGFR-TKI方案。并且, 奥希替尼降低了严重治疗相关毒副反应发生的概率。
近年来靶向治疗在晚期NSCLC治疗领域可谓风起云涌、百舸争流, 兼顾有效性及安全性的EGFR-TKI药物不断推陈出新, 成为EGFR突变型晚期NSCLC患者的福祉。在FLAURA研究结果公布之前, EGFR突变型晚期NSCLC患者的一线标准方案为一代或二代EGFR-TKI, 然而所有患者不可避免地会发生耐药, 耐药后约50%患者出现EGFR T790M突变。三代EGFR-TKI代表药物奥希替尼可以选择性作用于EGFR敏感突变(19外显子缺失及21外显子L858R)同时也能克服T790M突变。Ⅲ 期AURA3研究结果表明奥希替尼治疗T790M阳性晚期NSCLC患者的PFS及ORR均优于顺铂联合培美曲塞化疗方案, 并且安全性更优[1]。Ⅰ 期AURA研究提示奥希替尼可能成为EGFR敏感突变晚期NSCLC患者的一线治疗方案, 80 mg及160 mg剂量对应的ORR分别为67%及87%, 中位PFS分别为22.1个月及19.3个月[2]。基于令人兴奋的前期结果, Ⅲ 期FLAURA研究选择80 mg药物剂量以明确奥希替尼作为一线治疗是否改善EGFR敏感突变晚期NSCLC患者的PFS。
FLAURA研究对共计556例EGFR敏感突变的晚期NSCLC患者进行随机分组, 将奥希替尼与标准一代EGFR-TKI进行疗效比较, 结果表明奥希替尼显著延长了PFS(18.9个月vs. 10.2个月, HR 0.46, 95%CI 0.37~0.57, P< 0.001), 将疾病进展或死亡风险降低了54%[3]。此生存优势贯穿各亚组, 其中也包括有CNS转移的患者[3]。尽管研究截止时仍有25%的终点事件尚未发生, 奥希替尼组的OS优势未达到统计学意义, 但是鉴于约半数标准一代EGFR-TKI治疗组患者疾病进展时将因T790M突变而被交叉入组到奥希替尼组, 因此其反转效应是可期的。值得注意的还有, 尽管药物暴露时间更久, 然而奥希替尼组3级以上药物不良反应发生率及治疗中止率更低。
进一步分析FLAURA研究的结果。首先, 对EGFR敏感突变型晚期NSCLC最佳治疗方案(三代 vs. 一代序贯三代)需要重新思考。一线奥希替尼组的中位PFS为18.9个月, 一代EGFR-TKI组的中位PFS 为10.2个月[2], 若与AURA3研究[1]中耐药后改换奥希替尼治疗的中位PFS 10.1个月相加, 则一代EGFR-TKI序贯奥希替尼治疗的中位PFS达到20.3个月。乍一看两种治疗策略的PFS相近, 然而需要指出的是, AURA3研究中仅40%患者(419/1 036)经筛选确认存在T790M突变方可随机入组, 因此可以推测一线奥希替尼治疗可能使更多EGFR突变型NSCLC患者获益。其次, 从临床实践角度看, 二线奥希替尼药物治疗的前提条件需要确认T790M突变, 这意味着患者疾病进展后需要重新组织活检或血液检测。第三, 有创性活检对于相关并发症高危患者而言, 需要谨慎选择; 血浆循环肿瘤DNA(circulating tumor DNA, ctDNA)检测也面临假阴性结果的风险。部分携带T790M突变的患者可能由于上述原因会失去奥希替尼治疗机会, 进而影响预后。因此, 一线奥希替尼治疗更加符合临床实践操作, 避免再次活检问题。第四, CNS转移问题始终困扰一代EGFR-TKI治疗[4]。FLAURA研究结果表明, 无论是否存在CNS转移, 奥希替尼治疗的PFS均更优(转移者及非转移者的 HR分别为0.47和0.46), 并且同一代EGFR-TKI相比CNS疾病进展率更低(6% vs. 15%)[2]。评价奥希替尼治疗EGFR突变型NSCLC脑膜转移的BLOOM研究结果表明, 经过160 mg大剂量用药6个月, 共计32例患者中10例获得影像学评估缓解, 13例疾病稳定[5]。对于包括脑膜转移在内的CNS转移患者可能更适合一线奥希替尼治疗。最后, 明确奥希替尼耐药机制将为进一步优化EGFR突变型NSCLC一线治疗策略提供更多思路。目前已知EGFR基因20外显子C797S突变是最常见的奥希替尼耐药机制[6], HER2及MET基因扩增也影响奥希替尼的药效[7]。较之一代或二代EGFR-TKI药物, 奥希替尼耐药机制也对预后产生更加深远的影响。近期发表的FLAURA研究中疾病进展后的结果表明, 一线奥希替尼治疗后并未引发肿瘤生物学行为恶化, 并且未发现快速进展病例[8]。
未来EGFR突变型NSCLC治疗的发展方向, 一方面需要继续探索一线治疗的“ 黑马” , 兼顾有效性及安全性; 另一方面则需要对现有药物选择进行合理配置, 兼顾药物可及性与经济性。期待着FLAURA研究OS数据成熟, 期待更多奥希替尼药物相关随机对照研究证据补充, 给当前种种疑问一个明确答案。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|