作者简介:
田照(1990-),男,湖北恩施人,在读硕士研究生,研究方向为中医、民族医学防治筋骨病及骨肿瘤。
目的 探讨奥沙利铂联合卡培他滨治疗食管癌的临床疗效及安全性,为奥沙利铂超说明书适应证用于食管癌提供临床用药参考。方法 通过计算机检索PubMed、Cochrane 图书馆、中国期刊全文数据库、中国科技期刊全文数据库和万方数字化期刊全文库自建库到2018年5月公开发表的关于奥沙利铂与卡培他滨联合用药治疗食管癌的研究,应用RevMan 5.3软件进行数据分析。研究人群为食管癌或胃食管交界处癌患者。干预措施:治疗组以奥沙利铂、卡培他滨结合放疗,不含其他药物;对照组为其他药物、卡培他滨;可结合放疗等基础疗法,且两组一致;临床疗效结局指标为客观有效率、疾病控制率;安全性结局指标为白细胞减少率、血小板减少率及恶心呕吐发生率,并分别以优势比及其95%可信区间作为效应量对结局指标进行比较。结果 共检索到符合纳入标准的文献11篇(n=999)进行Meta分析,纳入的文献偏倚风险较小。Meta分析结果显示:①奥沙利铂联合卡培他滨结合放疗治疗食管癌的客观有效率(优势比=2.31,95%可信区间1.75~3.05, P<0.000 01)、疾病控制率(优势比=1.61,95%可信区间1.16~2.23, P=0.004)及生存率(优势比=2.64,95%可信区间1.86~3.75, P<0.000 01)明显优于与其他药物或卡培他滨结合放疗;②奥沙利铂联用卡培他滨结合放疗治疗食管癌的白细胞减少率(优势比=1.55,95%可信区间1.13~2.13, P<0.006)高于其他药物或卡培他滨结合放疗;血小板减少率与对照组相比无显著性差异;恶心呕吐发生率(优势比=2.07,95%可信区间1.47~2.90, P<0.000 1)高于其他药物或卡培他滨结合放疗。结论 奥沙利铂联合卡培他滨结合放疗治疗食管癌的客观有效率、疾病控制率及生存率优于其他药物或卡培他滨结合放疗,临床可以优先考虑奥沙利铂联合卡培他滨结合放疗以提高疗效。
Objective To perform a meta-analysis in the clinical efficacy and safety of the therapy protocols and provide a large data demonstration for esophageal cancer(EC)by Oxaliplatin out of instructions combined with Capecitabine.Methods Researching PubMed, the Cochrane library, CNKI, VIP and Wangfang data et al, domestic and overseas published documents about Oxaliplatin combined with Capecitabine in treatment of EC collected by us from building date library to May 2018 and RevMan 5.3 was applied to data analysis. The patients were who got EC or gastro-oesophageal junction cancer. Using Oxaliplatin and Capecitabine is experiment group without other medicines, other medicine or Capecitabine are contral group. The clinical efficacy index are disease control rate (DCR), overall response rate (ORR) and survival rate. The safety index are occurrence of leukocytopenia, thrombocytopenia, nausea and vomiting. The OR and the 95% confidence interval (CI) was calculated to estimate outcome index from each group.Results Eleven literatures were analyzed in the meta-analysis and showed lower bias risk. ①DCR, ORR and survival rate in treatment of EC by Oxaliplatin combined with Capecitabine showed better than the control group(ORR:OR=2.31,95%CI 1.75~3.05, P<0.000 01; DCR: OR=1.61,95%CI 1.16~2.23, P=0.004; Survival rate: OR=2.64,95%CI 1.86~3.75, P<0.000 01). ②The leukocytopenia in treatment of EC by Oxaliplatin combined with Capecitabine is higher than the control group(OR=1.55,95%CI 1.13~2.13, P<0.006). The thrombocytopenia in treatment of EC by Oxaliplatin combined with Capecitabine showed no significant statistical differences. Occurrence of nausea and vomiting in treatment of EC by Oxaliplatin combined with Capecitabine showed clearly higher than the control group with other medicine or Capecitabine(OR=2.07,95%CI 1.47~2.90, P<0.000 1).Conclusions DCR, ORR and survival rate in treatment of EC by Oxaliplatin combined with Capecitabine showed better than the control group with other medicine or Capecitabine. This programme could be consided as the priority in order to improve clinical efficacy.
食管癌(esophageal cancer, EC)是较常见的恶性肿瘤, 是第六大癌症主要死亡原因[1]。其常规治疗方法为围手术期进行放化疗[2]。目前尚未形成统一的放化疗标准, 据美国一项慢性转移性疾病的研究显示, 联合化疗方案比单药化疗方案具有更好的疗效, 且耐受力更好[3, 4], 国内多数专家认为:顺铂+5-氟尿嘧啶(Cisplatin+Fluoracil, DDP+5-FU)是目前EC联合化疗的标准方案[5]。在欧洲地区常用的化疗组合有阿霉素+顺铂+5-氟尿嘧啶输注(Doxorubicin+Cisplatin+Fluoracil, ECF)方案、多西紫杉醇+奥沙利铂+卡培他滨(Docetaxel+ Oxaliplatin+Capecitabine, TEX)方案等[6]。卡培他滨作为新型靶向抗肿瘤药物, 经肿瘤胸腺嘧啶磷酸化酶(TP酶)转化为5- FU在癌细胞中选择性激活并释放, 临床疗效较好, 毒性相对较低[7]。奥沙利铂作为第三代含铂化合物, 能间接抑制DNA复制和转录, 已被证实对部分癌症有效, 而毒副反应相对更小[8]。虽然奥沙利铂的说明书适应证主要是直肠癌和部分结肠癌 , 但临床已有报道奥沙利铂超适应证联合卡培他滨结合放疗用于EC, 此组合的客观疗效和安全性是否合理还有待评价。因此本研究采用系统评价的分析方法, 为奥沙利铂联合卡培他滨结合放疗治疗EC提供临床证据, 同时为奥沙利铂寻找更广泛的适应证及EC的临床治疗提供多方位的参考。
通过计算机检索Cochrane 图书馆(2018年第5期)、PubMed、CNKI、VIP和Wangfang 数据库, 检索时间均从建库到2018年5月, 检索语种仅限中文和英文。
按照PICOS策略制定检索式, 中文包括奥沙利铂、卡培他滨、希达罗、食管癌, 如CNKI检索式为:AB=(‘ 奥沙利铂’ )AND AB=(‘ 卡培他滨’ +‘ 希达罗’ ) AND TI=‘ 食管癌’ ; WangFang 数据库检索式为:题名或关键词:(奥沙利铂)* 题名或关键词:(卡培他滨+希达罗)* 题名或关键词:(食管癌); VIP检索式为:(M=奥沙利铂+M=草酸铂)* (M=卡培他滨+M=希罗达)* (M=食管癌)。
英文检索词包括esophageal cancer、carcinoma of esophagus、esophageal carcinoma、esophagus cancer、capecitabine、xelodo、oxaliplatin、L-OHP。所有检索采取主题检索和自由检索相结合的方式, 并根据具体数据库调整检索策略, 以PubMed为例, 其具体检索策略如下:
#1 esophageal cancer [Title/Abstract]
#2 carcinoma of esophagus [Title/Abstract]
#3 esophageal carcinoma [Title/Abstract]
#4 esophagus cancer [Title/Abstract]
#5 #1 OR #2 OR #3 OR #4
#6 capecitabine[Title/Abstract]
#7 xelodo[Title/Abstract]
#8 #6 OR #7
#9 oxaliplatin[Title/Abstract]
#10 L-OHP[Title/Abstract]
#11 #9 OR#10 #14 #5 AND #8 AND #11
为避免漏查文献, 对入选资料的参考文献进行二次检索, 并手工检索相关刊物, 用Google scholar搜索引擎在互联网寻求相关资料。
1.2.1 纳入标准
(1)研究设计:关于奥沙利铂联合卡培他滨治疗食管癌的随机对照试验、半随机对照试验、临床试验。
(2)研究对象:诊断标准符合2016 NCCN临床实践指南《食道癌和胃食管交界处癌》及EMSO指南《Oesophageal cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up》, 经病理组织学及细胞学检查确诊为食管癌病变患者。
(3)干预措施:治疗组为奥沙利铂联合卡培他滨, 不含其他药物; 对照组为其他药物、卡培他滨。可结合放疗等基础疗法, 且两组一致。
(4)结局指标:疗效指标客观疗效按 WHO 实体瘤近期客观疗效评价指南(1981 年), 分为完全缓解(complete response, CR)、部分缓解(partial response, PR)、疾病稳定(stable diseasse, SD)和疾病进展(progressive disease, PD), 以CR+PR 计算有效率, 包括客观有效率、疾病控制率、生存率; 安全性指标包括白细胞减少率、血小板减少率、恶心呕吐发生率等。
1.2.2 排除标准
(1)回顾性研究及硕士、博士研究生学位论文等; (2)文献质量较差; (3)研究对象及干预措施不符合入选标准; (4)提供数据不完整。
文献质量按照Cochrane 手册推荐的随机对照研究质量评价标准的偏倚风险评估工具进行判定。
两位研究人员独立进行资料提取和数据整合, 交叉对比。首先根据检索出的题目、摘要筛选出明显不合格的文献, 再次阅读筛选未确定资料。遇到任何分歧或争议双方协商讨论解决, 或提交第三位评价员讨论解决。
按循证医学要求整理数据, 建立数据库并核准合成。本研究的疗效指标和安全性指标分析均采用优势比(odds ratio, OR)及其95%可信区间(confidence interval, CI)为效应统计量; 统计学异质性检验采用Q统计量的I2检验分析。有异质性时采用随机效应模型合并数据, 用敏感性分析和亚组分析导致明显异质性的原因; 异质性过大则采用专用描述分析。所有统计分析均使用RevMan 5.3软件完成。
依据检索策略, 共检索到相关文献102篇, 其中中文文献76篇, 英文文献25篇。剔除重名文献57篇, 获得相关文献45篇, 其中中文文献29篇, 英文文献16篇。通过阅读题目和摘要, 剔除雷同文献2篇, 获得相关文献43篇, 其中中文文献27篇, 英文文献16篇。通过阅读全文剔除诊断标准、数据和结局指标不符合要求文献32篇, 最终纳入研究文献11篇。筛选流程见图1。
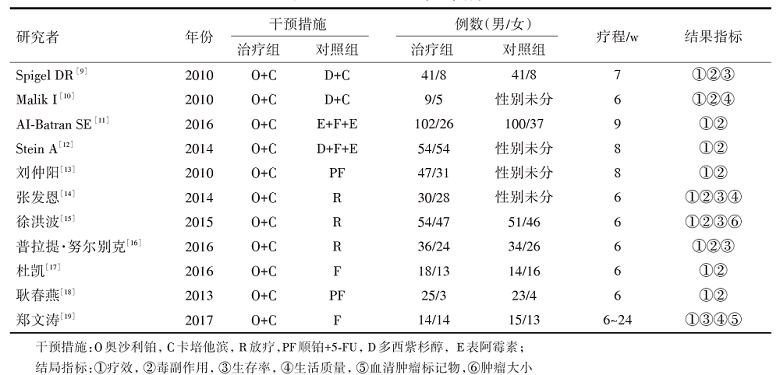
纳入的11篇文献中有10篇提到随机, 但未具体说明方法, 11篇研究均未提及盲法, 8篇提及退出与失访。文献样本最多265例, 最少14例; 疗程最长24周, 最短4周。治疗组均为奥沙利铂联合卡培他滨, 对照组用其他单药或卡培他滨联合放疗。纳入文献的基本特征信息见表1。
| 表1 纳入研究文献的基本特征 |
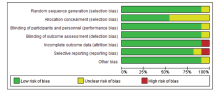
文献质量按照Cochrane5.2手册推荐的随机对照研究的质量评价标准进行偏倚风险评价, 结果见图2、图3。
2.3.1 客观有效率分析
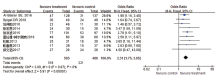
文献[9, 11, 13, 14, 15, 16, 17, 18, 19]报道了奥沙利铂联合卡培他滨治疗EC的客观有效率, 异质性检验显示, P=0.87, I2=0< 50%, 具有同质性, 用固定效应模型。Meta分析结果显示, OR=2.31, 95%CI 1.75~3.05, P< 0.000 01。说明奥沙利铂联合卡培他滨治疗EC的疗效较优, 差异有统计学意义, 见图4。
2.3.2 疾病控制率分析
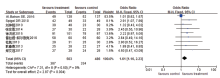
文献[9, 11, 13, 14, 15, 16, 17, 18, 19]报告了奥沙利铂联合卡培他滨治疗EC的疾病控制率, 将CR+PR+SD作为疾病控制率的有效统计量, 进行Meta分析, 异质性检验显示, P=0.50, I2=0< 50%, 可用固定效应模型, OR=1.61, 95%CI 1.16~2.23, Z=2.87, P=0.004。说明奥沙利铂联合卡培他滨治疗EC疾病控制率优于对照组, 见图5。
2.3.3 生存率分析
文献[9, 14, 15, 16, 19]报告了奥沙利铂联合卡培他滨治疗EC的2年生存率数据, 异质性检验显示, P=0.24, I2=28%< 50%, 固定效应模型分析得出OR=1.69, 95%CI 1.39~2.06, P< 0.000 01。说明奥沙利铂联合卡培他滨治疗EC的生存率优于对照组, 见图6。
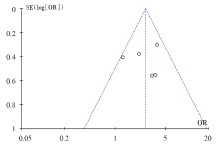
生存率是EC治疗疗效评价的重要指标, 为检测其发表偏倚, 做了漏斗图, 可见图形基本对称, 呈倒漏斗形, 说明纳入文献发表偏倚较小, 见图7。
2.4.1 白细胞减少率分析
文献[9, 10, 11, 12, 13, 14, 15, 17, 18]报告了白细胞减少率数据, 异质性检验显示, P=0.007, I2=64, 说明具有异质性, 采用随机效应模型, 合并效应量OR=1.26, 95%CI 0.94~1.69, Z=1.55, P=0.12, 差异无统计学意义。
由于奥沙利铂联合卡培他滨治疗EC的白细胞减少率分析时具有异质性, 故为了寻找产生异质性的原因, 进行敏感性分析, 去除1篇质量较低的文献[13], 再次对文献[9, 10, 11, 12, 13, 14, 15, 17]进行统计, 异质性检验显示, P=0.59, I2=0< 50%, 具有同质性, 用固定效应模型分析, OR=1.55, 95%CI 1.13~2.13, P< 0.006。说明奥沙利铂联合卡培他滨治疗EC白细胞减少率大于对照组。见图8。
2.4.2 血小板减少率分析
文献[9, 11, 13, 14, 15, 17, 18]报告了血小板减少率数据, 异质性检验显示, P=0.000 01, I2=88%, 存在较大异质性, 用随机效应模型, 合并效应量OR=0.71, 95%CI 0.51~1.0, 差异无统计学意义。提示治疗组血小板减少率与对照组无显著性差异。
由于奥沙利铂联合卡培他滨治疗EC的血小板减少率统计具有明显异质性, 为寻求原因, 进行亚组分析。以疗程大于等于8周和小于8周分为两个亚组, 大于等于8周的文献[10, 12, 14, 15]异质性检验显示, I2=92%, 有明显异质性, 用随机效应模型, 菱形跨过垂线两侧, 说明奥沙利铂联合卡培他滨治疗EC疗程大于等于8周时血小板减少率与对照组无显著差异(P=0.89), 见图9。
对小于8周的文献[15, 17, 18]异质性检验显示, I2=44%< 50%, 无实质性异质性, 用随机效应模型, OR=1.25, 95%CI 0.38~4.07, 菱形跨过垂线两侧, 说明奥沙利铂联合卡培他滨治疗EC疗程小于8周时血小板减少率与对照组无显著差异(P=0.72), 结果见图10。
2.4.3 恶心/呕吐发生率
文献[9, 10, 11, 14, 15, 16, 17, 19]报告了治疗前后恶心呕吐数据, 异质性检验显示, P=0.09, I2=44%< 50%, 具有同质性, 用固定效应模型, 合并效应量OR=2.07, 95%CI 1.47~2.90, P< 0.000 1, 说明奥沙利铂联合卡培他滨治疗食管癌的恶心呕吐发生率高于对照组, 见图11。
EC作为恶性肿瘤之一, 开放性根治术易产生肺功能损害、感染等多种并发症, 严重影响患者生存时间和生活质量。探寻疗效可靠且副作用小的保守治疗方法仍是EC领域的难题[20]。研究显示, 北美地区EC方案的5年生存率约为20.6%, 和我国20.9%大致相当, EC患者生存时间与选择的治疗方式有密切关系[21]。目前EC的主要治疗方式是围手术期放化疗, FU方案是公认的化疗方案, 但其不良反应较突出[4]。奥沙利铂虽是用于治疗转移性直肠癌和原发肿瘤完全切除后的Ⅲ 期结肠癌, 但其超说明书适应证联合卡培他滨结合放疗治疗EC的合理性有待评价。本研究从临床疗效和安全性进行系统评价以期为此方案的临床运用提供数据支撑。
本研究显示, 奥沙利铂联合卡培他滨结合放疗治疗EC的客观有效率(OR=2.31, 95%CI 1.75~3.05)、疾病控制率(OR=1.61, 95%CI 1.16~2.23)明显优于与其他药物或卡培他滨结合放疗。从临床疗效分析, 奥沙利铂联合卡培他滨结合放疗效果确切, 可作为EC的治疗方案。奥沙利铂联合卡培他滨结合放疗治疗EC生存率(OR=1.69, 95%CI 1.39~2.06)明显优于对照组, 能在一定程度上延长患者的生存时间, 故奥沙利铂联合卡培他滨结合放疗可作为EC治疗的重点参考方案。奥沙利铂联合卡培他滨结合放疗治疗EC的白细胞减少率(OR=1.55, 95%CI 1.13~2.13)及恶心呕吐发生率(OR=2.07, 95%CI 1.47~2.90)稍高于其他药物或卡培他滨结合放疗。从临床安全性分析看, 对于易发生白细胞减少和恶心呕吐的患者应慎用奥沙利铂联合卡培他滨结合放疗的方案。血小板减少率亚组分析显示大于等于8周亚组血小板减少率与对照组无明显性差异, P> 0.05, 疗程小于8周时奥沙利铂联合卡培他滨治疗EC的血小板减少率对照组无明显性差异, P> 0.05。每一种EC治疗方案的安全性均需从神经、呼吸、胃肠、骨骼等多个系统予以评价。本研究因数据有限, 仅此抛砖引玉, 期待广大学者不断挖掘相关数据予以充实。
本研究按循证医学原则、方法及要求进行系统评价, 纳入的中英文文献数量较均衡, 质量相对较高, Meta分析显示未见明显发表偏倚, 数据和结论有一定可靠性, 由于国内外研究的给药剂量、方式、地域差别等诸多因素会对结果产生一定影响, 所以期待更大样本量、更全面的分析研究。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|