[编者按] 疾病的正确诊断和合理治疗是患者和医务工作者共同的心愿。在广东省人民医院肿瘤中心, 吴一龙教授指导临床医生应用循证医学理论进行肿瘤的多学科综合治疗, 开展临床病例讨论。讨论会上各学科共同围绕一个病例或一个病种进行会诊, 临床、病理、B超、放射影像等资料齐全, 除相关科室提前准备的中心性发言外, 到会人员各抒己见, 气氛热烈。参会人员受益匪浅, 提高了对疑难病例的诊治水平。为了将他们的诊治经验传播出去, 让更多的临床医生获益, 我刊开辟“ 循证病例讨论” 栏目, 希望广大医务工作者关注此栏目。
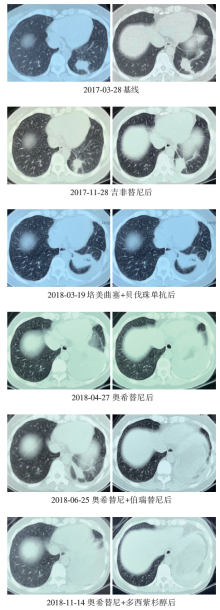
患者, 女性, 43岁, 从不吸烟。无肿瘤家族史, 体能评分(performance status, PS)=1分。2017-03-28因“ 腰部疼痛2个月” 入院。患者2017年1月摔倒后出现腰部疼痛, 2017-03-27外院CT示:左下肺肿块, 考虑周围型肺癌; MRI示:多发椎体骨质破坏。2017-03-31我院行CT引导下经皮肺穿刺活检术, 病理显示左下肺浸润性腺癌, 基因检测示:EGFR 19del(ARMS法)。确诊为左下肺周围型腺癌cT2N1M1c(多发椎体骨)Ⅳ B期。2017-04-17开始一线吉非替尼治疗, 并行腰椎姑息性放疗, 最好疗效评价为部分缓解[(partial response, PR); 缩小41%], 2017-11-28复查胸+上腹部增强CT及头颅增强MRI示全面进展(肺、脑、脑膜), 无进展生存期(progression-free survival, PFS)=7.4个月。2017-12-04行腰椎穿刺术, 脑脊液二代测序(next generation sequencing, NGS)示:EGFR 19del。2017-12-08开始二线培美曲塞联合贝伐珠单抗治疗, 共4周期, 2018-03-19复查胸+上腹部增强CT及头颅增强MRI示双肺、肝、脑部进展, 疗效评价为疾病进展[(progression disease, PD); 增大38%], PFS=3.4个月。2018-03-23行肝脏穿刺活检术, 肝肿瘤组织NGS示:EGFR 19del, T790M突变, EGFR扩增[拷贝数(copy number, CN)=3.2], MET扩增(CN=3.4); 外周血NGS检查示:EGFR 19del, T790M突变。2018-04-02开始三线奥希替尼治疗, 2018-04-27复查胸+上腹部增强CT示肝脏病灶局部进展, 肺原发灶缩小, PFS=0.8个月。外周血NGS:EGFR 19del, EGFR扩增(CN=2.8), MET扩增(CN=4.5)。2018-05-25开始四线奥希替尼联合伯瑞替尼(口服小分子MET酪氨酸激酶抑制剂)治疗, 2018-06-25复查胸+上腹部增强CT及头颅增强MRI示肝脏病灶进展, 肺部病灶缩小, 颅内多发转移瘤较前缩小, 脑干见新发病灶, PFS=1个月。2018-06-25行腰椎穿刺术, 脑脊液未见肿瘤细胞, 脑脊液ctDNA的NGS检测也未见有临床意义的基因突变。2018-06-28开始五线奥希替尼联合多西紫杉醇(40 mg/QW)治疗, 共8次、4个周期, 最好疗效评价为疾病稳定[(stable disease, SD); 缩小6%] , 2018-11-14复查胸+全腹部增强CT及头颅增强MRI示全面进展(脑、双肺、胸膜、多发骨、肝、肝门区和腹膜后多发淋巴结), PFS=4.5个月。2018-11-16行头颅伽玛刀治疗。外周血NGS示:EGFR 19del, EGFR扩增(CN=2.5), MET扩增(CN=3.7), BRAF V600E突变。多次基因检测结果详见表1, 各线用药后胸部病灶变化情况详见图1。2018-11-20开始六线紫杉醇+卡铂+贝伐珠单抗+阿特珠单抗治疗, 已完成2周期, 目前PS=1分, 有临床获益, 等待疗效评估。
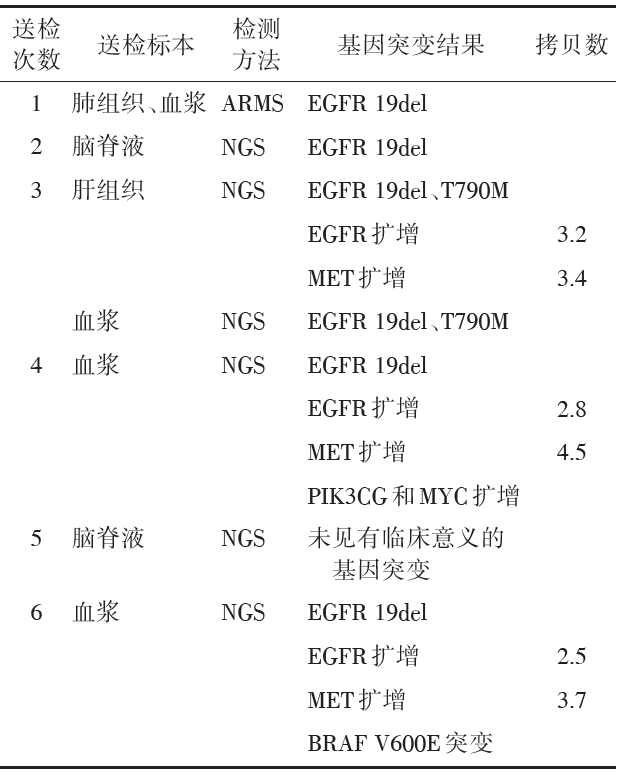
| 表1 患者多次基因检测的结果 |
康劲(肺内科医师):汇报病史特点(略)。提出讨论要点:(1)是否存在肿瘤异质性; (2)整个诊疗过程的评价; (3)若再次进展, 下一步该如何诊治。
吴一龙(肿瘤学教授):对肿瘤患者各线治疗进行疗效评价时, 有两项指标不能忽视, 一是每阶段的PS评分; 二是每种治疗手段有无临床获益。做出临床决策时, 必须清楚疾病每个阶段的标准治疗方案, 在标准治疗的基础上, 结合患者具体情况做出相应的调整。本病例中, 一线治疗为吉非替尼, PFS=7.4个月, 最好疗效PR, 病灶缩小41%, 进展时表现为全面进展, 此时二线标准治疗方案是什么?
杨衿记(肺内科主任医师):晚期肺腺癌患者, 驱动基因为EGFR突变, 一线一代EGFR酪氨酸激酶抑制剂(EGFR - tyrosine kinase inhibitor, EGFR-TKI)治疗后全面进展, 脑脊液NGS未见T790M突变, 推荐含铂双药化疗。但该患者当时拒绝使用铂类(害怕脱发等毒性), 拒绝参加临床试验, 所以二线治疗选择了培美曲塞联合贝伐珠单抗治疗。
旁述:中国临床肿瘤学会(CSCO)原发性肺癌诊疗指南(2018版) [1]显示:Ⅳ 期EGFR突变阳性非小细胞肺癌耐药后治疗的基本策略:根据进展类型分为局部进展型、缓慢进展型、快速进展型。若为局部进展型, 推荐继续EGFR-TKI治疗+局部治疗(2A类推荐证据)。若为缓慢进展型, 推荐继续原EGFR-TKI治疗(2A类推荐证据)。若为快速进展型, 检测T790M突变状态, T790M阳性者, 推荐奥希替尼或含铂双药化疗, T790M阴性者推荐含铂双药化疗(1类推荐证据)。可选策略:活检评估耐药基因, 根据基因检测结果入组临床试验。
陈华军(肺内科副主任医师):患者二线治疗的PFS为3.4个月, 结束第2周期时肺部及脑部病灶稳定, 肝结节稍增大, 当时决定继续2周期培美曲塞联合贝伐珠单抗治疗后复查CT, 如果肝结节继续增大, 行穿刺送基因检测。
吴一龙:二线治疗后进展, 此时的标准治疗方案又是什么?
康劲:NGS提示T790M突变, 三线应选择奥希替尼。
吴一龙:NGS示EGFR 19del, T790M突变, 选择奥希替尼是正确的, 但本例中T790M出现的时机有待考证。EGFR T790M是一代EGFR-TKI最常见的耐药机制, 该患者一线TKI耐药后脑脊液中T790M阴性, 经二线化疗后血浆中发现T790M, 应考虑该突变首次出现的时间是在一线TKI耐药后, 但当时只进行脑脊液NGS检测, 并未行血浆NGS检测, 因而无法验证。
黎扬斯(肺内科医师):脑脊液基因谱不同于外周血和组织。本例患者一线吉非替尼耐药后出现全面进展, 此时单一的脑脊液NGS无法反映患者的全身状态, 结合血浆NGS会更有助于诊断。针对T790M的检测, 血浆的检出率在一定程度上比脑脊液高, 但也受到进展部位的影响。
旁述:脑脊液上清循环游离DNA(circulating free DNA, cfDNA)具有独特的基因谱, 可作为液体活检的重要途径。吴一龙教授团队[2]发现EGFR T790M在脑脊液循环肿瘤细胞的检出率远低于颅外病灶, 可能与颅内EGFR-TKI浓度低以及T790M的空间异质性相关。另一方面, 对于EGFR驱动的非小细胞肺癌脑膜转移的患者, 血脑屏障阻碍神经系统cfDNA释放到血浆, 因而相比于血浆cfDNA, 脑脊液cfDNA更能反映颅内的基因谱, 可用于动态监测脑膜转移的肿瘤负荷[3]。
吴一龙:故事发展到这里, 三线奥希替尼的PFS只有0.8个月, 原因是什么?
杨衿记:患者三线治疗前外周血和肝组织NGS提示T790M突变, 经过奥希替尼治疗后再次进展, 此时外周血T790M消失, 这是奥希替尼的耐药机制之一, 也是预后不良的指标。此次进展表现为肺部病灶缩小, 肝病灶增大增多、部分缩小, 推测为不同部位肿瘤的异质性引起。肺部及肝脏部分病灶缩小, 可能是这部分病灶中存在EGFR 19del和T790M突变, 没有MET扩增, 所以病变得到控制, 但在肝的其他病灶中, 既有T790M突变, 同时伴随MET扩增、EGFR扩增, 这部分表现为原发耐药, 所以奥希替尼治疗的PFS较短。因为是混合疗效, 可考虑继续服用奥希替尼, 同时对肝部病灶进行局部治疗, 但肝有多个病灶, 不适合使用微创或消融术, 所以加上MET抑制剂伯瑞替尼。
旁述:美国哈佛大学Dana Faber癌症研究所2018年在《JAMA Oncol》上发表的一篇文章中提到, 伴T790M突变的患者使用奥希替尼进展时, 外周血cfDNA NGS检测T790M突变消失患者的中位至治疗中断时间(time to treatment discontinuation, TTD)显著短于保留T790M突变的患者[4]。作者进一步对AURA研究中的患者进行回顾性分析, 外周血NGS检测发现T790M突变消失的患者显示出更短的PFS, 即T790M突变消失患者会出现早期耐药, 从而验证了上述结果。
关于肿瘤异质性和混合疗效, 钟文昭等[5]对180例有配对组织标本的EGFR突变肺腺癌患者进行EGFR直接测序, 并进行分组比较分析, 最终得出亚洲肺腺癌患者中EGFR存在突变异质性, 以多发肺结节患者比例最高, 这可能是出现了混合疗效, 即肿瘤对靶向治疗的反应存在差异的原因。
吴一龙:奥希替尼治疗后T790M消失, 分为两种类型:(1)如果患者有临床获益, 病灶维持稳定或缩小, 此时T790M消失, 这部分患者预后是好的; (2)在疾病进展的过程中T790M消失, 则是预后不良。
张一辰(肺内科医师):奥希替尼治疗的PFS只有0.8个月, 属于原发耐药, 耐药机制主要有几下几种:(1)EGFR T790M的丰度, 如果丰度很低, 进展时出现T790M消失, 那可以考虑T790M的亚克隆是一个发挥次要作用的亚克隆; (2)共存突变, 本患者使用奥希替尼前肝组织NGS存在EGFR扩增、MET扩增, 这可以解释为什么获益时间这么短。而EGFR扩增和MET扩增同时存在时不能单纯考虑MET扩增是一个更占优势的耐药机制, 可以通过荧光原位杂交技术(fluorescence in situ hybridization, FISH)鉴别。治疗上可考虑采用双分子抗体联合奥希替尼, 但目前仅限于临床试验。
杨衿记:同意张医生的观点, 补充一点, 目前诊断EGFR扩增和MET扩增均通过NGS和FISH, 并没有进行蛋白质印迹法等蛋白表达检测, 因而无法判断产生突变或扩增的蛋白是否活化, 哪些基因突变真正起作用。建议临床上标本足够时, 加做蛋白表达相关检测, 在针对性选择靶向药物上更具指导意义。
吴一龙:同意两位的观点, 但需注意到在判断是否存在MET扩增和EGFR扩增时NGS报告的可信度。MET扩增目前在国际上并没有标准的定义, 不能单纯根据检测公司的NGS报告作出临床决策。同样的问题, EGFR扩增拷贝数多少才有临床意义, 目前也暂无定论。回到本例中, 此时患者MET扩增、EGFR扩增是否为耐药机制, 是以哪一个为主, 还是共同驱动, 不得而知, 同意尝试性加入伯瑞替尼治疗, 但必须看到, 奥希替尼联合伯瑞替尼在四线治疗中几乎没有发挥作用, PFS只有1个月。那五线为何仍使用奥希替尼联合多西紫杉醇?
陈华军:主要有以下两个原因:(1)四线治疗进展后脑脊液NGS未见突变靶点, PS评分在0~2分, 已经过培美曲塞化疗, 下一线选择多西紫杉醇单药化疗是标准治疗, 改成每周方案以减少化疗副作用; (2)患者肿瘤异质性明显, 使用奥希替尼之后有临床获益, 咳嗽减少, 肺部和脑部病灶均缩小, 所以继续使用, 再加上广谱的单药化疗。
杨衿记:此时的基因组学证据是不完整的, 脑脊液NGS未见突变, 没有加做血浆NGS加以验证。
吴一龙:从此处看, 患者奥希替尼从三线治疗开始, 持续到五线治疗, 部分病灶控制良好, 所以奥希替尼的PFS不能只算0.8个月, 而是因为肿瘤异质性的存在, 对其疗效造成干扰。多西紫杉醇化疗联合奥希替尼4.5个月后全面进展, 六线治疗选用紫杉醇+卡铂+贝伐珠单抗+阿特珠单抗的理由是什么?
陈华军:参考了IMpower150临床研究的结果。
旁述:IMpower150[6]是一项多中心、开放性、随机、对照的Ⅲ 期临床研究, 探索了化疗+抗血管生成药物+免疫检查点抑制剂用于晚期非鳞癌非小细胞肺癌一线治疗的疗效和安全性评估。研究设置了阿特珠单抗+卡铂+紫杉醇、贝伐珠单抗+卡铂+紫杉醇、阿特珠单抗+贝伐珠单抗+卡铂+紫杉醇三个亚组, 研究结果为阿特珠单抗+贝伐珠单抗+卡铂+紫杉醇显示了更长的PFS和总生存期, 差异有统计学意义。该研究特别强调:对于EGFR/ALK阳性的患者, 必须使用过标准靶向治疗失败后并满足其它条件才可以入组。
吴一龙:解读IMpower150的研究结果要谨慎:(1)这是一个亚组分析, 样本量小; (2)针对EGFR突变的患者, 无法分辨是抗血管生成药物起效还是免疫药物起效; (3)后续IMpower130、IMpower132研究发现去除贝伐珠单抗之后, 疗效并无差别; (4)对于阿特珠单抗, 目前主推的针对肝转移和/或EGFR突变的疗效并不明显。相比于目前六线的方案, 我更倾向于奥希替尼联合西妥昔单抗, 这两个药联合使用时可以把胞内胞外EGFR受体所有通路全部阻断。从目前临床经验看, 无论是疗效还是耐受性, 对一个经过多线治疗的患者是值得尝试的。
杨衿记:患者最后一次外周血NGS中出现BRAF V600E突变, 此处有无意义?
吴一龙:在进化树中, 此时出现的BRAF突变只是旁支, EGFR扩增和MET扩增更早出现, 所以应更关注EGFR扩增和MET扩增的问题。
陈华军:总结今天的病例, 本例为晚期肺腺癌患者, 有驱动基因突变, 整个治疗过程中出现肿瘤的不断进化和基因谱的不断改变, 已经过六线治疗, 目前初步评估有临床获益, 后续会继续追踪该患者病情, 及时反馈, 如果未来再次出现新的基因组学改变, 再进行针对性的讨论和治疗。
吴一龙:补充几点:(1)一个好的临床医师, 一个好的科学家, 必须具有怀疑精神、批判精神、分析精神, 青年医生在成长过程中应重视这方面的训练和思考。目前大多数医生过度相信NGS报告, 这是不恰当的, 所有的NGS报告必须结合临床、批判性地去看待, 必须经过临床验证才能相信。(2)如何解读一个临床研究。只有大型的Ⅲ 期临床试验结果才有可能改变我们的临床实践, 只根据临床试验的亚组分析, 仍不足以支持, 只是提供了参考的方向。应谨慎解读每个研究结果, 不能本末倒置。(3)越是复杂的患者, 治疗线数越多, 基因谱越复杂, 越应该拿出来讨论, 这也是多学科综合治疗及循证医学的意义和魅力所在。
后记:患者完成2周期紫杉醇+贝伐珠单抗+卡铂+阿特珠单抗化疗后疗效评估:SD(缩小12%)。 2019-01-15、2019-02-13继续行第3、第4周期化疗, 2019-03-12复查头颅MRI及胸+全腹部增强CT提示进展(颅内病灶明显增多、增大, 双肺转移灶多数稍增大)。 PFS=3.7个月。行腰椎穿刺术, 脑脊液未见肿瘤细胞。 脑脊液NGS示:EGFR 19del, MET扩增(CN=3.1), EGFR扩增(CN=14.5)。外周血NGS示:EGFR 19del, BRAF V600E突变。请示吴一龙教授后, 于2019-03-28开始七线阿法替尼治疗, 2019-04-24复查胸及上腹平扫CT提示双肺转移灶明显增多增大, 肝多发转移瘤病灶较前明显增大, 疗效评价为PD, PFS=0.9个月, 按照上述多学科综合讨论结果, 2019-04-25开始阿法替尼联合西妥昔单抗治疗, 2019-05-05复查胸部平片初步评估肺部病灶无明显变化, 患者临床症状同前, PS评分为2分。返当地医院对症支持治疗, 后于2019-05-25离世。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|