郝纯毅,北京大学肿瘤医院教授、主任医师、博士研究生导师。现任北京大学肿瘤医院大外科常务副主任、软组织与腹膜后肿瘤中心主任、肝胆胰外二病区主任、国际合作部主任,国际外科、胃肠病及肿瘤科医生协会(IASGO)副秘书长、学术委员会委员,中国医疗保健国际交流促进会软组织肿瘤委员会主任委员,中国临床肿瘤学会(CSCO)胰腺癌专家委员会主任委员,CSCO胃肠胰神经内分泌瘤专家委员会副主任委员,中国肿瘤微创治疗技术创新战略联盟副主任委员,第四届 CSCO 执行委员会委员,International School of Surgical Oncology (ISSO)学术委员会委员,中华医学会外科学分会胰腺学组委员,中华医学会北京肿瘤专业委员会委员,中国老年学学会老年肿瘤专业委员会执行委员会委员,中国医师协会外科医师分会委员,北京市卫生系统肝胆胰肿瘤外科学科带头人,英国卡迪夫大学荣誉教授。兼任《世界华人消化杂志》、《国际肝病》、《癌症》、《中国实用外科杂志》、《中 华 消 化 外 科 杂 志》、《中 华 外 科 杂 志》、《中 华 胃 肠 外 科 杂 志》、《Hepatogastroenterology》及《World J Gastroenterol》等杂志编委。近年来主持参与省部级以上课题 20 余项,国内外期刊发表论文100余篇。
研究一: Janssen QP, Buettner S, Suker M, et al. Neoadjuvant FOLFIRINOX in patients with borderline resectable pancreatic cancer: A systematic review and patient-level meta-analysis[J]. J Natl Cancer Inst, 2019, 111(8):782-794.
研究二:Katz MH, Shi Q, Ahmad SA, et al. Preoperative modified FOLFIRINOX treatment followed by Capecitabine-based chemoradiation for borderline resectable pancreatic cancer: Alliance for clinical trials in oncology trial A021101[J]. JAMA Surg, 2016, 151(8):e161137.
1b。
FOLFIRINOX (5-氟尿嘧啶+亚叶酸钙+伊立替康和奥沙利铂)是转移性胰腺癌患者的标准治疗方案。新辅助 FOLFIRINOX 方案在可能切除胰腺癌(borderline resectable pancreatic cancer, BRPC)患者中的有效性仍有争议。
虽然目前的共识指南支持BRPC的术前治疗, 但尚未对该策略进行前瞻性的多中心研究。 现有的研究多是回顾性的, 由于被研究患者的异质性、使用的治疗方案和模式的不一致, 可使临床结果不一致。
研究一:评估新辅助 FOLFIRINOX方案在BRPC治疗中的有效性。
研究二:探讨在合作组环境中进行BRPC多学科治疗研究的可行性。
研究一:
• 研究方法:系统评价和Meta分析。
• 检索方法:于2017年 9 月 1 日使用EMBASE、MEDLINE(通过OvidSP)、Web of Science、Scopus、Cochrane Central 和 Google Scholar 进行全面的文献检索。搜索使用以下关键词发表的英文文章:FOLFIRINOX、folinic acid、fluorouracil、irinotecan、oxaliplatin、pancreas cancer、drug combination等。
• 入选标准:关于BRPC患者应用新辅助FORFIRINOX化疗的前瞻性或回顾性研究。
• 评价方法:两名评价者分别对每个试验进行评价, 使用 Kaplan-Meier 方法进行分析。
• 评价指标:主要终点指标是总生存期(overall survival, OS)。次要终点指标包括无进展生存期(progression-free survival, PFS)、切除率、R0切除率和 3~4级不良事件。
研究二:
• 研究条件:美国肿瘤临床试验联盟14个肿瘤研究所的协作项目(NCT01821612)。
• 研究起止时间:2013年5月29日至2014年2月7日。
• 研究方法:前瞻性、多中心、单臂、病例对照研究。
• 研究对象:无远处淋巴结或远处转移的临界可切除的胰腺癌患者, 年龄≥ 18岁, PS评分0~1。
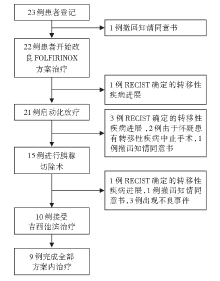
• 干预措施:干预措施流程见图1。
• 评价指标:主要终点指标包括入组率, 术前方案的安全性和耐受性, 术前治疗和手术切除完成率。次要终点指标包括影像学缓解率, 组织学缓解率, 至局部或远处复发时间, PFS及OS。
研究一:大多数研究(n=20)给予新辅助 FOLFIRINOX 周期的中位数范围为4~9个周期; 切除率为67.8%[95%可信区间(confidence interval, CI)60.1%~74.6%], R0切除率为83.9%(95%CI 76.8%~89.1%)。纳入研究的中位OS为11.0~34.2个月。患者的生存数据从20项研究中的283例患者获得, 中位OS为22.2个月(95%CI 18.8~25.6个月), 中位PFS为18.0个月(95%CI 14.5~21.5个月)。3~4级不良事件的汇总事件率以中性粒细胞减少最高(17.5例/100例患者, 95%CI 10.3~28.3例), 腹泻为11.1例/100例患者, 95%CI 8.6~14.3例, 疲劳为10.8例/100例患者, 95%CI 8.1~14.2例。
研究二:每个月2.6名患者的入组率优于预期的比例。14/22 名患者(64%, 95%CI 41%~83%) 有 3 级或更高的不良反应事件, 15/22名患者(68%, 95%CI 49%~88%)接受了胰腺切除术。这15例患者中, 12例(80%)需要进行血管切除术, 14例(93%)显微镜下切缘阴性, 5例(33%)标本中残留癌细胞少于 5%, 2例(13%)标本病理完全缓解。所有患者的中位OS为21.7个月(95%CI 15.7个月~未达到)。
研究一:对新辅助 FOLFIRINOX方案治疗的BRPC患者, 荟萃分析显示中位OS及切除率和 R0切除率有获益趋势。需要在随机试验中进一步评估这些结果。
研究二:该合作研究的成功证明了在多机构环境中为该疾病阶段进行质量控制试验的可行性。入组率超过预期目标, 毒性可控, 68%的患者接受了胰腺切除术。
胰腺癌的恶性程度极高, 预后极差, 5年生存率仅约9%[1]。手术切除目前仍然是胰腺癌治疗的主要手段, 随着胰腺外科手术技术的进步和围手术期管理的改善, 胰腺癌围手术期并发症和死亡率均有明显的下降, 但远期生存率却无显著的提高。胰腺癌对放化疗的治疗抗性较强, 长期以来缺乏有效的药物治疗方案, 提高胰腺癌远期预后的关键在于探索新的内科治疗策略。
自2003年开始, FOLFIRINOX方案首先在转移性胰腺癌患者中进行临床研究[2]。 随着大量研究结论的出现, 近年来NCCN指南已推荐FOLFIRINOX方案为局部晚期及转移性胰腺癌的标准一线化疗方案, 而2018年ASCO所报道的胰腺癌切除术后改良FOLFIRINOX对比吉西他滨辅助化疗的“ 重磅” 研究[3], 其结论进一步将三药联合化疗方案推广到了术后辅助化疗领域, 并被新版的NCCN指南推荐为体力状况良好患者一线辅助化疗方案。 从肿瘤药物研究的角度看, 最初在Ⅳ 期肿瘤中显示疗效, 进而推广至局部晚期肿瘤, 其后应用于新辅助治疗, 甚至最后推广到辅助治疗, 是很多药物临床研究的经典“ 套路” , 但值得注意的是, FOLFIRINOX虽然也被NCCN指南推荐为可切除及BRPC的新辅助治疗方案, 但其并无高级别的证据支持。
既往研究证实, 针对初始不可切除胰腺癌的转化治疗, FOLFIRINOX方案化疗无疑有显著的效果。而从本文中2篇文献的结论来看, 对于BRPC, 也显示该化疗方案在提高R0手术切除率方面的意义。但在受到鼓舞之余, 我们需要理性思考, 对于BRPC的新辅助化疗, 需考虑以下5个问题:
第一, 目前仍缺乏Ⅲ 期随机对照研究的证据支持FOLFIRINOX方案相比其他方案的客观有效率、R0切除率及远期生存率。本文评价的两项研究分别为系统回顾和Ⅱ 期单臂研究。Ⅱ 期单臂研究证据级别相对较低。而文献一的Meta分析本身也存在无法避免的设计缺陷, 如纳入分析的各研究中对于可能切除的定义采取了多个标准, 接受新辅助化疗的周期和是否联合局部放疗亦不统一, 对于R0切除的标准有的研究采取的是“ 1 mm” 标准, 有的则为“ 0 mm” 标准, 更有一些研究甚至未指明其R0切除标准。这些均影响了该系统回顾结论的科学性。
第二, 新辅助化疗本身的风险不可忽视。首先, 治疗前为取得病理学证据, 需常规进行胰腺组织病理学活检, 有创操作将不可避免地带来出血、感染、胰瘘甚至肿瘤种植的风险。此外, 对于梗阻性黄疸的患者, 新辅助化疗前需要留置胆道支架或者外引流, 将增加胆管感染的可能性。其次, 新辅助化疗也存在治疗过程中肿瘤进展无法手术的风险。虽然有研究显示FOLFIRINOX方案新辅助化疗可将局部晚期胰腺癌手术切除率提高至61%[4], 但许多研究也证实约20%的患者对该化疗方案无效。如文献二的A021101研究, 纳入的22例患者中5例患者(22.7%)在化疗期间出现明确或可疑的新发转移灶。诚然, 对于A021101研究而言, 其入组的患者均为可能切除的病例, 治疗期间肿瘤进展可以归因于生物学行为较差。但若将新辅助化疗扩展至初始可切除的胰腺癌患者, 治疗过程中肿瘤进展导致手术切除机会的丧失则意味着违反医学研究的基本伦理原则。
第三, NCCN指南对胰腺癌可能切除的定义本身虽然已极尽详细, 但仍然存在许多人为空间和难以避免的技术因素。首先, 可切除和不可切除的胰腺癌, 一般而言, 大多没有太大争议, 但如何理解何谓“ 可能切除” , 由于经验和理念的差异, 不同的外科医生则存在不同的理解, 在实践中往往倾向不同的策略, 迄今NCCN的专家组成员对胰体尾癌腹腔干动脉受累(可行Appleby术达根治性切除)属于“ 可能切除” 还是“ 不可切除” 仍存在不同声音。其次, 胰腺癌可切除性的判断主要依据增强CT或MRI等影像学检查, 对于新辅助治疗后的纤维化, 影像学上和肿瘤组织无法明确区分, 因而非常影响肿瘤对血管累及程度的判断, 单纯依靠影像学检查会降低评价的准确性, 亟需新的技术手段对新辅助化疗后的疗效进行评估。
第四, 胰腺癌新辅助化疗的疗效和生存期获益是否正相关尚难断定。例如, 新辅助治疗后的病理学完全缓解一般而言被认为是肿瘤生物学行为较好、预期生存和治疗效果好的标志。但根据约翰霍普金斯大学医院的报道, 该院接受FOLFIRINOX方案新辅助化疗后手术病理证实达到病理学完全缓解的16例患者中, 超过三分之一(6/16)的患者在术后数月内复发转移并在术后1年内死亡, 该结论颠覆了大多数肿瘤医生的常识。胰腺癌的生物学行为可能与其他大多数消化系统恶性肿瘤差异很大, 其他肿瘤新辅助治疗的成功经验并不能盲目地照搬。
第五, 较高的毒副反应率可能限制了FOLFIRINOX方案新辅助化疗的应用。临床实践中观察发现, 三药联合化疗的毒副作用要显著高于单药吉西他滨或吉西他滨联合白蛋白结合型紫杉醇化疗方案。3级以上不良反应率较其他化疗方案高, NCCN指南将FOLFIRINOX或改良FOLFIRINOX方案的应用范围严格限定于PS评分0~1分的患者。与欧美人群不同之处在于, 中国胰腺癌患者往往本身体质更差, 化疗耐受能力差, 一定程度上限制了FOLFIRINOX方案在国内的使用。
综上所述, FOLFIRINOX 方案新辅助化疗在可能切除的胰腺癌中有巨大的潜在应用价值, 但仍需要进一步大样本的随机对照研究证实。目前临床实践中, 对于该化疗方案在可能切除的胰腺癌患者中的应用, 需要严格评估体力状况, 并建议经多学科团队讨论后方可实施。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|