作者简介:
何池忠(1968-),男,安徽枞阳人,医学博士,副主任医师,目前的工作方向为缺血性脑血管病的介入诊断与治疗。
脑卒中是神经科最常见的急危重症, 具有高发病率、高复发率、高致残率和高致死率等特点, 已经成为我国第一位死亡原因。其中, 超过40%的缺血性卒中由急性大血管闭塞(large vessel occlusion, LVO)引起, 这种类型卒中可使患者6个月死亡率增加3.5倍, 良好预后比例下降67%, 早期有效地实现血管再通、挽救缺血半暗带是治疗的关键[1]。研究表明, 早期的静脉溶栓和以机械取栓为主的血管内治疗可以使闭塞血管再通, 改善患者预后, 而实施这些治疗措施需要时间窗和组织窗的指引[2]。
众所周知:脑梗死早期血管再通治疗具有时间依赖性, 时间就是大脑(time is brain)一直是其核心理念。传统意义上的时间窗包括两个方面的内容:①发病后0到3~4.5 h, 这是重组组织型纤溶酶原激活剂(recombinant tissue plasminogen activator, rtPA)静脉溶栓治疗的时间窗, 其临床意义已由大量随机对照试验(randomized controlled trial, RCT)证实, 并在很多国家地区得到广泛验证[3]。②发病后0~6 h, 这是LVO患者机械取栓的时间窗, 其安全性和有效性已得到多个高水平RCT研究及Meta分析的证实。2015年《N Engl J Med》公布的5项RCT一致表明, 以机械取栓为主的血管内治疗可大幅提高血管再通率, 带来显著的临床获益, 与内科治疗相比, 机械取栓对于提高90天独立功能比例, 校正优势比为2.49[95%可信区间(confidence interval, CI) 1.76~3.53], 绝对获益率提高19.5%, 使1例患者临床改善[至少降低改良Rankin量表评分(modified Rankin scale, mRS)1分]所需治疗的人数为2.6[4, 5, 6, 7, 8, 9]。
随着影像技术的发展、介入材料的进步和病例选择的优化, 时间窗的内容也在演变, 近年来机械取栓的“ 超时间窗(距最后正常的时间 6~24 h)” 日益收到关注。DAWN 研究纳入“ 超时间窗” 的前循环 LVO 患者, 时间中位数为12.2 h, 以临床症状[美国国立卫生研究院卒中量表(National Institutes of Health Stroke Scale, NIHSS )评分] 与影像检查结果[CT灌注成像(CT perfusion, CTP) 或磁共振弥散加权成像(diffusion-weighted imaging-magnetic resonance, DWI-MR) ]不匹配为筛选条件, 结果显示机械取栓组90天功能独立 (mRS 0~2 分) 比例更具明显优势(49% vs. 13%, 95%CI 21%~44%, 后验优势概率> 0.999)[10]。另一项类似的研究 DEFUSE 3 筛选了距最后正常的时间在6~16 h且低灌注区域与脑梗死核心体积不匹配的前循环 LVO 患者, 时间中位数为9.3 h, 也得到阳性结果[11]。最近有关DAWN和 DEFUSE 3的亚组分析数据陆续公布, 进一步证实了“ 超时间窗” 机械取栓的安全性和有效性[12]。
机械取栓“ 超时间窗” 的确立, 是近年脑梗死早期血管再通治疗的一件大事, 拓宽了治疗适应证, 同时也促使脑梗死的早期治疗由单纯的时间窗向多模式影像检查确立的组织窗的转变。组织窗是一种基于病理结构的临床标准, 可反映缺血发生后缺血半暗带向梗死核心的动态演变, 组织窗指引下的血管再通可扩大治疗的适宜人群, 过程更加精准, 结果更加优化, 所以Robinson教授认为卒中治疗理念须从“ 时间就是大脑” 向“ 不匹配就是大脑 (mismatch is brain)” 转变[13]。
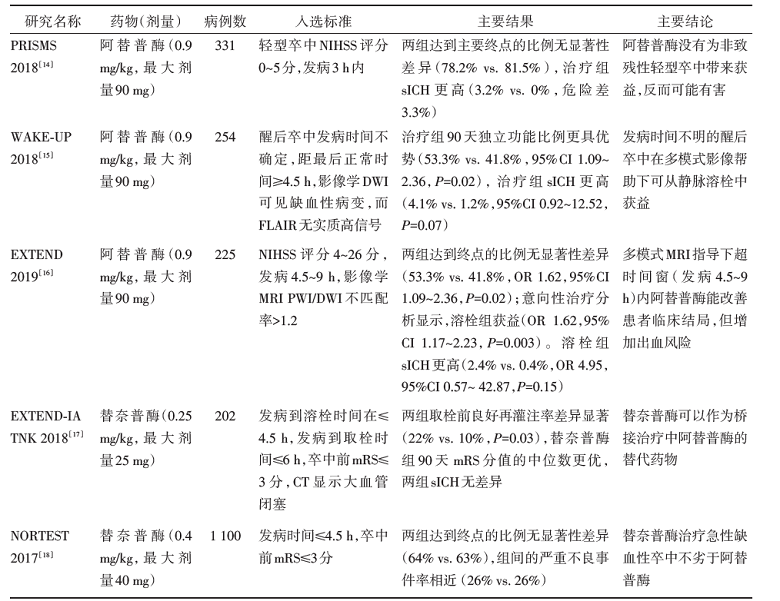
自1995年美国NINDS研究公布以来, rtPA静脉溶栓一直被认为是实现早期血管再通的金标准。最近相继发表的几个大型RCT, 展现了静脉溶栓在不同卒中领域的新进展, 见表1[14, 15, 16, 17, 18]。2019年10月美国心脏协会(American Heart Association, AHA)/美国卒中协会(American Stroke Association, ASA)发布的《2019急性缺血性卒中早期治疗指南》更新版, 对这些研究进行了详细的评估, 并根据这些成果及时地在指南中对静脉溶栓的适应证、多模式影像检查、轻型卒中和醒后卒中的静脉溶栓及新型溶栓剂替奈普酶的使用等方面大幅更新了推荐内容[19], 以期让这些研究成果能及时转化到临床实践中从而发挥最大效力。
| 表1 近期发表的主要静脉溶栓RCT研究 |
以机械取栓为主的血管内治疗已经成为缺血性卒中早期血管再通治疗的一线方案, 目前在我国得到推广。2018年8月中国卒中协会发布了《急性缺血性卒中血管内治疗中国指南2018》[20], 对机械取栓的实施流程、患者的筛选及围手术期管理等方面提出了38条推荐意见, 在临床上发挥了指导作用。但需指出的是, 指南是基于以往循证医学证据提出的诊疗建议, 并不能完全反映真实世界的实际情况, 实际工作中面临的一些争议问题, 需临床医师根据指南和自身经验做出综合判断。
指南根据发病的3类时间节点对机械取栓的适应证进行规定。发病6 h内:卒中前mRS 0~1分; 由颈内动脉或大脑中动脉 M1段闭塞引起; 年龄≥ 18岁; NIHSS≥ 6分; Alberta卒中项目早期CT评分(Alberta Stroke Program Early CT Score, ASPECTS)≥ 6分(Ⅰ 类, A级)。距最后正常时间6~16 h的前循环LVO:符合DAWN或DEFUSE 3研究入组标准(Ⅰ 类, A级)。距最后正常时间16~24 h前循环LVO, 符合DAWN研究入组标准(Ⅱ a类, B级)。这些适应证均基于以往RCT的设计, 不合理地丢失了大量真实世界中的LVO患者。越来越多的研究发现部分“ 超适应证” LVO患者也能从机械取栓中获益[21, 22, 23, 24]。这些“ 超适应证” 包括大脑中动脉 M2、M3段闭塞, ASPECTS≤ 5分, NIHSS≤ 5分, 发病时间> 24 h, 后循环LVO, 卒中前mRS> 1分等。“ 超适应证” 取栓是目前争议的热点, 我们认为“ 超适应证” 不是禁忌证, 期待更多的RCT厘清争议。
材料和技术的进步一直是发展机械取栓的原动力。以第二代取栓支架Solitaire和Trevo为代表的支架取栓技术助推了5大RCT的诞生, 因此被指南推荐为血管内治疗的首选技术。事实上随着材料的改进, 真实世界中取栓技术呈现“ 百花齐放” 的局面。①口径大、通过性好的中间导管的出现, 发展了新的直接血栓抽吸技术(a direct aspiration first-pass thrombectomy, ADAPT)。最近公布的COMPASS研究再次证实它在90天神经功能预后等方面均不劣于支架取栓[25]。临床上ADAPT具有操作简单、血运重建快、花费低等优点而备受青睐, 将其与支架取栓技术结合又产生了一批具有良好应用前景的新技术, 如Solumbra技术、SWIM技术、导管推越技术 ADVANCE等。②球囊导引导管(balloon guide catheters, BGC)逐渐代替常规导引导管。BGC的好处在于术中阻断正向血流和减少栓子逃逸, 也带来新的取栓技术如双重抽吸技术、Trevo联合近端血流控制技术等。③出现了一批设计新颖的取栓支架, 如Revive SE支架、Tigertriever支架等, 尚需临床资料的支持。
治疗理念由时间窗向组织窗转变, 构成了20多年来脑卒中早期血管再通治疗的基本脉络。组织窗的临床评估目前还缺乏统一的标准, 且评估过程冗繁复杂, 一定程度上妨碍了临床推广和应用。我们认为现阶段将组织窗与时间窗结合起来才能更好地指导临床工作。替奈普酶是一种新型溶栓剂, 具有半衰期长、使用方便的特点, 有望取代阿替普酶而使静脉溶栓变得简便易行, 值得期待。机械取栓的疗效毋容置疑, 但只有约15%的患者蒙获其益, 如何改进技术、优化流程及治疗对象, 使更多患者获益, 是今后的一个重要研究方向。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|