作者简介:
 | 段金海,医学博士,主任医师,硕士研究生导师。专注于神经内科专业技术工作,有较为广阔的临床视野和较强的临床动手能力,能独立解决本专业复杂疑难病例的诊治工作。对神经科常见疾病,如脑血管病、痴呆的诊疗具有优势。掌握脑血管病介入治疗术,高龄患者颈动脉支架植入术成果已在国内外期刊发表。2015年3月至2016年3月在加拿大McGill大学附属Lady Davis Institute/Jewish General Hospital及Montreal Neurological Hospital任访问学者。2017年9月至10月在瑞典Karolinska Institute接受阿尔茨海默病和其他痴呆症的诊疗技术培训。兼任广东省医学会脑血管病分会急诊救治学组副组长、广东省老年保健协会神经免疫与感染专业委员会委员、广东省医学会神经病学分会第七届委员会生化学组组员、中华医学会老年医学分会青年委员会委员、广东省医学会老年医学分会委员兼秘书、广东省保健协会老年性痴呆医养融合分会副主任委员、中国老年医学会舒缓医学分会第一届青年委员会副主任委员兼副秘书长。参译学术专著《老年医学》,任《中华老年医学杂志》通讯编委。主持省部级课题6项,发表学术论文20余篇。 |
Thomalla G, Simonsen CZ, Boutitie F, et al. MRI-guided thrombolysis for stroke with unknown time of onset[J]. N Engl J Med, 2018, 379(7):611-622.
1b。
阿替普酶(一种重组组织纤溶酶原激活剂)静脉溶栓治疗是发病4.5小时内急性缺血性脑卒中的标准药物。14%~27%的脑卒中患者不能明确具体的发病时间, 通常是因为患者从睡眠中醒来时才识别出脑卒中症状。这类患者通常不接受静脉阿替普酶溶栓治疗, 只有其中一部分符合机械血栓切除术的适应证。
研究发现, 大部分醒后脑卒中可能发生在觉醒前的最后几个小时, 仍然在静脉溶栓治疗的时间窗内。在已知症状发作时间的脑卒中患者中, 磁共振成像(magnetic resonance imaging, MRI)已经确定了磁共振弥散加权成像(diffusion-weighted imaging, DWI)中存在可见的缺血性病变, 同时液体衰减反转恢复(fluid-attenuated inversion recovery, FLAIR)序列未发现相同区域中的高信号, 可以作为影像学判断发病4.5小时内的预测依据。
根据目前的指导原则, 只有对发病时间少于4.5小时的急性脑卒中患者, 才能使用静脉溶栓治疗。本研究试图确定卒中发作时间未知并且MRI提示新发脑梗塞的患者, 能否从阿替普酶静脉溶栓治疗中获益。
进行基于MRI的脑卒中溶栓治疗(WAKE-UP研究)的有效性和安全性研究, 以确定阿替普酶治疗是否可以改善卒中发作时间未知以及DWI与FLAIR之间不匹配患者的功能结局。
• 研究条件:欧洲8个国家61个中心参与的WAKE-UP研究(由欧盟第七框架计划资助, NCT01525290, EudraCT号2011-005906-32)。
• 研究起止时间:2012年9月24日至2017年6月30日。
• 研究方案:多中心、随机、双盲、安慰剂对照试验。
• 研究对象:发作时间未知的脑卒中患者。在研究人员MRI的判断下, 患者在DWI中显示急性缺血性病变, 但在FLAIR上使用标准窗口设置没有实质性高信号。
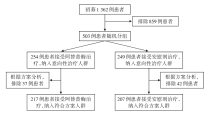
• 干预措施:随机接受阿替普酶(0.9 mg/Kg, 以10%的剂量推注, 其余的则在60分钟内输注)或匹配的安慰剂, 具体流程见图1。在基线、随机分配后22~36小时、5~9天(或出院)和90天进行临床评估。
• 评价指标:主要终点指标是良好的临床结局 [定义为随机分组后90天, 按改良的Rankin量表(modified Rankin scale, mRS)评分为0或1]; 次要终点指标包括mRS在90天时的序数评分、90天有治疗反应的患者比例、90天时的总体结果得分等。主要安全性终点指标为死亡和死亡或依赖的综合结果(90天时mRS量表评分4~6分); 次要安全性终点指标是导致神经系统症状恶化的症状性颅内出血和随机分组后22~36小时MRI上显示2型实质性血肿的发生率。
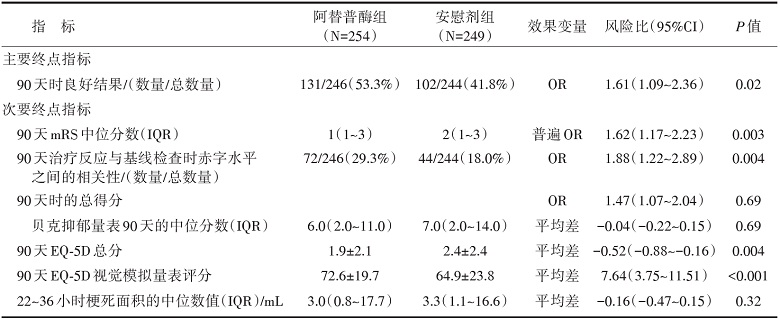
800名患者中的503名患者入选后, 由于缺乏资金, 该试验提前终止。阿替普酶组和安慰剂组分别有8例和5例患者失访。阿替普酶组246例患者中有131例(53.3%)显示90天时良好结果, 安慰剂组244例患者中有102例(41.8%)显示良好结果 [校正优势比(odds ratio, OR)1.61, 95%可信区间(confidence interval, CI)1.09~2.36, P=0.02]。阿替普酶组在90天时的mRS评分的中位数为1, 安慰剂组为2(校正后的普遍OR 1.62, 95%CI 1.17~2.23, P=0.003)。见表1。
| 表1 WAKE-UP研究的主要和次要终点指标(意向性治疗人群) |
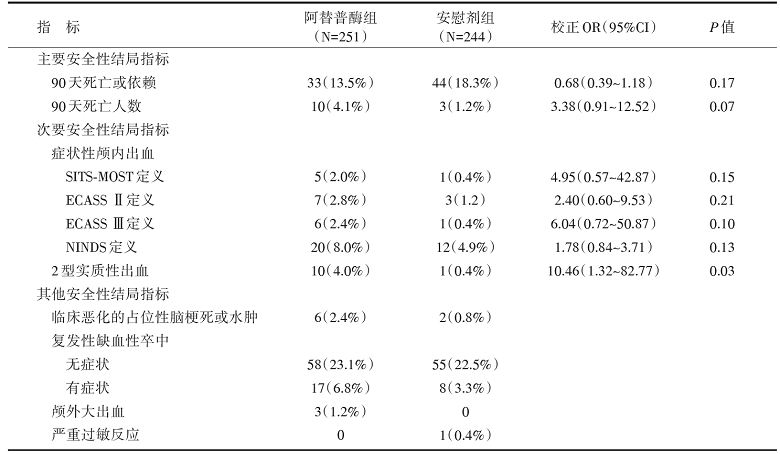
阿替普酶组有10例死亡(4.1%), 安慰剂组有3例(1.2%)(OR 3.38, 95%CI 0.92~12.52, P=0.07)。阿替普酶组和安慰剂组症状性颅内出血的发生率分别为2.0%和0.4%(OR 4.95, 95%CI 0.57~42.87, P=0.15)。见表2。
| 表2 WAKE-UP研究的安全性结局指标 |
在发病时间未知的急性脑卒中患者中, 在缺血区域的DWI和FLAIR不匹配的指导下, 静脉注射阿替普酶的患者, 在90天内其功能预后明显优于安慰剂组, 但是颅内出血数量也高于安慰剂组。
WAKE-UP研究中, 卒中发作时间未知的患者在DWI中表现出缺血性病变的MRI表现, 但在FLAIR的相应区域没有明显可见的信号变化, 其中90天的功能结局在接受阿替普酶静脉溶栓治疗的患者更为有利的人数比接受安慰剂的患者要多。MRI不匹配模式表明卒中发生在大约4.5小时内, 仍然在溶栓治疗的时间窗内。结果发现, 阿替普酶组的患者在90天时无神经功能缺损或严重残疾的比例比安慰剂组高11.5%。通过mRS评分发现, 阿替普酶溶栓组患者得分更高, 并且在所有类别上都比安慰剂有更好的结局。
静脉溶栓治疗试验的荟萃分析显示, 给药对结局具有时间依赖性, 在症状发作后4.5小时内阿替普酶静脉溶栓具有明显获益[1]。WAKE-UP研究根据MRI弥散加权成像与FLAIR显示不匹配来选择患者。在之前的两项研究中, 对此结果的综合认同率为73%~78%[2, 3]。WAKE-UP研究的结果为卒中发作时间未知的患者使用阿替普酶静脉溶栓提供了影像学参考标准。
WAKE-UP研究提供了阿替普酶再灌注治疗有益于轻度或中度卒中患者的证据, 这些患者通常不适合进行血管内治疗。WAKE-UP研究中阿替普酶在轻度或中度卒中患者中的治疗效果与溶栓试验汇总分析一致, 即根据卒中严重程度, 阿替普酶治疗的疗效没有显著性差异[4]。
WAKE-UP研究的安全性结局指标表明, 与安慰剂组相比, 阿替普酶组的死亡人数和2型实质性出血患者要多得多。这一发现与卒中溶栓试验的汇总分析相似, 即阿替普酶治疗相关的死亡率有增加的趋势[5, 6]。WAKE-UP研究的次要安全性结局指标为症状性颅内出血, 其无论用何种方式(SITS-MOST、ECASSⅡ 、ECASSⅢ 、NINDS)表示这种并发症的定义, 阿替普酶组中有症状性颅内出血的发生率都较高, 这与以前的溶栓治疗卒中的试验结果一致[6]。由于资金中断, WAKE-UP研究被提前终止, 并且招募的患者少于计划的人数, 这个因素限制了对安全性结果的解释, 因为随着样本量的增加, 在阿替普酶组中观察到的死亡率更高的趋势可能已经变得很明显。
尽管阿替普酶具有临床获益, 但在两个试验组之间, 随机分组后22~36小时的MRI梗死体积无明显差异。这一发现与DEFUSE 3研究[4]的结果相似, 在DEFUSE 3研究中, 24小时较小的梗死体积并未反映出血栓切除术的临床获益。
总之, 对于急性卒中和症状发作时间不明的患者, MRI弥散加权成像表现为缺血性病变, 但在FLAIR的相应区域没有实质性信号, 静脉阿替普酶溶栓组的功能预后优于安慰剂组。但是, ECASS-4 EXTEND 研究却得出了阴性结果。ECASS-4EXTEND研究对发病4.5~9 小时或醒后发病、有明显影像学错配的缺血性卒中患者进行了阿替普酶静脉溶栓治疗, 与对照组相比, 其并未改善患者的90天mRS评分, 且使用阿替普酶静脉溶栓治疗的患者死亡率更高[7]。
最近刚发表的EXTEND研究[8]为一项多中心随机对照试验, 探索了是否能放宽溶栓时间窗至9小时。纳入患者标准主要基于起病时间(起病后4.5~9小时; 对于醒后卒中患者, 将入睡时间和醒来时间的中点作为起病时间)和影像学证据(CT灌注成像或MRI灌注成像提示存在低灌注但是可挽救的缺血脑组织)。该研究纳入了225名患者, 阿替普酶溶栓组113名患者, 安慰剂组112名患者。治疗有效性以起病后第90天mRS评分评估(主要比较了两组患者获得评分为0或1的情况), 相比安慰剂组(33例, 29.5%), 阿替普酶溶栓组有更多患者获得mRS评分0~1分(40例, 35.4%)(P=0.04); 安全性根据症状性颅内出血情况评估, 相比安慰剂组(1例, 0.9%), 阿替普酶溶栓组(7例, 6.2%)有更多患者出现症状性颅内出血(P=0.05)。因此, 这项研究提示扩大溶栓时间窗或许能使更多卒中患者获益, 但是症状性颅内出血的风险也更高。这也与WAKE-UP研究的结论相吻合。
由于临床上常用的静脉溶栓药物都对卒中症状出现时间有明确的要求, 阿替普酶静脉溶栓要求在4.5小时内, 尿激酶静脉溶栓要求在6小时内, 因而对那些卒中发作时间未知但有可能在静脉溶栓时间窗内的患者, 很可能会因此错过最佳血管再通时间而加重病情, WAKE-UP研究有可能为该类患者的临床治疗方案选择提供新的思路, 但同时, 我们也应持谨慎的态度, 注意关注其安全性。
这些研究结果还需要更多、更大样本量试验进一步验证, 或许将来很有可能不再采用“ 时间窗” , 而是通过医学影像技术采用更精确的“ 组织窗” 来筛选合适的患者。许多相关问题也有待进一步研究来探索答案。期待WAKE-UP后续的研究结果, 也希望有更多类似的临床研究能为急性缺血性脑卒中患者带来更好的治疗方案。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|