| 王震,医学博士,广东省人民医院、广东省肺癌研究所副主任医师,硕士研究生导师。2014年9月至2015年8月获得ASCO Cancer Foundation The Long-term International Fellowship (LIFe)奖学金资助在美国俄亥俄州大学James Cancer Center访问学者。2003年7月至2003年12月在德国Greifswald大学血液和肿瘤移植研究中心从事研究工作。从医20余年,具有丰富的临床工作经验。致力于以化疗、靶向治疗和免疫治疗为基础的肺癌多学科综合治疗以及肺癌转化医学研究。主持或参与多项临床试验,作为研究者曾参与IPASS、LUX-LUNG系列、AURA3、FLAURA、CheckMate系列、KEYNOTE系列等国际著名多中心临床试验。 |
Paz-Ares L, Luft A, Vicente D, et al. Pembrolizumab plus chemotherapy for squamous non-small-cell lung cancer[J]. N Engl J Med, 2018, 379(21):2040-2051.
1b。
转移性鳞状非小细胞肺癌(non-small cell lung cancer, NSCLC)的标准一线方案是铂类化疗或帕博利珠单抗, 针对肿瘤细胞的程序性死亡配体1(programmed death ligand 1, PD-L1)表达≥ 50%的患者。
最近有研究显示, 在非鳞状NSCLC患者中, 帕博利珠单抗联合化疗可显著延长患者总生存期(overall survival, OS)。而在转移性鳞状NSCLC患者中这种联合治疗方案是否也能延长OS仍需证据支持。
研究帕博利珠单抗联合化疗对转移性鳞状NSCLC患者OS的影响。
• 研究条件: 来自17个国家137个中心参加的KEYNOTE-407临床试验(NCT02775435)。
• 研究方法:多中心, 双盲, 随机对照试验, Ⅲ 期临床研究。
• 研究时间:2016年8月19日至2017年12月28日进行随机化分组。
• 研究对象:未接受过任何治疗的经病理明确诊断的Ⅳ 期鳞状NSCLC患者, 年龄≥ 18岁、PS评分0~1分、根据RECIST 1.1, 存在至少1个可测量病灶, 并提供用于确定PD-L1状态的肿瘤样品。
• 干预措施:入组患者以1:1进行随机分组, 接受帕博利珠单抗 200 mg或生理盐水(安慰剂), d1, 每3周一个周期维持治疗至35周期。所有患者研究开始均接受卡铂(曲线下面积6 mg/mL/分, d1)+紫杉醇(200 mg/m2, d1)或白蛋白紫杉醇(100 mg/m2, d1、8、15), 每三周一个周期, 共4个周期。安慰剂疾病进展(progression disease, PD)后可交叉至帕博利珠单抗维持治疗。见图1。
• 评价指标:主要终点指标包括OS和无进展生存期(progression-free survival, PFS), 次要终点指标包括缓解率(response rate, RR)和安全性。
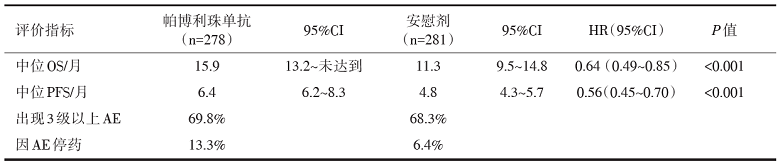
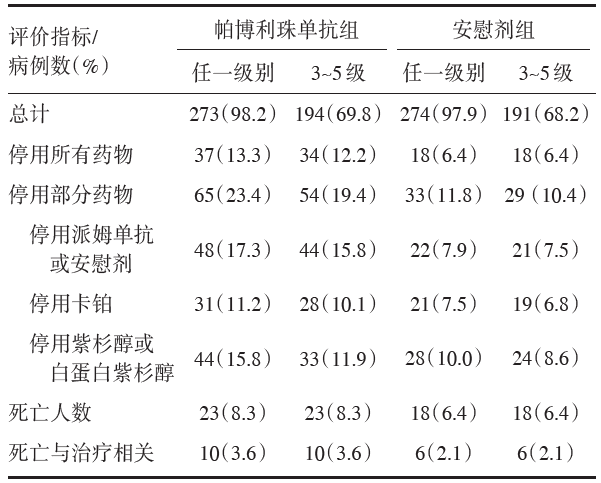
共入组晚期鳞状非小细胞肺癌患者559例。中位随访时间为7.8个月。帕博利珠单抗的中位OS显著长于安慰剂, 分别为15.9个月[95%可信区间(confidence interval, CI) 13.2~未达到]和11.3个月(95%CI 9.5~14.8), 降低了死亡风险36%[死亡风险比(hazard ratio, HR)0.64, 95%CI 0.49~0.85, P< 0.001]。中位PFS分别为6.4个月和4.8个月。出现3级以上不良事件(adverse event, AE)发生率相似, 但帕博利珠单抗组因AE停药发生率较高, 见表1和表2。
| 表1 KEYNOTE-407主要结果 |
| 表2 KEYNOTE 407毒副反应 |
对于先前未经治疗的转移性鳞状NSCLC患者, 帕博利珠单抗联合卡铂 + 紫杉醇/白蛋白紫杉醇较之单独使用化疗, 可显著延长患者的总体生存期和无进展生存期。
非小细胞肺癌中鳞癌占25%~30%, 因缺乏有效的驱动基因突变, 一直属难治性疾病。KEYNOTE-407研究是非小细胞肺癌的里程碑事件, 虽然正式发表1年余, 仍然值得讨论一下。
随着免疫治疗的兴起, 免疫治疗联合化疗延长了晚期肺癌的生存, 使化疗重新变得重要起来。关于晚期肺鳞癌的化疗目前仍无太大进展。Ⅱ 期临床研究C-TONG 1002一线白蛋白结合型紫杉醇 + 卡铂对比吉西他滨 + 卡铂治疗晚期肺鳞癌, ORR、PFS、OS均相类似, 白蛋白紫杉醇方案在改善生活质量方面略有优势[1]。Ⅲ 期临床研究SQUIRE采用表皮生长因子受体(epithermal growth factor receptor, EGFR)抑制剂耐昔妥珠单抗(Necitumumab)联合吉西他滨 + 顺铂对比单纯化疗一线治疗晚期肺鳞癌, OS略有延长(11.5个月vs. 9.9个月), 但因为副作用及临床获益有限, 应用受到限制。虽然EGFR高表达和拷贝数扩增者有生存获益, 但因缺乏验证尚不能成为有效的疗效预测指标[2]。
近年来晚期非鳞癌一线免疫治疗的临床试验不断有报道, 能够带来惊喜的却并不多。KEYNOTE-407是其中可圈可点者。
KEYNOTE-407结果提示一线帕博利珠单抗联合化疗显著延长了晚期肺鳞癌的PFS和OS。试验组的有效率和疗效持续时间显著优于对照组。试验组免疫相关性不良事件(28.8% vs. 8.6%)和3度以上不良事件(10.8% vs. 3.2%)明显增加。由于长时间维持治疗, 免疫治疗组因不良事件导致停药的比率显著高于安慰剂组[3]。帕博利珠单抗组在第9周和第18周较单纯化疗组明显改善患者的生活质量[4]。
PD-L1肿瘤比例评分是帕博利珠单抗的生物标志物。KEYNOTE-024研究证实, PD-L1大于50%的晚期非小细胞肺癌一线帕博利珠单抗较化疗有明显生存获益[5, 6]。KEYNOTE-407根据PD-L1表达分成PD-L1< 1%、1~49%、≥ 50%三个亚组, 前两个亚组帕博利珠单抗联合化疗较单纯化疗PFS和OS均有优势, 但是PD-L1≥ 50%亚组两种方案的OS(HR 0.64, 95%CI 0.37~1.10)无统计学差异[4]。虽然亚组结果不足为信, 但还是引发一些问题, 如帕博利珠单抗单药的生物标志物不同于与化疗联合?PD-L1的疗效预测意义鳞癌不同于非鳞癌?
KEYNOTE-407采用紫杉醇和白蛋白结合型紫杉醇作为化疗方案。60%的患者选择了紫杉醇。不论紫杉醇还是白蛋白结合型紫杉醇, 加用帕博利珠单抗均提高了OS、PFS和ORR, 3~5级不良事件相似[7]。白蛋白结合型紫杉醇因为无需激素等抗过敏药物预处理的特点在免疫联合化疗中似乎具有某些优势。
KEYNOTE-407研究对美国患者进行了费效比分析。帕博利珠单抗联合化疗较单纯化疗预计延长生命1.95年(3.86 vs. 1.91), 费效比增幅(incremental cost-effectiveness ratio, ICER)为美元86 293/质量矫正生存年(quality-adjusted life year, QALY)。因为免疫治疗预计延长生命约一倍, 且ICER小于美元10 000/QALY, 因此成为有成本效益的一线晚期肺鳞癌治疗方案。但对于PD-L1≥ 50%者, 帕博利珠单抗联合化疗较帕博利珠单抗单药更节约成本, 可能原因是用于比较的因子太不确定, 且需要进一步随访[8]。
IMpower131是关于一线治疗晚期肺鳞癌的Ⅲ 期临床试验。中期分析提示, 白蛋白紫杉醇 + 卡铂联合抗PD-L1抗体阿特珠单抗(Atezolizumab)较单纯化疗可以降低29%的进展或死亡风险, 但OS无差别[9]。将KEYNOTE-407和IMpower131比较后发现, 帕博利珠单抗较阿特珠单抗显著延长OS和PFS, 两者ORR相似。PD-1高表达者, 两组OS和PFS相似, PD-L1阴性者, 帕博利珠单抗较阿特珠单抗明显延长OS和PFS[10]。因为是中期结果, 尚不能得出明确的结论。
其它晚期肺鳞癌免疫治疗显得更暗淡些。细胞毒T细胞淋巴细胞抗原4(cytotoxic T-lymphocyte-associated antigen 4, CTLA-4)抑制剂伊匹木单抗联合紫杉醇 + 铂类对比单纯化疗的研究发现, 联合组较单纯化疗组未延长OS(13.4个月 vs. 12.4个月, HR 0.91, 95%CI 0.77~1.07, P=0.25), 中位PFS均为5.6个月(HR 0.87, 95%CI 0.75~1.01), 免疫联合化疗的毒性高于单纯化疗[11]。最终结果尚未发表, 看起来前景不容乐观。
到目前为止, 帕博利珠单抗联合化疗是晚期肺鳞癌一线选择方案, 不必考虑肿瘤组织PD-L1的表达状态。免疫联合化疗加后续免疫维持治疗, 患者需长时间治疗, 免疫相关毒性是需要考虑的问题。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|