| 应志涛,医学博士,副主任医师。 中国抗癌协会血液肿瘤委员会青年委员,中国老年血液学淋巴瘤学组委员,中华医学会肿瘤学分会青年委员,中国临床肿瘤学会(CSCO)青年专家委员会委员。 2009年毕业于北京大学医学部,获得肿瘤学博士学位。2009年开始于北京大学肿瘤医院淋巴瘤科工作至今,主要研究方向为淋巴瘤规范化诊断与治疗。2014年至2015年分别在美国University of Florida和Memorial Sloan Kettering Cancer Center淋巴瘤科作为访问学者参观学习。参编多部肿瘤学书籍,发表论文20余篇。 |
Sehn LH, Herrera AF, Flowers CR, et al. Polatuzumab Vedotin in relapsed or refractory diffuse large B-cell lymphoma[J]. J Clin Oncol, 2020, 38(2):155-165.
2a。
虽然弥漫大B细胞淋巴瘤(diffuse large B cell lymphoma, DLBCL)患者经标准R-CHOP方案治疗可获得治愈, 但仍有30%~40%的患者出现复发或者难治, 其中30%~40%的患者经挽救化疗后续予自体造血干细胞移植(autologous stem-cell transplantation, ASCT)仍可治愈; 而对于不适合移植或挽救化疗无效或移植后复发的患者, 预后差, 中位总生存期(overall survival, OS)仅6个月, 其治疗包括以吉西他滨或铂类为基础的方案以及苯达莫司汀联合利妥昔单抗(Bendamustine+Rituximab, BR)方案, 尚无标准治疗。
Polatuzumab Vedotin由一种人源化抗CD79b抗体与抗有丝分裂剂MMAE(单甲基阿司他丁E)偶联而成的抗体药物偶联物(antibody-drug conjugate, ADC), 单药或联合CD20单抗治疗复发/难治性DLBCL的客观有效率(objective response rate, ORR)为13%~56%, 但完全缓解率(complete response, CR)低, 仅0~15%, 提示需联合其他药物以提高疗效。BR方案治疗不可移植的复发/难治性DLBCL的疗效不佳, 中位无进展生存期(progression-free survival, PFS)仅3.6~6.7个月, Polatuzumab Vedotin联合BR可能提高疗效。第二代CD20单抗奥滨尤妥珠单抗(Obinutuzumab)相较利妥昔单抗能更好地使免疫系统攻击并杀死B细胞, 与Polatuzumab Vedotin及苯达莫司汀联合治疗是具有前景的方案。
Polatuzumab Vedotin联合苯达莫司汀及奥滨尤妥珠单抗(pola-BG)治疗复发/难治性DLBCL的疗效及安全性; Polatuzumab Vedotin联合BR(pola-BR)对比BR方案治疗复发/难治性DLBCL的疗效。
• 研究条件:包括美国、澳大利亚等共13个国家的62个中心参与研究(NCT02257567)。
• 研究起止时间:2014年10月15日至2016年6月10日。
• 研究方法:国际多中心、随机、开放标签、Ⅰ b/Ⅱ 期临床试验。
• 研究对象:经病理确诊的复发/难治性且不适合造血干细胞移植的DLBCL。
• 入组标准:
病理确诊的复发/难治性DLBCL; 既往接受过苯达莫司汀治疗的患者, 苯达莫司汀疗效维持时间在1年以上, 接受其他方案治疗的患者的疗效持续时间在1年以上; 至少有一个二维可测量病灶, 长径大于1.5 cm; 中心病理可重新评估病理; 预期生存期至少24周; ECOG评分0~2。
• 排除标准:
对苯达莫司汀、利妥昔单抗或奥滨尤妥珠单抗存在用药禁忌; 入组后第一周期第一天用药前4周内用过任何类型的单抗、放射免疫结合物、ADC; 入组后第一周期第一天用药前2周内用过放疗、化疗、免疫治疗、免疫抑制疗法或任何以抗肿瘤为目的的药物; 入组后第一周期第一天用药前100天内接受造血干细胞移植或CAR T治疗; 接受过异基因造血干细胞移植; 适合行ASCT; 存在严重的不能控制的合并症、活动性感染。
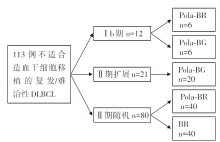
• 干预措施:研究设计流程见图1。所有患者接受苯达莫司汀(B)90 mg/m2静脉滴注(intravenously, IV), 第一周期d2~d3, 后续周期d1~d2; 利妥昔单抗(R)375 mg/m2 IV, 每一周期d1或奥滨尤妥珠单抗(G)1 000 mg IV, 第一周期d1、d8、d15, 后续周期d1; 接受Polatuzumab Vedotin(Pola)1.8 mg/kg IV, 第一周期d2, 后续周期d1。
• 评价指标:Ⅰ b期:主要终点:安全性和耐受性; Ⅱ 期:主要终点:CR, 次要终点:治疗结束时的ORR、最佳ORR、反应持续时间(duration of response, DOR)及PFS; 探索终点:根据分子标志物分析DOR、PFS和OS, 分子标志物包括根据细胞起源及免疫组化评估的双表型。
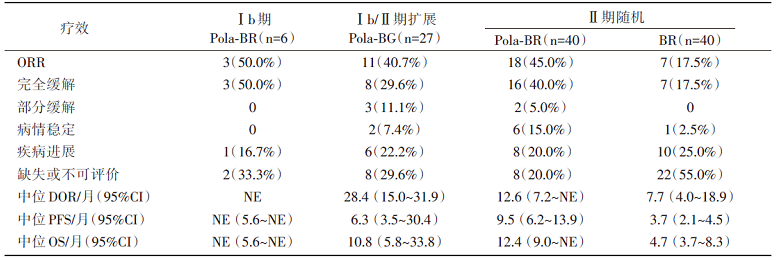
6.1 独立评估委员会(independent review committee, IRC)评估的治疗结束时的疗效, 如表1。在Ⅱ 期随机队列中, pola-BR组较BR组有较高CR(40% vs. 17.5%, P=0.026), 有较长的PFS(9.5个月 vs. 3.7个月, 风险比=0.36, 95%CI 0.21~0.63, P< 0.001)和OS(12.4个月 vs. 4.7个月, 风险比=0.42, 95%CI 0.24~0.75, P=0.002)。
| 表1 IRC评估治疗结束时的疗效 |
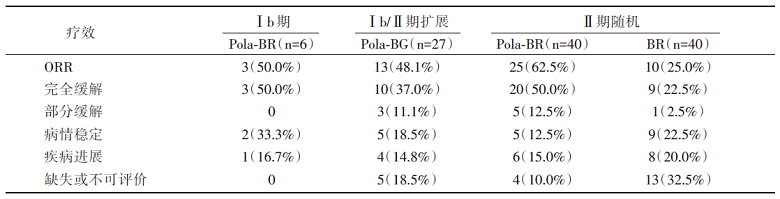
6.2 IRC评估的最好疗效, 如表2。
| 表2 IRC评估的最好疗效 |
对比BR方案, Polatuzumab Vedotin联合BR提高了不可移植的复发/难治性DLBCL的CR, 显著降低死亡风险。
弥漫大B细胞淋巴瘤(DLBCL)是一组高度侵袭性非霍奇金淋巴瘤, 经过标准R-CHOP方案治疗, 仍有约30%~40%的患者会复发进展[1, 2]。对于年轻体力状态好的患者, 可以选择二线挽救化疗, 有效后给予大剂量化疗联合自体造血干细胞移植(autologous stem-cell transplantation, ASCT)巩固治疗, 部分患者仍可能治愈[3]。如果患者因年老或者体力状态差, 或移植后再次复发, 再接受常规化疗疗效不佳[4]。
CD19 CAR T的出现显著提高了这部分患者的预后, 为这一领域的新药研究设立了一个很高的疗效标杆[5, 6, 7, 8]。但存在的许多问题也不容忽视, 如:患者既往接受过多种方案治疗, 并非所有患者都能成功采集细胞; 少部分患者的细胞体外培养可能不成功; 自体来源的CAR T细胞体外培养需要一定时间, 如果患者病情进展快, 不能等到细胞回输; 治疗相关毒副反应发生率高; CAR T细胞治疗后仍可能无效或复发进展; 细胞培养成本高, 价格高昂。
靶向CD79b的ADC类药物Polatuzumab Vedotin联合苯达莫斯汀和利妥昔单抗(Pola-BR)在不适合接受移植或移植后复发的DLBCL患者中CR为40%, 接近CD19 CAR T疗效。中位PFS和OS分别为9.5个月和12.4个月。Pola-BR组有更多患者发生严重血液学毒性, 而加入Polatuzumab Vedotin所发生的神经毒性全部为轻度。2019年美国血液学年会进一步更新了该研究的结果, 共46例患者接受Pola-BR治疗, 17例(38%)患者疗效维持时间超过12个月, 13例(29%)疗效维持时间超过24个月[9]。该方案为复发难治DLBCL患者带来更多治疗选择。
实际上, 临床上有多个化疗方案可以作为复发难治DLBCL的挽救化疗方案。本研究仅探讨了Polatuzumab Vedotin联合BR的安全性和疗效, 与其他方案联合是否为阳性结果目前仍未知。吉西他滨联合奥沙利铂及利妥昔单抗(R-GEMOX)是针对不适合移植的复发难治DLBCL患者常用的二线化疗方案[10, 11]。MO40598研究(NCT04182204)是一项正在进行的Ⅲ 期、多中心、随机对照研究, 探讨Polatuzumab Vedotin联合R-GEMOX是否优于R-GEMOX。
尽管二线挽救化疗联合ASCT能够治愈部分年轻体力状态好的患者, 但临床上发现并非所有患者都对挽救化疗敏感。如何增加挽救化疗的有效率是目前临床的一个难题。既然Polatuzumab Vedotin在不适合移植的患者中展示出一定疗效, 是否能加入适合移植患者的挽救化疗中, 提高疗效, 增加患者接受移植的机率。实际上, 来自以色列的一项真实世界研究中, 已经在尝试对于复发难治DLBCL患者接受Pola-BR有效后再桥接ASCT或者CAR T细胞治疗[12]。后续需要开展随机对照Ⅲ 期研究, 探讨Polatuzumab Vedotin能否增加挽救化疗的有效率, 使更多患者有机会接受ASCT。
DLBCL经过一线治疗仍有部分患者复发进展, 一线如何提高DLBCL患者的疗效也是目前的研究热点。可惜的是, 既往研究中加入的新药均未能得到阳性结果[13, 14, 15]。正在进行的一项全球多中心, Ⅲ 期随机对照研究(POLARIX)中, 对比了Polatuzumab Vedotin联合R-CHP与R-CHOP治疗初治DLBCL, 该研究结果值得期待。
总之, 作为最常见的淋巴瘤亚型, DLBCL一直是新药研究的热点领域。相信随着更多新药的加入, 以及更多有意义研究结果的出现, DLBCL的预后能够真正得到改善, 使更多患者获益。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|