| 林根,医学博士,福建省肿瘤医院胸部肿瘤内科主任医师,硕士研究生导师。中国临床肿瘤学会(CSCO)患者教育专业委员会副主任委员,CSCO免疫治疗专家委员会常务委员,CSCO青年专家委员会常务委员,CSCO神经系统肿瘤专家委员会常务委员,中国南方肿瘤临床研究协会(CSWOG)肺癌专业委员会常务委员,中华医学会肿瘤学分会肺癌学组委员,中华医学会肿瘤学分会青年委员会委员,中国抗癌协会青年理事会常务委员,中国抗癌协会化疗专业委员会委员;福建省抗癌协会肺癌专业委员会副主任委员,福建省抗癌协会免疫治疗专业委员会副主任委员,福建省抗癌协会肿瘤内科专业委员会常务委员兼秘书,福建省抗癌协会肺癌专业委员会青年委员会主任委员,福建省抗癌协会肿瘤内科专业委员会青年委员会主任委员。《J Clin Oncol》审稿专家、《J Clin Oncol中文版-肺癌专刊》编委会委员。主持多项国家自然基金面上项目及省部级课题;以第一作者和/或通讯作者在《Ann Oncol》、《J Thorac Oncol》等杂志发表论文60余篇。 |
Rudin CM, Awad MM, Navarro A, et al. Pembrolizumab or placebo plus etoposide and platinum as first-line therapy for extensive-stage small-cell lung cancer: Randomized, double-blind, phase Ⅲ KEYNOTE-604 study[J]. J Clin Oncol, 2020, 38(21):2369-2379.
1b。
依托泊苷联合铂类是广泛期小细胞肺癌(extensive-stage small-cell lung cancer, ES-SCLC)一线标准治疗方案之一。帕博丽珠单抗单药在小细胞肺癌中显示出抗肿瘤活性。
比较帕博丽珠单抗联合依托泊苷和铂类(etoposide and platinum, EP)治疗ES-SCLC的无进展生存期(progression-free survival, PFS)和总生存期(overall survival, OS)是否优于EP单纯化疗。
• 研究条件:来自美国、西班牙等18个国家140个研究中心参加的临床研究(NCT03066778)。
• 研究时间:2017年5月15日至2018年7月30日。
• 研究方法:多中心、随机、双盲、安慰剂对照的Ⅲ 期临床试验。
• 研究对象:从未接受过治疗的Ⅳ 期SCLC, 如果患者有脑转移灶, 要求脑部病灶治疗后稳定≥ 14天。
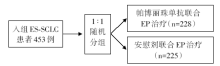
• 干预措施:入组患者按1∶ 1比例随机分配至帕博丽珠单抗联合EP治疗组或安慰剂联合EP治疗组, 见图1。
• 评价指标:主要研究终点为PFS和OS; 次要研究终点为客观缓解率(objective response rate, ORR)和缓解时间(duration of response, DOR)。
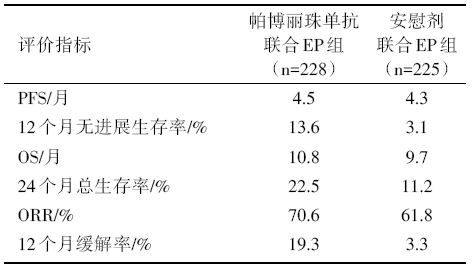
共入组ES-SCLC患者453例, 两组的基线特征均衡。帕博丽珠单抗联合EP治疗组较安慰剂联合EP组显著改善PFS[风险比(hazard ratio, HR) 0.75; 95%CI 0.61~0.91, P=0.002 3]。虽然帕博丽珠单抗联合EP组较安慰剂联合EP组可改善OS, 但未达到统计学差异(HR 0.80; 95%CI 0.64~0.98, P=0.016 4)。帕博丽珠单抗联合EP组较安慰剂联合EP组提高ORR、12个月无进展生存率/缓解率及24个月总生存率, 见表1。
| 表1 KEYNOTE-604主要研究结果 |
帕博丽珠单抗联合EP组3~4级不良反应发生率76.7%, 5级不良反应率为6.3%; 安慰剂联合EP组为74.9%和5.4%。
帕博丽珠单抗联合EP组一线治疗广泛期SCLC, 较安慰剂联合EP组改善PFS。帕博丽珠单抗联合EP组未发生非预期的不良反应。
近几十年来, 小细胞肺癌治疗效果及方式进步有限, 两项Ⅲ 期临床研究IMpower133[1]、CASPIAN[2]证实了化疗联合免疫检查点抑制剂能够改善广泛期小细胞肺癌的总生存, 由此广泛期小细胞肺癌的治疗进入了一个新的发展阶段。
同样是免疫联合化疗, KEYNOTE-604这一Ⅲ 期临床研究却是一个阴性结果。我们把KEYNOTE-604、IMpower 133、CASPIAN这三个研究放在一起比较一下:(1)在研究设计方面, IMpower 133、KEYNOTE-604研究终点为双终点PFS和OS, 而CASPIAN为OS单个终点; IMpower133、KEYNOTE-604为随机双盲的Ⅲ 期临床研究, 而CASPIAN为开放性的研究; 在统计学方面, KEYNOTE-604采用的是单侧有效性检验, 这与其他两个研究也有所不同。(2)在入组人群的基线特征上, KEYNOTE-604入组患者ECOG评分更差, 更多的患者存在基线脑转移(14.5% vs. 8.5% vs. 10.4%)。(3)从研究结果看, 三个临床研究结果具有非常相似的一面, 在前面的6~8个月, 试验组和对照组的PFS曲线在前6~8个月左右均没有分开, 后期才逐渐分开, 这提示我们可能只有一小部分小细胞肺癌患者能从免疫治疗中获益; 从长期生存获益上看, 三个研究均显示试验组1年生存率约50%、2年生存率约20%, 说明这三个临床研究结果均有临床价值, 可惜的是KEYNOTE-604研究未获得统计学显著差异。
如何看待KEYNOTE-604临床研究的阴性结果?业内部分专家认为可能是程序性死亡受体1(programmed death-1, PD-1)单抗与程序性死亡配体1(programmed death ligand-1, PD-L1)单抗的区别导致的, 但实际上, 在小细胞肺癌中, 二线nivolumab治疗[3]和三线pembrolizumab[4]都显示出抗肿瘤效应。因此, 上述三个临床研究结果的差异, 在某种程度上可能与小细胞肺癌免疫治疗获益人群范围较小、获益人群在总体入组人群的占比上的偏倚有关。
现有的资料表明:PD-L1表达和肿瘤突变负荷(tumor mutational burden, TMB)均无法作为小细胞肺癌免疫治疗的可靠疗效预测标志物。高达60%左右的小细胞肺癌属于免疫沙漠型, 高TMB、低PD-L1表达、较少肿瘤浸润免疫细胞等构成了目前小细胞肺癌免疫微环境的标签[5]。因此, 继续探明小细胞肺癌免疫微环境、多途径打破小细胞肺癌的免疫逃逸, 是未来进一步提高免疫治疗疗效的关键。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|