| 陆舜,临床医学博士,主任医师,博士研究生导师,国家科技部重点专项首席专家,国务院特殊津贴获得者,国家卫生健康突出贡献中青年专家,二级教授,上海市领军人才,上海市优秀学术带头人,上海市优秀医苑新星。目前担任上海交通大学附属胸科医院肿瘤科主任,上海市肺部肿瘤临床医学中心主任。作为第一负责人承担国家科技部重点专项、科技部国际合作课题、国家自然基金重点项目、面上项目等多项课题。2019年获得“国之名医”称号,2020年获得上海市劳模称号,2021年入选“国家卫生健康突出贡献中青年专家”。作为第一负责人获得中国抗癌协会一等奖、上海市医学科技奖一等奖、华夏医学科技奖二等奖及上海市科技进步一等奖等。 作为第一/通讯作者发表论文及论著200余篇,其中SCI收录90余篇,包括《Lancet Oncol》、《Lancet Respir Med》、《J Clin Oncol》、《Nat Commun》、《Proc Natl Acad Sci U S A》、《Ann Oncol》、《ClinCancer Res》等知名杂志,总IF值338.9。目前担任美国临床肿瘤学会(ASCO)亚太区协会中国代表、多学科诊治小组(MCMC)成员,国际肺癌研究会(IASLC)出版委员会委员,国际肺癌研究会官方杂志《J Thorac Oncol》副主编,《Lung Cancer》副主编,《Oncologist》杂志编委,中华医学会肿瘤学会委员、中国抗癌协会肺癌专业委员会主任委员、中国临床肿瘤学会(CSCO)常务理事、希斯科基金会副理事长、上海市医学会理事及肿瘤学分会主任委员等职务。作为知名专家参与多项国际肺癌指南的制定。 |
Reck M, Rodrí guez-Abreu D, Robinson AG, et al. Five-year outcomes with pembrolizumab versus chemotherapy for metastatic non-small-cell lung cancer with PD-L1 tumor proportion score ≥ 50%[J]. J Clin Oncol, 2021, 39(21):2339-2349.
1b。
KEYNOTE-024是一项随机、开放标签、Ⅲ 期临床试验, 旨在比较帕博利珠单抗单药和含铂化疗在程序性死亡蛋白配体-1(programmed cell death ligand 1, PD-L1)肿瘤比例评分(tumor proportion score, TPS)≥ 50%的非小细胞肺癌(non-small-cell lung cancer, NSCLC)初治患者中的疗效, 是首个证明了一线免疫治疗优于含铂化疗的Ⅲ 期临床试验[1]。
5年生存率是癌症治疗的重要里程碑, 由于转移性NSCLC患者的随访时间和数据至今依旧有限, 因此KEYNOTE-024研究展示的5年疗效和安全性结果弥补了这一空白。
分析KEYNOTE-024的5年生存数据, 确定免疫单药在转移性NSCLC的长期获益。
• 研究条件:来自16个国家142个研究中心参加的临床研究(NCT02142738)。
• 研究时间:2014年9月19日至2020年6月1日。
• 研究方法:多中心、开放标签, 随机对照的Ⅲ 期临床试验。
• 研究对象:PD-L1 TPS ≥ 50%的Ⅳ 期NSCLC初治患者。排除EGFR或ALK阳性突变、未经治疗的脑转移、或需系统治疗的活动期自身免疫疾病患者或已接受糖皮质激素或免疫抑制剂治疗的患者。
• 干预措施:患者按1:1比例随机分成两组, 一组接受200 mg静脉注射帕博利珠单抗, 每3周1次, 持续35个周期; 另一组由研究者选择接受铂类为基础的化疗(卡铂/顺铂)加培美曲塞或吉西他滨, 或卡铂加紫杉醇治疗4~6个周期。其中, 培美曲塞只允许用于非鳞癌患者, 可用作维持治疗。
• 评价指标:主要终点指标为无进展生存期(progression-free survival, PFS), 由盲态独立中心审查(blinded independent central review, BICR)委员会根据实体瘤疗效评价标准(Response Evaluation Criteria Solid Tumors, RECIST)v1.1进行评估。次要终点包括总生存期(overall survival, OS)和客观缓解率(由BICR根据RECIST v1.1标准进行评估)、安全性和耐受性等指标。
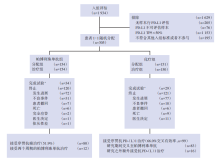
本研究共纳入305例患者, 随机分成接受帕博利珠单抗单药治疗组(n=154)和化疗组(n=151; 图1)。从随机分组到数据截止(2020年6月1日)的中位时间为59.9个月(55.1~68.4个月)。初始接受化疗的患者中, 有99例接受了抗程序性死亡蛋白-1(programmed cell death-protein 1, PD-1)或PD-L1治疗, 有效交叉率达66.0%。
帕博利珠单抗治疗组中位OS为26.3个月[95%可信区间(confidence interval, CI)18.3~40.4个月], 化疗组中位OS为13.4个月(95%CI 9.4~18.3个月), 风险比(hazard ratio, HR)0.62(95%CI 0.48~0.81, 见图2)。利用Kaplan-Meier法进行的生存分析结果显示帕博利珠单抗单药组的5年总生存OS率为31.9%(95%CI 24.5~39.5), 化疗组为16.3%(95%CI 10.6~23.0)。
 | 图2 利用Kaplan-Meier法评估帕博利珠单抗单药组和化疗组的生存分析 注:对每个治疗组的最后一次访视时存活或失访患者进行数据审核, 并用Kaplan-Meier法估算OS。图上的生存曲线上的标记(小栅栏)为删失时间点 |
除达到完全缓解(complete response, CR)或部分缓解(partial response, PR)的患者有生存获益之外, 疾病稳定(stable disease, SD)患者的OS也有获益。探索性分析显示, 帕博利珠单抗单药组和化疗组达到SD患者的中位OS分别为21.1个月(95%CI 14.1~34.5)和14.5个月(95%CI 8.9~21.1)。更进一步的探索性分析发现帕博利珠单抗单药组患者中因治疗相关不良事件(treatment-related adverse events, TRAE)导致治疗停止的21例患者中位OS为35.9个月(95%CI 7.9~未达到), 5年生存率为35.1%(95%CI 15.7~55.3)。
帕博利珠单抗治疗组TRAE发生率为76.6%(3~5级, 31.2%), 化疗组为90.0%(3~5级, 53.3%)。在帕博利珠单抗单药组和化疗组中, 分别有22.7%和20.7%的患者发生了严重TRAE; 34.4%(3~5级, 13.6%)和5.3%(3~5级, 0.7%)的患者发生了免疫介导的不良反应和输液反应。长期随访期间并没有发现新的安全性信号。
在初始接受帕博利珠单抗单药治疗的151例患者中, 39例(25.8%)完成了35个周期治疗, 82.1%患者有缓解(RECIST v1.1评估)。完成35个周期帕博利珠单抗单药治疗后36个月(即大约5年)的生存率仍为81.4%(95%CI 64.7~90.7)。完成35个周期治疗的患者发生TRAE与本研究总人群TRAE发生率一致。
帕博利珠单抗单药一线治疗转移性NSCLC(PD-L1 TPS≥ 50%)患者, 相比化疗可提供持久且具有临床意义的生存获益, 已成为这部分人群的标准治疗方案。
KEYNOTE-024研究[1], 最早于2016年欧洲肿瘤内科学会(European Society for Medical Oncology, ESMO)公布随访11.2个月的研究数据, 并同步发表在《N Engl J Med》, 首次发现免疫单药在PD-L1 TPS ≥ 50% 转移性NSCLC一线治疗中, 无论PFS还是客观缓解率(objective response rate, ORR)均显著优于含铂化疗方案, 并具有更低的毒副作用。该研究是继IPASS研究[2]开启靶向治疗时代, 取代含铂化疗成为驱动基因突变阳性NSCLC患者一线治疗选择后, 成功改变驱动基因阴性PD-L1 TPS≥ 50% NSCLC一线治疗成为首选方案的研究, 免疫单药改写NSCLC一线治疗格局。同时PD-L1检测也被国内外各大指南[3, 4]列入与EGFR突变、ALK和ROS1融合等驱动基因检测并列的生物标志物, 用于指导临床治疗决策, 开启免疫精准时代。
时至今日, KEYNOTE-024研究, 是目前唯一一个在免疫治疗针对晚期肺癌一线证实5年生存率大幅提升的Ⅲ 期研究。中位随访时间59.9个月, 在含铂化疗组有效交叉率高达66.0%的前提下, PD-L1高表达患者帕博利珠单抗组的5年总生存率为31.9%, 近似于含铂化疗组(16.3%)的2倍, 帕博利珠单抗组的中位OS(26.3个月)较含铂化疗组(13.4个月)相比也几乎翻倍(HR 0.62, 95%CI 0.48~0.81)。5年生存率一直是癌症治疗的关注点, 也具有里程碑意义, 帕博利珠单抗单药的5年总生存率确实令人振奋, 与之前KEYNOTE-001研究[5]公布的PD-L1高表达初治人群的5年生存率(29.6%)一致, 证明免疫单药极大改善NSCLC预后并再次验证长期疗效, 进一步稳固帕博利珠单抗单药在PD-L1高表达NSCLC人群的优选地位。与此同时KEYNOTE-024研究也带给临床更多思考, 免疫治疗模式必须树立长生存理念, 强调坚持评估OS的重要性。
探索分析也带给临床更多提示, 达到SD的患者较含铂化疗相比同样可以从帕博利珠单抗治疗中得到OS获益(21.1个月 vs. 14.5个月)。帕博利珠单抗单药治疗组因TRAE而早期停止治疗的患者生存获益没有受到影响, 仍然可以从帕博利珠单抗单药治疗中获益(中位OS 35.9个月, 5年生存率35.1%)。通过对39例完成35个周期帕博利珠单抗单药治疗的患者进行分析, 中位OS可达35.7个月, 在数据截止时有32例患者仍然存活, 完成35个周期治疗后36个月(近似5年)总生存率为81.2%, 46.2%的患者在没有PD或后续治疗的情况下存活, 这部分数据提示, 帕博利珠单抗用满两年的患者可以有非常好的预后, 即便后续停药依然有81.9%的5年总生存率。在12例随后进展并接受第二疗程帕博利珠单抗治疗的患者中, ORR为33.3%, 持续缓解率为83.3%, 数据截止时有66.7%患者存活, 帕博利珠单抗再挑战同样可行, 用药满两年和再挑战患者的安全性与研究总人群保持一致, 这样的结论在帕博利珠单抗联合化疗的Ⅲ 期临床中也类似[6, 7]。长期随访中没有发现新的安全信号, 帕博利珠单抗长期应用的安全性得到验证, 结合持久获益特点, 与既往报道的帕博利珠单抗可以改善或维持患者健康相关生活质量(health-related quality of life, HRQoL)相一致[8]。
毫无疑问KEYNOTE-024研究结果给临床带来巨大震撼, PD-L1 TPS≥ 50%驱动基因阴性NSCLC人群帕博利珠单抗单药即可带来生存获益。免疫联合化疗在非鳞(KEYNOTE-189)[9]和鳞状(KEYNOTE-407)[10]转移性NSCLC人群中不受PD-L1表达影响, 较含铂化疗相比显示出OS和PFS的显著获益, 针对其中PD-L1 TPS≥ 50%的人群, 间接比较上述研究, 在免疫治疗的基础上化疗的加入似乎并未改善OS, 仅提高了ORR和PFS[6, 9, 10], 迄今为止尚未有头对头研究给临床带来更多提示, 探索优化驱动基因阴性NSCLC一线免疫治疗模式任重而道远。同时以免疫治疗为基石的探索层出不穷, 包括抗PD-(L)1药物, 无论是单药治疗, 还是联合化疗、放疗、抗血管生成药物、抗细胞毒T淋巴细胞相关抗原4(cytotoxic T lymphocyte-associated antigen 4, CTLA-4)药物及其他免疫激活或抑制新靶点(beyond PD-1/L1)药物等的组合模式, 双特异性抗体和抗体偶联药物(antibody-drug conjugate, ADC)等。不满足于此, 对于驱动基因阳性NSCLC人群, 我们也想知道相应酪氨酸激酶抑制剂(tyrosine kinase inhibitor, TKI)药物耐药后免疫联合化疗是否比单纯化疗效果更好, 专门针对这部分人群的KEYNOTE-789[11]等研究在试图回答这一问题。此外, 超越PD-L1的免疫相关生物标志物, 也是精准时代进一步探索的方向。
中共中央、国务院印发《“ 健康中国2030” 规划纲要》[12]中提出, 到2030年, 总体癌症5年生存率要提高15%。除了改善患者治疗现状之外, 还应关注创新药的可及性和药物价格等方面, 共促2030年目标。KEYNOTE-024研究5年随访结果, 无疑增加了信心, 31.9%的5年总生存率, 意味着近三分之一的患者可以活过五年, 帕博利珠单抗单药带来的长生存, 引领肺癌逐渐走向“ 慢病化” 时代, 具有划时代的意义, 将使中国肺癌患者的长期生存得到极大的改善。此外, 无论在全球还是在中国, 帕博利珠单抗是目前所有免疫治疗当中获批适应证最多的免疫检查点抑制剂, 肺癌领域KEYNOTE系列多个大型Ⅲ 期临床都取得阳性结果和长随访数据, 同样也是肺癌循证医学证据最多的免疫药物, 单药和联合化疗方式已经成为NSCLC一线治疗标准和首选。未来期待帕博利珠单抗能在局部晚期和早期肺癌中有更多更惊艳的数据, 更重要的是, 希望帕博利珠单抗有更多来自中国的研究数据或真实世界数据, 更好的阐明药物对中国患者的获益, 造福更多中国患者。
致谢:感谢默沙东(中国)投资有限公司胡佳骅和延艳为本文翻译提供学术支持, 感谢上海北翱医药科技有限公司为本文提供辅助编辑工作, 及默沙东(中国)投资有限公司的支持。
编者说明:本文原文“ Five-year outcomes with pembrolizumab versus chemotherapy for metastatic non-small-cell lung cancer with PD-L1 tumor proportion score ≥ 50%” , 首次发表在《J Clin Oncol》, 2021, 39(21):2339-2349, 本次二次发表已取得首次发表期刊的版权转让书, 对原文部分内容进行摘译, 不涉及一稿多投及侵犯版权等问题。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|