| 东省“三八”红旗手,首届“羊城好医生”获得者。现任中华医学会消化内镜分会委员,中国医师协会消化医师分会委员,广东省医师协会消化内镜医师分会主任委员、广东省医学会消化病学分会副主任委员及《中华消化内镜杂志》《Gastroenterology》《GUT》等国内外消化权威杂志编委。毕业于中山医科大学全英班并相继取得硕士、博士学位,曾在日本崎玉省立肿瘤医院消化内镜中心、香港威尔士亲王医院内镜中心进修,并在美国德州大学医学分部(University of Texas Medical Branch,UTMB)消化内科从事博士后研究工作。承担国家自然科学基金、广东省自然科学基金及广东省人民医院登峰计划重大项目等各种科研课题10余项,获广东省、广州市科技进步奖5项,在国内外核心杂志上发表论文100余篇,其中包括在顶级医学期刊《Br Med J》及《Lancet》子刊《EClinicalMedicine》上发表研究论文。致力于消化系统疾病的临床、教学和科研工作,洞悉本专业领域国内外研究动向,尤其擅长胃食管反流病、消化性溃疡出血等胃酸相关性疾病,功能性胃肠病,炎症性肠病的诊断与治疗以及内镜下球囊扩张、支架放置、胆总管取石、套扎及注射止血、息肉切除等各种治疗。 |
Choi IJ, Kook MC, Kim YI, et al. Helicobacter pylori therapy for the prevention of metachronous gastric cancer[J]. N Engl J Med, 2018, 378(12):1085-1095.
1b。
早期胃癌患者胃粘膜通常具有腺体萎缩、肠化生等癌前病变发生, 因此内镜下切除术后胃内其余部位仍有新发胃癌(异时性胃癌)的风险。
根除幽门螺杆菌对改善胃粘膜组织学改变及预防异时性胃癌的作用仍存在争议。
评估根除幽门螺杆菌对预防异时性胃癌及改善胃粘膜组织学变化的有效性。
• 研究条件:韩国国立癌症中心的临床研究项目(NCT02407119)。
• 研究方法:单中心、双盲、随机对照临床试验。
• 研究时间:2003年8月至2013年3月。
• 研究对象:经内镜活检诊断明确且已安排内镜下切除的早期胃癌或高级别上皮内瘤变患者, 伴有幽门螺杆菌感染、无淋巴结或器官转移, 年龄18~75岁。
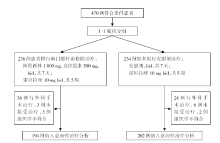
• 干预措施:阿莫西林、克拉霉素、雷贝拉唑方案根除幽门螺杆菌治疗7天, 雷贝拉唑额外使用4周以促进溃疡愈合, 具体干预措施见图1。
点指标包括异时性腺瘤发生率、总生存率(overall survival, OS)等。
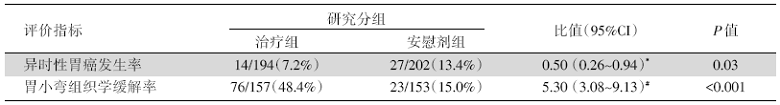
研究共入组396例早期胃癌患者, 中位随访时间为5.9年。组织学评估共纳入327例患者。研究终点指标详见表1和表2。
| 表1 主要研究终点 |
| 表2 次要研究终点 |
幽门螺杆菌根除治疗可降低早期胃癌患者异时性胃癌发生率并改善粘膜组织学改变。
早期胃癌指癌组织浸润局限于粘膜或粘膜下层, 无论是否伴有淋巴结转移; 其预后显著优于进展期胃癌[1]。早期胃癌的治疗主要有内镜下治疗及外科手术治疗。研究证明, 经内镜下粘膜剥离术(endoscopic submucosal dissection, ESD)治疗的早期胃癌患者, 其5年生存率超过90%[2]。但是, 大量研究发现, 因早期胃癌患者胃粘膜通常存在癌前病变, 包括胃粘膜萎缩、肠上皮化生和不典型增生等, 在行内镜下胃早癌切除治疗后, 仍可能在其余部位新发胃癌(亦称为异时性胃癌)。
世界卫生组织国际癌症研究署(World Health Organization, WHO/International Agency for Research on Cancer, IRAC)将幽门螺杆菌归类为Ⅰ 类致癌物[3]。幽门螺杆菌感染与腺体萎缩及不典型增生、肠上皮化生等癌前病变高度相关[4]。根除幽门螺杆菌对改善胃粘膜组织学及预防异时性胃癌的作用尚无定论。在本研究之前, 既往研究受限于研究设计、样本量及随访时间等的缺陷, 导致结论存在争议。其中, 既往两项相关临床试验均为开放性研究, 且未排除可能漏诊的于入组1年内发生同时性胃癌的患者[5, 6]。本研究基于随机、双盲设计, 一定程度上避免了偏倚及混杂因素, 较有力地证明了根除幽门螺杆菌对降低早期胃癌患者异时性胃癌发生率、改善组织学改变的有效性, 对胃癌尤其是异时性胃癌的防治策略具有积极意义。
该文章尚存在一些不足之处:(1)研究样本量不大, 仅为单中心研究, 结论仍需大样本、多中心的双盲、随机对照研究进一步确认; (2)研究除早期胃癌患者外, 亦纳入了高级别瘤变患者; (3)发表于《BMJ》的一项网状荟萃分析证实, 文章所使用的标准7天三联疗法(克拉霉素和阿莫西林/甲硝唑联合质子泵抑制剂)根除幽门螺杆菌的有效性较低[7]。本研究中治疗组幽门螺杆菌根除率就仅有80.4%。如果采用Maastricht Ⅳ / Florence共识意见推荐的延长疗程方案或者我国指南推荐的含铋剂四联14天疗法, 提高了幽门螺杆菌的根除率, 是否可以进一步降低异时性胃癌发生率及改善粘膜组织学改变尚不明确。尽管该研究有待完善之处, 但仍然为临床提供了有力的证据支持根除幽门螺杆菌可以降低早期胃癌ESD术后异时性胃癌的发生, 目前已被纳入多项国内、国际专家共识及指南。
既往研究关于根除幽门螺杆菌对改善腺体萎缩及肠上皮化生的作用仍存在争议[8]。有研究显示在部分人群中, 当不存在肠上皮化生时根除幽门螺杆菌, 可以逆转胃腺体萎缩, 阻止癌前病变演变为癌变[9]。而该研究证明了根除幽门螺杆菌对胃小弯肠上皮化生具有一定的改善作用。但是, 对于胃大弯处腺体萎缩及肠化, 根除幽门螺杆菌仅显著改善萎缩, 而对于肠化的改善没有显著的统计学意义。由此可见, 根除幽门螺杆菌对于胃粘膜不同部位癌前病变的改善作用仍需进一步研究证实。另外, 该研究还显示, 虽然根除幽门螺杆菌降低了异时性胃癌的发生, 但治疗组总体的生存率较对照组并无明显提高(治疗组5年总生存率97.0%; 对照组5年总生存率98.2%)。可能原因与异时性胃癌发生率低, 且经研究定期随访、及时发现异时性胃癌并规范治疗, 患者预后仍较好有关。尽管在总生存率指标中并未观察到统计学差异, 但根除幽门螺杆菌对于减轻早癌患者心理、经济负担及提高远期生活质量的意义重大。
综上所述, 对于筛查及临床实践中发现的早期胃癌患者, 需高度警惕内镜下切除后异时性胃癌发生。对于伴有幽门螺杆菌感染的早期胃癌患者, 根除幽门螺杆菌可显著降低异时性胃癌的发生, 制定系统、科学的治疗方案及随访策略将对胃癌患者的规范管理产生积极的影响。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|