| 张必翔,主任医师,博士生导师,华中科技大学同济医学院附属同济医院普通外科主任,国家卫生健康突出贡献专家。兼任国际肝胆胰协会委员、亚太肝胆胰协会会员委员会委员、亚太肝脏外科发展委员会委员、国际肝胆胰协会中国分会MDT专业委员会主任委员、中国稀土学会稀土生物医学委员会副主任委员、中国医师协会外科医师分会肝脏外科专业委员会副主任委员、中国研究型医院学会智能医学专业委员会副主任委员、中国医药教育学会肝胆胰外科专业委员会副主任委员、中国腹腔镜肝切除发展与推广委员会副主任委员、武汉市普通外科学会副主任委员。 主要研究方向为肿瘤器官特异性转移的分子机制及靶向干预。擅长复杂困难的肝癌切除术、肝门胆管癌根治术、胰十二指肠切除术及临床肝移植。主持国家自然科学基金面上项目5项,科技部重大专项子课题1项、国家重点研发计划子课题1项、湖北省科技创新重大项目1项。以第一作者或通信作者在《Gastroenterology》《Hepatology》《J Hepatology》等国际知名期刊发表SCI收录论文70余篇。作为第一完成人获湖北省科技进步奖一等奖1项、作为主要完成人获中国抗癌协会科技进步奖一等奖等多项奖励。 |
Chen J, Lu L, Wen T, et al. 2021 ESMO 945P - Adjuvant lenvatinib in combination with TACE for hepatocellular carcinoma patients with high risk of postoperative relapse (LANCE): Updated results from a multi-center prospective cohort study[J]. Ann Oncol, 2021, 32(5S): S818-S828.
2a。
目前手术切除是我国治疗肝细胞癌(hepatocellular carcinoma, HCC)的主要手段, 但术后高复发风险是目前面临的主要挑战。对于高复发风险的HCC患者, 肝动脉化疗栓塞术(transarterial chemoembolization, TACE)作为辅助治疗虽然可减少肿瘤复发, 延长无病生存期(disease-free survival, DFS)和中位总生存期(overall survival, OS), 但其疗效仍不尽如人意。目前尚无标准辅助治疗来降低HCC患者术后复发风险。仑伐替尼是一种多靶点受体酪氨酸激酶抑制剂(tyrosine kinase inhibitor, TKI), 用于晚期HCC患者的一线治疗。
评估仑伐替尼联合TACE相较于TACE辅助治疗肝癌切除术后高复发风险患者的疗效和安全性。
• 研究条件:计划纳入240例患者参与的研究(NCT03838796)。
• 研究方法:多中心、前瞻性、队列研究。
• 研究时间:2019年1月至2023年6月。
• 研究对象:病理确诊为HCC, 无仑伐替尼治疗或过敏史, 术后复发风险高, 年龄18~75岁, ASA评分Ⅰ ~Ⅲ 级, Child Pugh A级, 其余各器官功能良好。术后复发风险高的标准包括:伴有大血管或胆管侵犯(门静脉、肝静脉或胆管癌栓), 肿瘤破裂或侵犯邻近器官, 二级微血管侵犯(microvascular invasion, MVI, M2)合并以下三种情形之一:肿瘤数目≥ 3、肿瘤最大直径≥ 8 cm、边界不清, 包膜不完整。
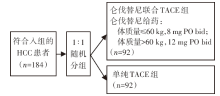
• 干预措施:本研究目前共纳入184例患者, 分为仑伐替尼+TACE组(联合组)和TACE组, 每组92例。仑伐替尼给药:体质量≤ 60 kg, 8 mg PO bid; 体质量> 60 kg, 12 mg PO bid。TACE:切除术后1个月行肝动脉造影, 观察有无肿瘤染色。如有可疑的肿瘤染色, 微导管超选至肿瘤血管, 注射栓塞剂和化疗药物。如未见明显肿瘤染色, 则缓慢注入少量栓塞剂, 见图1。
• 评价指标:主要终点指标为DFS; 次要终点指标为OS和至肿瘤复发时间(time to recurrence, TTR)。
入组联合组患者中位年龄为53岁(23~78岁), 大部分为男性患者(87.0%), 其中, 74例患者有HBV病史(80.4%), 两组患者的基线临床病理特征均衡, 包括性别、年龄、HBV病史、肝功能、肿瘤特征和AFP水平等。
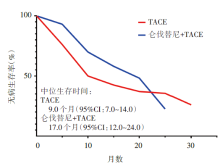
联合组的中位DFS为17.0个月[95%可信区间(confidence interval, CI)12.0~24.0], 显著优于TACE组9.0个月(95%CI 7.0~14.0), P=0.022 8[风险比(hazard ratio, HR)0.6, 95%CI 0.4~1.0)], 见图2。OS及TTR未达到。联合组最常见的3/4级不良事件(≥ 5%)包括:高血压(19.6%)、腹泻(15.2%)、牙龈出血(13.0%)、手足皮肤反应(8.7%)、关节痛(5.4%)及肝功能受损(5.4%)。
对于术后高复发风险的HCC患者, 仑伐替尼联合TACE比单纯TACE延长了DFS, 且联合组未出现预期外的其他安全事件。
手术切除是肝细胞癌(HCC)的一种最重要的治疗手段。在我国, 除了对早期的肝癌(中国肝癌临床分期CNLC-Ⅰ 期)进行手术, 对于CNLC-Ⅱ b甚至Ⅲ A期肝癌患者, 手术切除也是可选择的治疗方案之一。但术后高复发和转移是治疗的主要挑战。术后辅助治疗的手段以降低术后复发转移尤为重要。然而到目前为止的各大HCC诊疗指南中, 除了病毒性肝炎相关HCC患者使用抗病毒药物辅助治疗, 其它的术后辅助治疗手段均未得到充分的认可和采纳。既往的几项研究, 包括本中心牵头的一项多中心随机对照试验(randomized control trial, RCT)研究在内的研究结果提示术后辅助TACE治疗[1]以及中医药治疗(槐耳颗粒)[2]可为术后高危复发风险的HCC患者带来一定获益, 但靶向药物及程序性死亡受体1(programmed death 1, PD-1)/程序性死亡配体1(programmed death ligand 1, PD-L1)抑制剂在内的系统治疗药物在HCC术后辅助治疗中的疗效还缺乏相关循证医学证据。
索拉非尼作为第一个临床应用于HCC的靶向治疗药物, 以它为基础药物作为HCC术后辅助治疗探索的STORM研究结论认为HCC术后使用索拉非尼不能使患者有生存获益[3]。目前在晚期HCC患者的系统治疗中, 新的靶向治疗药物和治疗方案不断涌现, 因此, 目前探索适合于肝癌术后辅助治疗的治疗药物和治疗方案是必要而时机成熟的。
复旦大学华山医院在钦伦秀教授带领下联合国内多家中心发起的LANCE研究, 是一项术后采用仑伐替尼联合TACE对比单纯TACE治疗术后高危复发风险患者的前瞻性队列研究。在研究人群的选择上, LANCE研究与STORM研究不同, LANCE研究根据现有的已证明术后复发高危风险相关因素为基础筛选术后高危复发人群作为研究人群, 较之STORM研究将所有行肝切除的HCC患者纳入研究更为合理, 因已有数据表明早期HCC行规范切除后即使不进行辅助治疗, 五年生存率也在70%以上, 对于这部分患者, 目前的治疗共识为仅需对有高危复发风险的患者进行早期干预。在具体辅助治疗的选择上, LANCE研究的试验组给药方案为TACE联合仑伐替尼治疗, 是在已有研究结论证明TACE对高危复发HCC患者的有效性的基础上进一步探索联合仑伐替尼的效果。2020年美国临床肿瘤学会(American Society of Clinical Oncology, ASCO)会议上, LANCE研究的初步结果公布:单纯TACE治疗组中位DFS约为8个月, 但TACE联合仑伐替尼组中位DFS可延长至12个月, 两组结果有显著差异。在今年的欧洲肿瘤内科学会(European Society for Medical Oncology, ESMO)年会上, LANCE研究公布了扩大样本量的研究结果同样令人惊喜, 单纯TACE组DFS为9个月, 而联合治疗组达到了17个月。然而该研究并未涉及以PD-1/PD-L1单抗为基础的免疫治疗在HCC术后辅助治疗中的应用探索。鉴于目前免疫治疗在晚期HCC患者中的治疗前景, 笔者相信在未来, 类似LANCE研究这样的全国多中心前瞻性队列研究也会开展用于探索免疫治疗在HCC高危复发人群中的疗效。
| [1] |
|
| [2] |
|
| [3] |
|