| 金浩生,外科学博士,副主任医师,硕士生导师,广东省人民医院肝胆外科行政副主任(主持工作),外科第一党支部书记。兼任广州市抗癌协会肝胆胰肿瘤专业委员会副主任委员、广东省基层医药协会肝胆胰微创分会副主任委员、广东省健康管理学会肿瘤防治专业委员会副主任委员、广东省医学会肝癌分会常务委员、中国研究型医院学会肝胆胰外科专业委员会肝癌学组常务委员、广东省医学会外科分会青年委员会常务委员、广东省肝脏病协会胆胰分会委员、广东省高层次人才评审专家。 在临床一线从事普通外科及肝胆外科专业20余年,擅长肝胆疾病的微创治疗,肝胆肿瘤的综合治疗,近年采用以转化手术为目标,联合免疫靶向等系统综合的方法治疗肝胆恶性肿瘤,极大地提高患者5年生存率,取得良好疗效。 曾获“中华外科青年学者奖”,主刀手术视频获得“全国中青年医师腔镜肝脏手术视频决赛”第一名,近年主持广东省自然科学基金等项目5项。以第一作者及通讯作者发表SCI论文10余篇。 |
Xia Y, Wang P, Pu L, et al. Preliminary efficacy and safety of perioperative treatment of camrelizumab combined with apatinib in resectable hepatocellular carcinoma (HCC):A prospective phase Ⅱ study[J]. J Clin Oncol, 2021, 39(15S):Abstr4082.
2b。
肝切除术(liver resection, LR)是肝细胞癌(hepatocellular carcinoma, HCC)的主要治疗选择; 然而, 仅10%~20%患者诊断为可切除性HCC, 可切除性HCC患者进行手术切除后, 5年内复发率为80%。新兴证据显示, 新辅助程序性死亡受体1(programmed death 1, PD-1)阻断治疗在各癌种中均有良好应用, 可用于肿瘤降期、消除微转移灶及预防复发, 但对于肝细胞癌的新辅助或辅助治疗, 目前暂无全身性疗法获批。卡瑞利珠单抗(camrelizumab)联合阿帕替尼(apatinib)在不可切除HCC患者的治疗中显示出令人鼓舞的疗效, 但目前尚缺乏在可切除HCC中应用的试验。
单中心、单臂Ⅱ 期临床试验, 旨在评估卡瑞利珠单抗联合阿帕替尼用于可切除HCC围手术期治疗的有效性与安全性。
• 研究方法:本研究单中心、单臂Ⅱ 期临床试验(NCT04297202)。
• 研究对象:纳入标准包括年龄≥ 18岁, 经组织学或细胞学证实为可切除HCC, 根据实体瘤疗效评价标准(Response Evaluation Criteria in Solid Tumor, RECIST v1.1/mRECIST)有≥ 1个可测量病灶, 未经系统治疗, ECOG PS 0或1, 足够器官功能。排除标准:已知或疑似患有活动性自身免疫性疾病/感染性疾病, 临床显著的并发症/癌症。
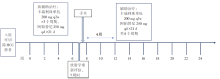
• 干预措施:选取未行系统治疗且符合外科切除标准的患者, 按照卡瑞利珠单抗200 mg q2w× 3个周期, 阿帕替尼250 mg qd× 21 d, 进行治疗, 第7周影像评估证实仍符合外科切除标准, 行外科切除术, 术后4周开始给予卡瑞利珠单抗(200 mg q3w)、阿帕替尼(250 mg qd 3周/周期× 8个周期)治疗, 研究设计流程见图1。
• 研究终点:主要研究终点指标为主要病理缓解(major pathologic response, MPR), 定义为切除组织中50%~99%肿瘤坏死。次要研究终点指标包括病理完全缓解(pathologic complete response, pCR)、客观缓解率(objective response rate, ORR)、无复发生存期(relapse-free survival, RFS)、不良事件(adverse events, AE)及围手术期并发症等。探索性研究终点为自定义289个免疫相关基因的基因表达谱分析。
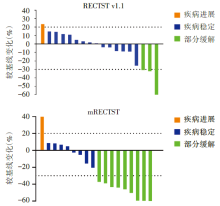
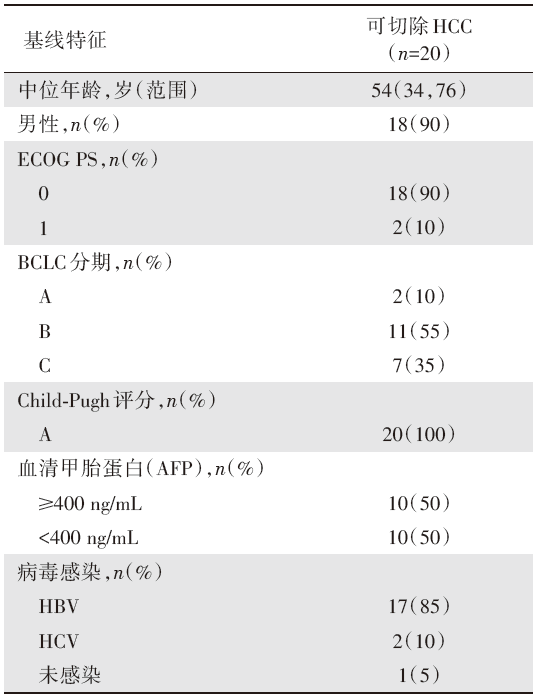
18例患者完成切除术前卡瑞利珠单抗及阿帕替尼治疗; 2例患者于切除术前治疗期间/后退出, 18例纳入疗效分析。5例(29.4%)达到MPR。RECIST评价患者缓解情况见图2。患者的基线特征见表1。
| 表1 基线特征 |
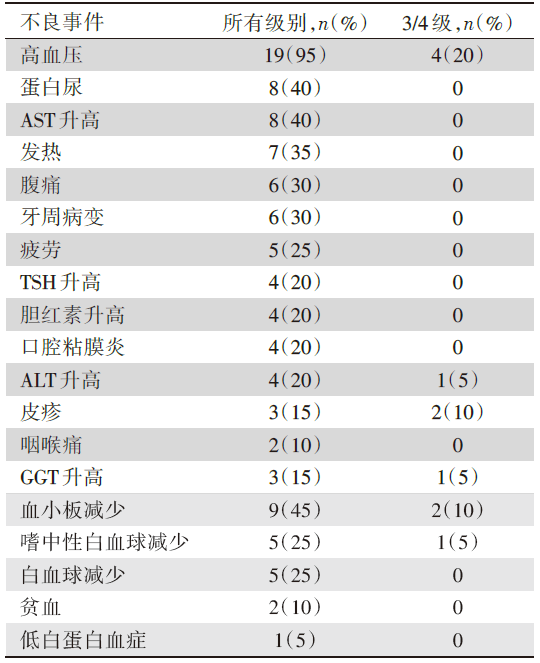
另外, 1例(5.9%)达到pCR, ORR分别为16.7%(RECIST v1.1)和44.4%(mRECIST), 1例发生疾病进展; 17例(94.4%)接受切除术。中位随访时间5.7(0.7~9.0)个月; 中位RFS未达到。所有患者均发生AE, 8例(40%)发生3/4级治疗引发的AE(treatment emergent AE, TEAE); 最常见不良事件为高血压(95%)、血小板减少(45%)、蛋白尿(40%)及AST升高(40%)。16例患者出现围手术期并发症, 最常见为ALT升高(87.5%)、AST升高(87.5%)、LDH升高(37.5%)。AE的安全性汇总见表2。
| 表2 安全性汇总 |
在可切除HCC患者中, 卡瑞利珠单抗联合阿帕替尼用于围手术期治疗的MPR为29.4%, 且安全性可管理。
肝细胞癌(HCC)是全球常见的恶性肿瘤之一, 其发病率和死亡率分别居世界第7位和第2位, 严重威胁人类的健康和生命。HCC是原发性肝癌中最常见的病理类型, 占比75%~85%[1]。目前HCC的根治性治疗手段主要有手术切除、肝移植以及射频消融等。然而, HCC的长期预后仍然不佳, 其主要原因是相当部分患者诊断时即为晚期而失去手术机会, 而且手术后患者肿瘤复发率亦较高[2, 3]。
近年来, 肝癌的全身系统性治疗取得显著进展, 尤其是免疫检查点抑制剂联合抗血管生成靶向药物如酪氨酸激酶抑制剂、贝伐珠单抗等方案, 在不可切除进展期肝癌的治疗中取得了令人鼓舞的结果。其中, T+A方案即阿替利珠单抗联合贝伐珠单抗治疗不可切除肝癌, 1年生存率可达67.2%, 客观反应率达33.2%[4]; 帕博利珠单抗联合仑伐替尼(可乐组合)方案治疗BCLC-B/C期(29例/71例)肝细胞癌, 中位生存期可达22个月, 客观反应率达到46%[5]。
随着全身系统性治疗的快速发展, 系统治疗在可切除肝癌术前新辅助治疗中的效果, 也有研究进行探索。一项Ⅱ 期临床试验, 研究了纳武利尤单抗联合伊匹木单抗用于切除肝细胞癌的治疗, 该研究中期报道入组病例17例, 可分析病例14例中有4例(29%)达到病理完全缓解, 未发现4级毒副反应病例, 未出现因术前治疗延误手术的病例[6]。同时, 仍有多项clinical trials网站注册的临床研究在探讨术前系统治疗在可切除肝癌术前治疗中的作用, 如纳武利尤单抗联合卡博替尼方案(NCT03299946)和帕博利珠单抗联合伦伐替尼等, 结果尚未发表。总体来说, 可切除肝癌新辅助治疗相关研究仍处在初始探索阶段, 目前可参考的数据仍十分有限。
本文评论的文献也是将研究问题聚焦到可切除肝癌的术前新辅助治疗, 是一项前瞻性、开放、单臂、单中心的Ⅱ 期临床研究(NCT04297202), 将卡瑞利珠单抗联合阿帕替尼应用于可切除HCC患者的围手术期治疗以评估其有效性与安全性。目前报道了18例完成疗效评价的HCC患者中17例(94.4%)接受了手术切除, 1例发生了疾病进展, MPR为29.4%, 1例达到pCR, ORR分别为16.7%(RECIST v1.1)和44.4%(mRECIST), 患者MPR为29.4%, 中位RFS未达到。所有患者均发生不良事件, 8例(40.0%)发生3/4级TEAE。该研究结果可为临床提供一定参考, 但仍有一些问题有待思考。
第一, 该研究没有详细阐明肝癌可切除的定义, 目前关于可切除的定义各个中心仍存在较大异质性。一般而言, 于亚太地区的临床外科医师更加倾向积极的手术切除治疗, 肿瘤多发、大血管侵犯、门脉高压均不是手术的绝对禁忌证[7, 8]。由于肝癌可切除定义在各个中心的异质性, 纳入标准难以统一, 目前肝癌术前新辅助治疗的研究多为单中心研究报道。
第二, 该研究为单臂、单中心, 缺乏对照组, 无法回答新辅助治疗能否改善可切除肝癌患者长期生存预后的问题; 同时, 该研究的样本量较小, 数据的代表性略显不足。
第三, 新辅助治疗存在的风险不容忽视。首先, 肝癌治疗前的组织活检, 存在穿刺术后出血、感染等风险, 若出现上述并发症可能造成治疗延迟, 甚至疾病进展风险。其次, 该研究报道的术前靶免治疗不良反应(3/4级)高达40%, 有可能造成部分患者治疗终止或者手术延迟, 甚至失去手术机会。
第四, 该研究的中位随访时间为5.7(0.7~9.0)个月, 中位RFS未达到, 目前随访时间过短, 新辅助治疗在可切除肝癌中的效果仍未明确观测到, 其研究结果的参考意义有限。
第五, 若经治疗后可切除HCC患者出现病情进展, 应该如何选择二线治疗方案, 也是需要探究的问题。针对基本状态恶化的情况(包括系统治疗相关的严重不良事件或肝功能恶化等), 可能的后续治疗选择为积极的支持对症治疗和姑息治疗; 而系统治疗未使肿瘤获得缓解, 须根据疾病进展的特征和前期的治疗方式制定个体化的治疗方案[9]。
综上所述, 对于可切除肝癌的术前辅助治疗, 依然存在较多争议和问题, 仍有待严谨、大型、多中心、随机的临床研究来明确新辅助治疗在肝癌中的地位。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|